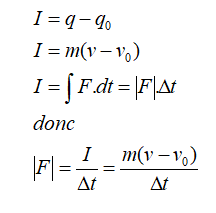masse et quantité de matière exercice
|
Calculer une quantité de matière
ρ la masse volumique s'exprime en grammes par litre (g L–1) ; V le volume du liquide s'exprime en litres (L) ; M la masse molaire s'exprime en grammes |
Quelle est la relation entre la masse et la quantité de matière ?
La formule utilisée ici est m n M = si on veut calculer une quantité de matière.
Si on veut calculer la masse, il suffit d'exprimer m : m = n × M.Comment calculer m avec m et N ?
La quantité d'une substance est parfois exprimée en nombre de particules (N).
Pour calculer la masse d'une substance (m) à partir de son nombre de particules, il faut d'abord trouver le nombre de moles (n).
Ensuite, on trouve la masse à l'aide de la formule m=nM. m = n M .Comment on calcule la quantité de matière ?
La quantité de matière d'une entité est le nombre de moles de cette entité.
Elle se note n et s'exprime en mole.
La quantité de matière n d'un élément (en mol), connaissant sa masse m (en g) et sa masse molaire M (en g·mol–1), se détermine grâce à la relation .- On reprend la formule : $n = \\dfrac{m}{M}$.
Et puisqu'on n'a pas la masse mais le volume on va « convertir » la masse en volume en utilisant la masse volumique : $ ρ =\\dfrac{m}{V}$.
On obtient alors la formule : $ n =\\dfrac{ ρ\\times V}{M}$.
|
Calculer une quantité de matière
La densité d'un liquide est le rapport entre la masse volumique de ce liquide et la masse volumique de l'eau (1 kg. EXERCICE 1.2 L'éthanol est un alcool de ... |
|
EXERCICES AUTOUR DES QUANTITÉS DE MATIÈRE
Lors de la synthèse de cette substance on utilise un volume Vol=20mL d'alcool benzylique de densité par rapport à l'eau dol=1 |
|
Cours Quantités de matière I. De la masse dune entité mentité à la
Exercice : Calculer la masse d'une molécule de dioxyde de carbone. Une molécule de dioxyde de carbone est composée de 1 atome de carbone et de 2 atomes |
|
Quantité de matière - Prophychi
On a besoin de 01 mol de sulfate de suivre hydraté de formule CuSO4(H2O)5. Quelle masse de cristaux doit-on prélever ? Un élève en a prélevé 30 |
|
Composition dun système chimique Prélever des quantités de
matière. Séquence 1. Quantité de matière masse et masse molaire. Exercice 1: Masse molaire des atomes ou ions monoatomiques. Calculer les masses molaires en |
|
Chapitre 1 La quantité de matière la concentration molaire et le
Par exemple la masse molaire atomique de l'oxygène est M(O)= 16 |
|
Exercices de révisions : Physique-chimie
6) Déterminer la masse de zinc ayant réagi et la masse de cuivre formé. [I-] = 10 ×102 mol/L. Exercice n°3 : Quantité de matière et tableau d' ... |
|
La-mole-unite-de-quantite-de-matiere-exercices-corriges-2.pdf
Il y a donc 3000 molécules d'isoprène dans la macromolécule. Exercice 3. A 20°C l'hexane de formule chimique C6H14 est un liquide de masse volumique égale à |
|
Grandeurs physiques liés à la quantité de matière Exercice 1
La masse molaire atomique du fer est = 558 . ⁄ . Correction. La densité du fer est relié aux masses volumiques du fer et de l'eau :. |
|
Cours de Chimie Structure de la matière
Exercice 03. Un échantillon d'oxyde de cuivre CuO a une masse m = 159 g. Combien y a-t-il de |
|
EXERCICES
1 MASSES MOLAIRES ET QUANTITÉS DE MATIÈRE. Exercice. Énoncé. D'après Belin 2019. Calculer la masse molaire des espèces chi-. |
|
La mole Ce quil faut retenir La mole : Exercices dapplication niveau
n : quantité de matière de l'échantillon en mol. M : masse molaire* de l'espèce chimique contenue dans l'échantillon en g.mol-1. *Pour déterminer la masse |
|
EXERCICES AUTOUR DES QUANTITÉS DE MATIÈRE
Exercice 1. 1. Un échantillon de glucose C6H12O6 a une masse mG=250g. 1.1.Calculer la masse molaire du glucose. 1.2.Déterminer la quantité de matière nG |
|
Exercice sur la mole et la quantité de matière Niveau : seconde Thème
Enoncé. Une bouteille contient une masse m = 440 kg d'ammoniac liquéfié. L'ammoniac a comme formule brute NH3. 1. Calculer la masse d'une molécule |
|
Calculer une quantité de matière
3 Quelle est la masse volumique de l'éthanol ? 4 Calculer la quantité de matière d'éthanol dans une bouteille de vin de 75 cL. EXERCICE 1.3 Pour préparer |
|
Composition dun système chimique Prélever des quantités de
Quantité de matière masse et masse molaire. Exercice 1: Masse molaire des atomes ou ions monoatomiques. Calculer les masses molaires en utilisant les données. |
|
Seconde Chapitre 6 Fiche dexercices 2 : quantité de matière et
Définitions. 1) Qu'est-ce qu'une mole d'atomes de soufre ? 2) Que représente la masse molaire atomique du soufre ? 3) Où trouve-t-on la masse molaire atomique |
|
Corrigé DS no 1 : Chimie : Quantité de matière - Physique : Lentilles
5 oct. 2019 Exercice 1 - Questions de cours (15 points). 1. Rappeler la formule permettant de relier la quantité de matière à la masse et la masse ... |
|
Grandeurs physiques liés à la quantité de matière Exercice 1
Donnée : masse volumique d'eau : =1g.m ?1. 3- On mélange 50mL d'heptane avec 20mL d'éthanol. On verse dans une ampoule à décanter |
|
Quantité de matière - Prophychi
On a besoin de 01 mol de sulfate de suivre hydraté de formule CuSO4(H2O)5. Quelle masse de cristaux doit-on prélever ? Un élève en a prélevé 30 |
|
EXERCICES AUTOUR DES QUANTITÉS DE MATIÈRE
Exercice 1 1 Un échantillon de glucose C6H12O6 a une masse mG=250g 1 1 Calculer la masse molaire du glucose 1 2 Déterminer la quantité de matière nG |
|
Grandeurs physiques liés à la quantité de matière Exercice 1
Exercice 1 : La densité du fer est = 78 calculer la masse d'un cube de fer d'arrête = 20 Calculer la quantité de matière d'atomes de fer |
|
Chap 1 exercices - Physicus
1 MASSES MOLAIRES ET QUANTITÉS DE MATIÈRE Exercice 1 Énoncé D'après Belin 2019 Calculer la masse molaire des espèces chi- |
|
Quantité de matière et masse molaire
Seconde Chapitre 6 Fiche d'exercices 2 : quantité de matière et masse molaire Définitions 1) Qu'est-ce qu'une mole d'atomes de soufre ? |
|
Exercice n° 1 On verse une masse m1=128g de fer en poudre dans
On verse une masse m1=128g de fer en poudre dans une coupelle Déterminer la quantité de matière n1 que cela représente ainsi que le nombre N1 d'atomes de fer |
|
Quantité de matière - Prophychi
On a besoin de 01 mol de sulfate de suivre hydraté de formule CuSO4(H2O)5 Quelle masse de cristaux doit-on prélever ? Un élève en a prélevé 300g |
|
Calculer une quantité de matière
3 Quelle est la masse volumique de l'éthanol ? 4 Calculer la quantité de matière d'éthanol dans une bouteille de vin de 75 cL EXERCICE 1 3 Pour préparer |
|
Corrigés exercices sur la mole les masses molaires la
Quelle quantité de matière n de créatine C4H9 N3O2 est-on autorisé à consommer quotidiennement ? Donnée: masse molaire de la créatine M = 131 g mol-l n = m |
|
Exo07 Quantite de matierepdf
4°) 20 x 10-2 moles d'eau QUANTITE DE MATIERE ET MASSE MOLAIRE EXERCICE 11 1°) Calculer la masse d'un atome de carbone sachant que le nombre de masse A |
|
Feuille dexercices sur la quantité de matière Calculer la masse
Classe de seconde - Feuille d'exercices sur la quantité de matière Ex 1 :Comment calculer une masse molaire M ? Calculer la masse molaire du |
Comment calculer la masse avec la quantité de matière ?
La formule utilisée ici est m n M = si on veut calculer une quantité de matière. Si on veut calculer la masse, il suffit d'exprimer m : m = n × M.Comment calculer N avec V et m ?
Si on a une esp? liquide, on n'aura souvent pas la masse mais le volume. On reprend la formule : $n = \\dfrac{m}{M}$. Et puisqu'on n'a pas la masse mais le volume on va « convertir » la masse en volume en utilisant la masse volumique : $ ? =\\dfrac{m}{V}$. On obtient alors la formule : $ n =\\dfrac{ ?\\times V}{M}$.Comment trouver la quantité de matière ?
La quantité de matière est noté : n. Mole = mol = unité de quantité de matière (n). La Mole est la réunion d'un nombre bien déterminé (6,02.1023) d'entités élémentaires. On appelle ce nombre le nombre d'Avogadro.- On la note M et son unité est le gramme par mole (g·moI-1). Exemple : M(C) = 12,0 g·mol-1. Si un élément est constitué de plusieurs isotopes (atomes qui ont le même nombre de protons mais un nombre de neutrons différents), la masse molaire atomique de cet élément tient compte de la proportion des différents isotopes.
| Exercices corrigés sur la quantité de matière (1) |
| Exercice sur la mole et la quantité de matière Niveau |
| Exercices du chapitre 1 : La quantité de matière |
| EXERCICES AUTOUR DES QUANTITÉS DE MATIÈRE FE - Chimie Physique |
| Chapitre 4 Déterminer une quantité de matière Exercices |
| Thème 1: Quantité de matière masse et masse - Free |
| Searches related to masse et quantité de matière exercice filetype:pdf |
|
Cahier de vacances de sciences physiques et chimiques
bon uniforme, nous te proposons cette fiche d'exercices ATTENTION Masse molaire ( g mol−1 ) Quantité de mati`ere ( mol ) Masse ( g ) Fer (Fe) 35 |
|
Exercices de physique-chimie Première Spécialité - ph-suetfr
1/ Calculer la masse molaire de l'aspirine 2/ Exprimer puis calculer la quantité de mati`ere maximale d'aspirine autorisée par jour 3/ En déduire le nombre |
|
DÉTERMINATION DES QUANTITÉS DE MATIÈRE - chimiephysique
28 sept 2015 · Calculer la masse molaire M(H2O) des molécules d'eau 2 Calculer les quantités de mati`ere contenus dans chaque échantillons Données : M( |
|
Physique CHIMIE - Cours, examens et exercices gratuits et corrigés
Correction CHIMIE Exercice 1 1 Calcul de la concentration molaire de la solution en sulfate d'ammonium Quantité de mati`ere de sulfate d'ammonium : n m0 |
|
EXERCICES INCONTOURNABLES - Dunod
Exercice 1 1 : Masse, piston et gaz parfait (ENSTIM) ** 7 © Dunod Calculer la quantité de mati`ere n0 de dioxyg`ene contenue dans le comparti- ment 0 et la |
|
Calculer une quantité de matière
La quantité de matière est une grandeur fondamentale en chimie Elle se note M, la masse molaire, s'exprime en grammes par mole (g mol–1) Pour une espèce EXERCICE 1 2 L'éthanol est un alcool de densité égale à 0,789 Un litre de |
|
Retrouvez prochainement les corrections sur http://pcracinefreefr
Classe de seconde - Feuille d'exercices n°3 sur la quantité de matière une quantité n = 0,500mol d'acétone de formule moléculaire C3H60 et de masse |