quantification de l'énergie d'un atome
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Chaque état possède une énergie invariante (quantification des niveaux d'énergie de l'hydrogène) Postulat optique : La transition entre deux états accessibles |
|
Chapitre 5 QUANTIFICATION DES ÉNERGIES ATOMIQUES
La quantification des énergies dans l'atome trouve un début d'explication avec le modèle atomique de Bohr (1913) Ce modèle décrit correctement le spectre |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
Le modèle de Bohr est une théorie physique cherchant à comprendre la constitution d'un atome et plus particulièrement celui de l'hydrogène et des ions |
|
Chapitre2 : Quantification de lénergie de latome dhydrogène
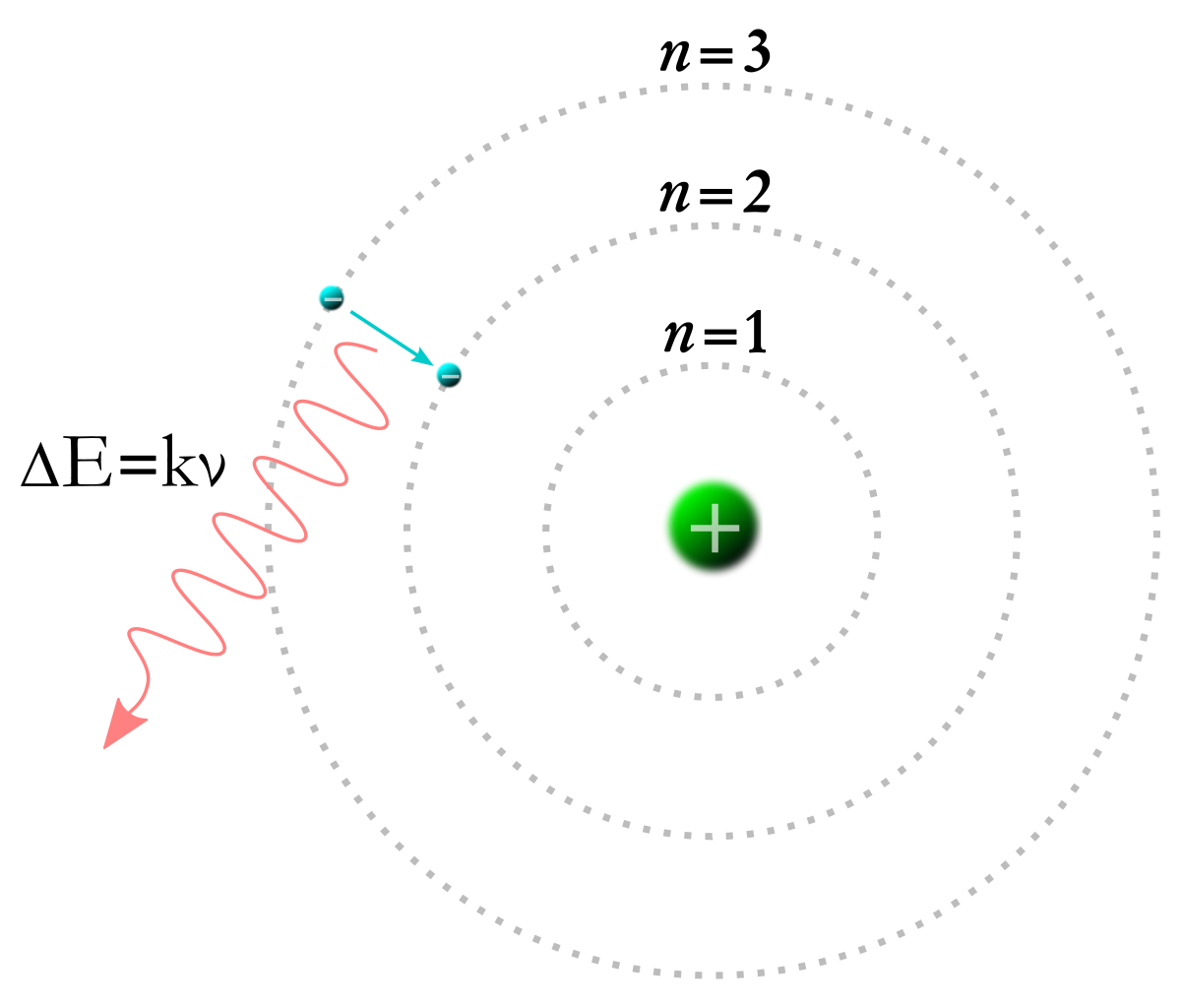
MODÈLE DE BOHR DE L'ATOME D'HYDROGÈNE CHAPITRE 2 QUANTIFICATION DE L'ÉNERGIE DE L'ATOME D'HYDROGÈNE Inversement : E ∆E hν = ∆E Ici un photon est absorbé |
|
I
L'expérience de Franck et Hertz met en évidence la quantification du transfert d'énergie entre un atome et le milieu extérieur 2- Niveaux d'énergie d'un atome |
|
Modèle de Bohr (1913)
L'atome peut passer d'un état d'énergie Ei à un état d'énergie Ef par -Quantification de l'énergie (Planck E=hv) -Quantification des niveaux d |
|
Physique quantique et niveaux dénergie dun atome
24 mar 2022 · photoélectrique la quantification du rayonnement et le photon les mécanismes d'émission et d'absorption d'un rayonnement visible ou |
|
QUANTIFICATION DE LÉNERGIE DES ATOMES
QUANTIFICATION DE L'ÉNERGIE DES ATOMES I QUELQUES RAPPELS SUR L'ATOME La dimension d'un atome est d'environ 10–10 m L'atome est noté de façon générale : X |
|
Quantification des niveaux dénergie
Mots clés de recherche : quantification des niveaux d'énergie photon modèle de l'atome spectre de l'hydrogène Provenance : Académie d'Orléans-Tours |
C'est quoi la quantification de l'énergie ?
Au niveau quantique, les particules sont des ondes et leur forme n'est pas aléatoire.
Elle est déterminée par le niveau d'énergie de la particule.
Ce phénomène s'appelle la quantification.
Ces paliers d'énergie trahissent la structure même des atomes et permettent leur modification.Pourquoi l'énergie d'un atome est quantifiée ?
L'énergie n'est qu'un nombre qui reste constant lors des transformations d'un système isolé.
Votre atome peut être considéré comme un système isolé, donc ayant une certaine énergie associée, très utile pour calculer ce qui arrive s'il se désintègre par exemple.Comment calculer l'énergie de l'atome ?
L'énergie de l'électron i se déduit de celle d'un atome hydrogénoïde en remplaçant Z par Z*i.
L'énergie totale de l'atome, à son tour, est obtenue en faisant la somme des énergies de chaque électron, supposés, dans ce modèle, être indépendants.- Et si la structure électronique de l'atome était en fait quantifiée ? Bohr supposa que les électrons ne pouvaient tourner autour du noyau que sur des orbites ou couches spécifiques de rayon de courbure constant.
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
L'électron de l'atome d'hydrogène ne possède qu'un nombre limité d'états accessibles. Chaque état possède une énergie invariante (quantification des niveaux |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
Le modèle de Bohr est une théorie physique cherchant à comprendre la constitution d'un atome et plus particulièrement celui de l'hydrogène et des ions |
|
QUANTIFICATION DE LÉNERGIE DES ATOMES
On dit qu'on a un spectre de raies On a donc une quantification de l'énergie des atomes. b) Relation entre la longueur d'onde et l'énergie de l'onde. Lors de la |
|
Chapitre II : Quantification de lénergie
Dans l'atome le noyau est immobile alors que l'électron de masse m se déplace autour du noyau selon une orbite circulaire de rayon r. • L'électron déplace sur |
|
A la découverte de la quantification des niveaux dénergie
Mots clés de recherche : quantification des niveaux d'énergie photon |
|
DL n 14 : Atome de Bohr
Pour quantifier l'énergie de l'électron Bohr ajouta un troisi`eme pos- tulat ou condition de quantification : les seules trajectoires circulaires. Page 2. DL |
|
Chapitre 5 QUANTIFICATION DES ÉNERGIES ATOMIQUES.
l'atome est négative les termes spectraux |
|
MECANIQUE QUANTIQUE
Oscillateur Harmomique. •. Puits de potentiel. •. Potentiel en atome d'Hydrogène (Cours 14 et 15). Quantification de l'énergie pour des systèmes simples. |
|
I- La quantification de lénergie transférée à un atome - 1
b- Principe. ? Les atomes de vapeur de mercure à faible pression sont bombardés avec des électrons d'énergie cinétique Ec variables. |
|
Cours LS1 - Interactions rayonnements ionisants
rayonnements ionisants : rayonnements qui provoquent l'ionisation de l'atome ; pour le vivant sont ionisantes les radiations d'énergie > 124 eV. |
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Chaque état possède une énergie invariante (quantification des niveaux d'énergie de l'hydrogène) Postulat optique : La transition entre deux états accessibles |
|
CHAPITRE III : QUANTIFICATION DE LENERGIE
CHAPITRE III : QUANTIFICATION DE L'ENERGIE III-1 MODÈLE ATOMIQUE DE BOHR (CAS DE L'ATOME D'HYDROGÉNE) Le modèle de Bohr est une théorie physique |
|
QUANTIFICATION DE LÉNERGIE DES ATOMES
On dit qu'on a un spectre de raies On a donc une quantification de l'énergie des atomes b) Relation entre la longueur d'onde et l'énergie de l'onde Lors de la |
|
Quantification des niveaux dénergie - Académie dOrléans-Tours
Mots clés de recherche : quantification des niveaux d'énergie photon modèle de l'atome spectre de l'hydrogène Provenance : Académie d'Orléans-Tours |
|
CHAPITRE IV Modèles Atomiques Et Quantification Energétique
Chapitre IV: Modèles Atomiques et Quantifications Energétique 54 I- Introduction : L'atome avec ses constituants n'est pas un élément statique du faite de |
|
Quantification de lénergie pour les systèmes simples
On peut classer les niveaux par valeur croissante de l'énergie en fonction du nombre de nœuds (points où le signe change) de la fonction d'onde V(x) 1er état |
|
I- La quantification de lénergie transférée à un atome
L'expérience de Franck et Hertz met en évidence la quantification du transfert d'énergie entre un atome et le milieu extérieur 2- Niveaux d'énergie d'un |
|
Modèle de Bohr (1913)
L'atome peut passer d'un état d'énergie Ei à un état d'énergie Ef par absorption ou emission -Quantification des niveaux d'énergie (Modèle de Bohr) |
|
Chapitre II Latome dhydrogène
L'énergie potentielle de l'atome de nature purement électrostatique s'écrit en fonction de la distance r de l'électron au noyau L'opérateur associé est la |
|
Quantification de lénergie
Jusqu'au début du XXeme siècle la mécanique classique prévoyait un continuum de valeurs possibles entre deux niveaux d'énergie d'un atome |
C'est quoi la quantification de l'énergie ?
Au niveau quantique, les particules sont des ondes et leur forme n'est pas aléatoire. Elle est déterminée par le niveau d'énergie de la particule. Ce phénomène s'appelle la quantification. Ces paliers d'énergie trahissent la structure même des atomes et permettent leur modification.Comment calculer l'énergie de l'atome ?
Les niveaux d'énergie d'un ion hydrogéno? sont similaires à ceux de l'atome d"hydrogène : on a : En = - R Z2/n2, où Z est le nombre de charges de l'élément considéré, Z-1 étant la charge de l'ion hydrogéno? correspondant.Pourquoi l'énergie d'un atome est quantifiée dans le modèle de Bohr ?
Selon le modèle de Bohr, un électron absorbe de l'énergie sous forme de photons et acc? à un niveau d'énergie supérieur si et seulement si l'énergie du photon est égale à la différence d'énergie entre l'état initial et l'état final.- On peut relier le travail de sortie, �� , et l'énergie maximale des électrons, �� M a x , étant donnée la fréquence, �� , en utilisant la formule �� = �� �� ? �� M a x , où �� est la constante de Planck.
| 41-101 Quantification de l'nergie des atomes |
| 41-101 Quantification de l'nergie des atomes |
| 1) Quantification de l'énergie d'un atome |
| CHAPITRE III : QUANTIFICATION DE L’ENERGIE - univ-setifdz |
| Chapitre2 : Quantification de l’énergie de l’atome d’hydrogène |
| Searches related to quantification de l+énergie d+un atome filetype:pdf |
Quelle est l’énergie d’un atome?
- Dans son état fondamental, l’énergie de l’atome vaut –13,6 eV.
. L’état fondamental correspond toujours au niveau de plus basse énergie.
|
Cours4pdf
Atomes I Atome à deux électrons électron 2 électron 11 12 12 noyau +Ze L' état du négligeons l'énergie cinétique du noyau, c'est-à-dire que nous considérons le mouvement du noyau La quantification existe également puisque l'on ne |
|
Lumière et énergie - Sciences Mont Blanc
Exemple : Calculer l'énergie des photons pour une radiation de fréquence ν de 6 Postulat: L'énergie d'un atome ne peut prendre que des valeurs discrètes |
|
UE 3 : Physique Fiche de cours & QCM - Tutorat Associatif Toulousain
Cette absorption se fait dans des énergies précises (quantification énergie), cela Découvert par Rutherford en 1911, le noyau atomique représente le cœur de |
|
Exercices résolus de Chimie Physique - 3ème édition - Cours
Déterminer le nombre de protons, neutrons et électrons d'un atome ou d'un ion, Le principe de quantification de l'énergie des atomes [Cours 3 3] et le modèle |
|
3ème Partie: REACTIONS EN PHASE GAZEUSE DU CHLORE ET
10 fév 1989 · Pour la quantification de cette analyse, on utilise la méthode de l'énergie d' activation de l'arrachement d'un atome d'hydrogène par un |
|
Conception et développement dun environnement dapprentissage
relation entre l'énergie électrique et l'énergie mécanique, quantifier cette Les particules composées d'atome et de molécules qui sont en mouvement créent |
|
Présentée en vue de lobtention du diplôme de - Hydrologieorg
(quantité, localisation et nature), la mise en évidence et la quantification des référence aux termes de l'Agence Internationale pour l'Energie Atomique : un |
|
Radioactivité LURE université ouverte màj_2014 - ResearchGate
L'atome Des protons et des neutrons qui constituent un noyau et des électrons qui 4 H+ + 2 électrons => 4He +énergie la quantification de la toxicité |