ph acide faible
|
Calcul du PH
Le pH d'une solution de sel d'acide faible et de base faible est celui d'un mélange d'acide faible et de base faible pH = 1/2 PK₂ b/bH + 1/2 pKa Ha/a- 11 |
|
Chapitre 1 Acides et bases
6) Un indicateur coloré de pH est un acide faible dont les formes acide et basique n'ab- sorbent pas la même partie du spectre visible Par exemple pour le |
|
Chapitre Chimie N°4 : Les Acides et les Bases faibles en solution
pH égal à 31 Q1/Calculer la concentration en ions H3O+ Q2/L'acide benzoïque est-il un acide fort ou un acide faible? Q3 / Ecrire l'équation de la |
|
Fiche de révisions sur les acides et les bases
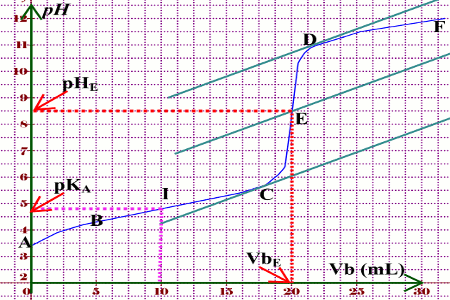
acide faible : c'est un acide dont la réaction sur l'eau n'est pas totale Cette droite est parallèle aux deux autres droites ; elle coupe la courbe pH = f ( V ) |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Lien entre le pH et le pKa d'un couple Le pH d'une solution contenant un acide faible AH et sa base conjuguée A‒ est lié au pKa du couple AH/A‒par la relation: |
|
PHDES SOLUTIONS DE MELANGE
pH = - log (C1 + α2 C2) Remarques: ✓ Si C1 >> α2C2 => pH imposé par l'acide fort pH = -log C1 ✓ Si C1 pH imposé par l'acide faible pH = -log ( |
|
VIEtude sommaire des mélanges
On calcule souvent le pH en négligeant l'acide faible Cette approximation grossière n'est justifiée que si l'apport d'ions hydronium par l'acide faible est |
Quelle est le pH d'un acide faible ?
Acide faible : pH
2- Le pH des acides et des bases.
Rappelle-toi que le pH est une mesure de la concentration d'ions hydrogène en solution.
En outre, un pH plus faible signifie que la concentration d'ions hydrogène est plus élevée.Comment savoir si un acide est faible ?
1Pour un acide fort : pH = - log C.
2) Pour une base forte: pH = 14 + log C.
Ces formules sont valables pour les concentrations supérieures à 10-7 mol/L.
3) Pour un acide faible : pH = 1/2 pKa - 1/2log C.
4) Pour une base faible : pH = 7 + 1/2 pKa + 1/2log C. 5pH = 1/2( pKa1 + pKa2)Quelle formule permet d'exprimer le pH d'un mélange d'un acide faible et de sa base conjuguée ?
L'équation de Henderson-Hasselbalch peut être utilisée pour calculer pour un mélange d'un acide faible HA et de sa base conjuguée A– la fraction α représentée par l'acide non dissocié HA : α(HA) = [HA] / (ca + cb) = [H3O+] / (Ka· c0 + [H3O+]).
- Un acide fort est un acide réagissant totalement avec l'eau.
Si sa concentration est c, alors .
Un acide faible AH réagit avec l'eau selon une réaction limitée .
Une base forte réagit avec l'eau selon une réaction totale.
|
§ 7 (suite) Titrages acide-base
Un indicateur est un acide faible dont la forme acide HIn est caractérisé par Titrage d'un acide fort par une base forte. pH ! "a = V0 / (V0 + Vtitr). |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand la fraction. |
|
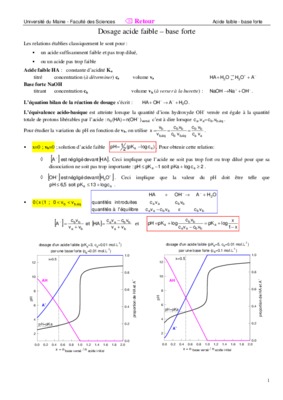
Dosage acide faible – base forte
un acide suffisamment faible et pas trop dilué. ? ou un acide pas trop faible x=0 ; vb=0 ; solution d'acide faible. )clog. pK(. 2. 1. pH. |
|
PH et pKa
Une solution contenant un acide fort a un pH inférieur à celui d'une solution de même concentration d'un acide faible. ([HCl] 0.1 M pH < 1; [CH3COOH] 0.1 M |
|
Fiche de synthèse n°2 - Réactions acido-basiques en solution
Lien entre le pH et le pKa d'un couple. Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
2. CALCUL DE PH DES SOLUTIONS AQUEUSES. 2.1. Cas d'un acide fort. 2.2. Cas d'un acide faible. 2.3. Cas d'une base forte. 2.4. Cas des bases faibles. 2.5. |
|
PH dune solution de chlorure dammonium pH = 5.6
Le chlorure d'ammonium NH4Cl est un sel soluble qui se dissocie dans l'eau suivant la réaction : NH Cl NH. Cl. 4. 4. ?. ?. +. ?. +. Cet acide faible |
|
Cours de Chimie - Informatique Titrage acide/base
17 avr. 2013 tion du graphique de l'évolution du pH en fonction du volume de réactif introduit. 1 Titrage d'un acide fort par une base forte. 1.1 Données. |
|
VI..Etude sommaire des mélanges
l'acide faible possède une constante d'acidité et une concentration assez faibles) ce dont on peut se rendre compte en calculant les pH des deux acides |
|
Dosages acidobasiques
9 fév. 2018 chera par exemple la concentration d'un acide (fort ou faible) ... sique (pH couleur d'un indicateur coloré |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand |
|
VIEtude sommaire des mélanges
Au p E de la titration des acides faibles par des bases fortes le pH se situe souvent au-dessus de 7 parce qu'à ce moment le milieu renferme uniquement la base |
|
Chapitre 1 Acides et bases
suivante entre concentration apportée en acide c et pH : pH = ?log (c) La base conjuguée d'un acide fort est dite “indifférente dans l'eau” |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide fort 2 2 Cas d'un acide faible 2 3 Cas d'une base forte 2 4 |
|
Fiche de révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides faibles : acide [ ]base[ log pK pH A + = Conséquence : pH = - log[H3 O |
|
PH et pKa - The Zysman-Colman Group
Plus la valeur de pKa est faible plus le Ka est grand plus l'acide est fort 4 Table de pKa http://evans harvard edu/ pdf /evans_pKa_table pdf |
|
PH DES SOLUTIONS AQUEUSES I Généralités
(Voir pH de solution de mélange de protolytes de natures différentes – Cas d'un mélange d'acide fort et d'acide faible) 3/ Cas où l'acide et la base sont en |
|
Chapitre 8 : Propriétés acide-base
Pour réaliser un tampon avec un acide faible il faut que son pKa soit proche du pH souhaité Ce qui est le cas ici : pKa(CH3COOH) = 4 75 Le nombre de mole de |
|
Les acides et bases en solution aqueuse - Groupe Transition
On appelle acide fort tout acide qui comme HCl est totalement ionisé dans l'eau Les principaux acides forts sont : HCl HBr HI H2SO4 (au moins par sa |
|
Fiche de synthèse n°2 : réactions acido-basiques en solution aqueuse
Le pH d'une solution contenant un acide faible AH et sa base conjuguée A? est lié au pKa du couple AH/A?par la relation: Cette relation découle de la |
Quel est le pH d'un acide faible ?
Acide faible : pH = 1/2 (pKa - log Ca) (11)Base faible : pH = 7 + 1/2 (pKa + log Cb) (15) Sel de base faible et d'acide fort : pH = 1/2 (pKa - log Csel) (24) Sel d'acide faible et de base forte : pH = 7 + 1/2 (pKa + log Csel) (21) Comment déterminer le pH d'un acide faible ?
Formule de calcul de pH
1Pour un acide fort : pH = - log C.2Pour une base forte: pH = 14 + log C. Ces formules sont valables pour les concentrations supérieures à 10-7 mol/L.3Pour un acide faible : pH = 1/2 pKa - 1/2log C.4Pour une base faible : pH = 7 + 1/2 pKa + 1/2log C. 5pH = 1/2( pKa1 + pKa2)Comment justifier un acide faible ?
1Un acide est dit "faible" si, en présence d'eau, s'établit un équilibre où coexistent l'acide et sa base conjuguée.2Un acide est dit "fort" si sa réaction avec l'eau peut être considérée comme totale et qu'il ne subsiste alors en solution que sa base conjuguée.- On considère qu'un acide est faible lorsque son pKa est supérieur à ?1,74 à 25 °C (pKa du cation hydronium H3O+). Pour un pKa supérieur à 14, on dit qu'il est indifférent. Un acide est d'autant plus faible que son pKa est élevé. Sa base conjuguée est donc d'autant plus forte et moins stable que ce même pKa est élevé.
| Acide faible - Base faible |
| PH et pKa - Zysman-Colman |
| ACIDES BASES - pH - Free |
| § 7 (suite) Calcul du pH de solutions - EPFL |
| Images |
| Searches related to ph acide faible filetype:pdf |
Comment savoir si une solution est acide ?
- Le pH d’une solution est compris entre 0 et 14.
. Si pH < 7, la solution est acide.
. Si pH = 7, la solution est neutre.
. Si pH > 7, la solution est basique.
Quelle est la démonstration pour un mélange d’acides faibles?
- DÉMONSTRATION POUR UN MÉLANGE D’ACIDES FAIBLES (1)Équilibres dans l’eau ? A 1 H + H 2 O? A 1 - + H
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Force des acides et des bases 1 5 Constantes d'acidité et de basicité 1 6 Coefficient de dissociation d'un acide faible : 2 CALCUL DE PH DES SOLUTIONS |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
PH et pKa - Eli Zysman-Colman
de même concentration d'un acide faible ([HCl] 0 1 M, pH < 1; [CH3COOH] 0 1 M , pH = 3 7) 6 Exercices 1) Le Ka d'un acide est 8 10-3 Quel est son pKa? |
|
Dosage acide faible – base forte
Les relations établies classiquement le sont pour : ▫ un acide suffisamment faible et pas trop dilué, ▫ ou un acide pas trop faible Acide faible HA : constante |
|
VIEtude sommaire des mélanges
l'acide faible possède une constante d'acidité et une concentration assez faibles) , ce dont on peut se rendre compte en calculant les pH des deux acides dans |
|
Propriétés des acides et des bases
Les acides faibles en solution aqueuse se dissocient seulement partiellement, la majorité des molécules restent non dissociées Acide faible A H H+ A- Page 20 |
|
Déterminer si un acide est fort ou faible
Un acide est faible s'il se dissocie partiellement lors de sa mise en solution On a alors la relation [H3O+]≠C Méthode à appliquer On connait le pH et la |
|
Les acides et bases en solution aqueuse - Groupe Transition
Echelle et table des constantes d'acidité Ka (pKa) 4 5 Coefficient d'ionisation ( de dissociation) d'un acide ou d'une base faible Pourcentage d'ionisation (de |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
7 II – LA REACTION ACIDE/BASE 8 1 LES ACIDES FORTS ET LES BASES FORTES 8 2 LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE |































![PDF] Intégration conceptuelle des équilibres acide-base par les PDF] Intégration conceptuelle des équilibres acide-base par les](https://upload.wikimedia.org/wikipedia/commons/thumb/5/53/Colored_pH_indicator_%28circle%29.png/341px-Colored_pH_indicator_%28circle%29.png)