oxydoréduction cuivre zinc
Comment calculer l'oxydoréduction ?
La réaction d'oxydoréduction est l'addition d'une oxydation et d'une réduction (de manière à simplifier les électrons).
L'équation d'une oxydoréduction s'écrit de la manière suivante : Ox1 + Réd2 = Ox2 + Réd1, avec Ox1 / Réd1 et Ox2 / Réd2 des couples oxydant-réducteur.Quel est le réactif du zinc ?
Le zinc en poudre réagit avec incandescence au contact du disulfure de carbone en produisant du sulfure de zinc et du carbone.
Comment mettre en évidence le zinc ?
Manipulation : On verse quelques gouttes d'hydroxyde de sodium dans la solution susceptible de contenir des ions zinc (II).
Si des ions zinc (II) sont présents, alors il se forme un précipité blanc.- Les réactifs sont le zinc solide et les ions zinc II.
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
Les ions cuivre (II) en solution arrachent ainsi des électrons au zinc métallique et transforment ce dernier en ions zinc aqueux. Dans ce système le zinc |
|
Chapitre 6 : Les réactions doxydoréduction
1) Réaction entre les ions cuivre II et le métal zinc : ? Expérience : On plonge une lame de zinc dans une solution de sulfate de cuivre II (couleur bleue) |
|
? Zn2+
conclusion : dans le récipient n°2 il y a oxydoréduction. Les ions Cu2+ se transforment en cuivre Cu métal et la lame de zinc se transforme en ions Zn2+. |
|
Chapitre IV Chimie : oxydo-réduction - 1°) Couple oxydant
L'ion Cu2+ capte deux électrons pour donner du cuivre métallique la réaction s'appelle une réduction. (2) Zn. Zn2+ + 2 e-. Le métal Zinc donne naisance à |
|
Les réactions doxydo-réduction
le zinc : Zn. Zn2+ + 2e- le cuivre : Cu. Cu2+ + 2e-. ? un oxydant est une espèce chimique capable de capter 1 ou plusieurs électrons. exemples :. |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
réduction de l'électrode de cuivre. Le potentiel standard de réduction de l'électrode de zinc se détermine de la même manière. Cette fois on. |
|
Exercices de révisions : Physique-chimie
Écrire les deux demi-équations d'oxydoréduction des deux couples auxquels le peroxyde d'hydrogène appartient Exercice n°6 : Action du cuivre sur le zinc. |
|
Réaction doxydoréduction - Correction
Exercice 02 : Zinc/Cuivre. On plonge une lame de zinc dans un bécher contenant un volume V = 50 mL d'une solution bleue de sulfate de cuivre II de |
|
Synthèses et caractérisations doxydes mixtes à base de cuivre zinc
31 mars 2016 catalyseurs à base d'oxyde de cuivre zinc ou chrome [Hamelinck et ... de cuivre réduites Cu0 en Cu+ suite aux réactions d'oxydo-réduction. |
|
Chapitre 4 :La corrosion
Réaction d'oxydoréduction : Le zinc métal n'a pas de domaine commun avec l'eau ... H : on a un dépôt de cuivre sur le zinc : Le système. |
|
Les réactions doxydo-réduction - Physique - Chimie
le zinc : Zn Zn2+ + 2e- le cuivre : Cu Cu2+ + 2e- ? un oxydant est une espèce chimique capable de capter 1 ou plusieurs électrons exemples : |
|
Réactions doxydo-réduction
Il y a eu transfert d'électrons du zinc métal vers les ions cuivre Ici Zn a libéré des électrons : il est réducteur ; Cu2+ a capté des électrons : il est |
|
Chapitre 6 : Les réactions doxydoréduction - Physagreg
1) Réaction entre les ions cuivre II et le métal zinc : ? Expérience : On plonge une lame de zinc dans une solution de sulfate de cuivre II (couleur bleue) |
|
Réactions doxydo-réduction - AlloSchool
Il s'agit d'une réaction chimique au cours de laquelle les ions Cu2+ se transforment en cuivre métallique Cu(s) qui se dépose sur la plaque de fer Ceci est |
|
Réaction doxydoréduction - Correction - AlloSchool
Exercice 02 : Zinc/Cuivre On plonge une lame de zinc dans un bécher contenant un volume V = 50 mL d'une solution bleue de sulfate de cuivre II de |
|
Thème 2 : Matière et matériaux Oxydoréduction corrosion des
Oxydoréduction corrosion des métaux et piles I- Expériences 1°) Réaction entre le zinc et les ions cuivre II On plonge une lame de zinc décapée dans une |
|
Oxydo-Réduction Objectifs: Réaliser une réaction entre un métal et
Lors d'une réaction d'oxydo-réduction l'oxydant prend des électrons au réducteur Les ions cuivre ( Cu2+ ) réagissent avec le métal zinc pour donner un |
|
Réactions doxydoréduction AQ2 - PTSI Ginette
le zinc Zn est capable de provoquer la réduction des ions cuivriques : Cu2+ • le cuivre Cu n'est pas capable spontanément de réduire les ions : Zn2+ ? Le |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
On considère une pile constituée d'une lame de zinc plongée dans une solution de -L'électrode de cuivre est la cathode et celle de fer est l'anode |
|
Oxy Do Reduction PDF Réaction doxydoréduction Cuivre - Scribd
29 jan 2022 · zinc se transforme en ions Zn La réaction inverse n'est pas possible Oxydation : Zn ? Zn2+ + 2e? (un atome de zinc perd deux électrons) |
Comment cuivre du zinc ?
. La quantité de poudre diminue, donc le zinc est un réactif.
. Le dépôt rouge-orangé qui se forme sur la poudre de zinc est du cuivre métallique.
. Le cuivre est un produit de la transformation chimique.
Comment faire des équations d'oxydoréduction ?
. Les électrons n'apparaissent donc pas dans le bilan.
Comment s'oxyde le zinc ?
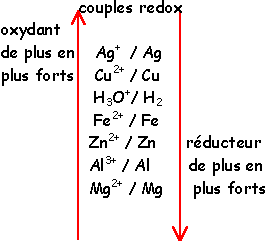
Quel est l'oxydant le plus fort ?
|
Chapitre 6 : Les réactions doxydoréduction - Physagreg
(aq) 2 Zn Cu aq s Zn Cu + + + → + Les atomes de zinc ont cédé deux électrons, les ions cuivre II en ont accepté deux Équation d'oxydoréduction ou rédox |
|
→ Zn2+
conclusion : dans le récipient n°2, il y a oxydoréduction Les ions Cu2+ se transforment en cuivre Cu métal et la lame de zinc se transforme en ions Zn2+ La |
|
REACTIONS DOXYDATION ET DE REDUCTION
L'atome de zinc a perdu deux électrons pour devenir un cation bivalent Zn Le cuivre élémentaire se transforme en oxyde de cuivre (II) (vert de gris) en présence Equilibrer les équations d'oxydo-réduction suivantes, et identifier l' oxydant et |
|
Classification qualitative des couples oxydant réducteur - Fastef
des ions *Rappeler le caractère exothermique de la réaction d`oxydoréduction entre Cuivre et Zinc |
|
Oxydo-réduction et corrosion
Les ions cuivre Cu2+ ont oxydé le fer : l'ion Cu2+ est un oxydant Le fer a L' électrode de zinc est le pôle , elle donne des électrons e- au circuit : Zn(s)=Zn2+ |
|
Chapitre 4 :La corrosion
Réaction d'oxydoréduction : OH2 4 H4 O 2 2 = Le zinc ne sera pas corrodé du tout (mais l'eau n'est pas stable) Boulon en cuivre sur une plaque de fer : |
|
Oxydation et réduction en solution aqueuse - Free
Après quelques heures on observe un dépot de cuivre sur la lame de zinc et la décoloration de la Il y a eu oxydoréduction entre deux corps : Zn et Cu2+ |
|
OXYDANT et REDUCTEUR réduction et oxydation - BTS - Sciences
L'électron est la « monnaie d'échange » dans une réaction d'oxydoréduction, tout comme le proton Expérience 1 : entre les éléments cuivre et zinc Cu 2+ |