On peut l'exprimer aussi en litre ( L ) pour les liquides et les gaz. 2. Comment mesurer le volume d'un liquide à Il existe au laboratoire des récipie
|
Chapitre IV Masse et volume dune substance I] Mesure du volume d
On peut l'exprimer aussi en litre ( L ) pour les liquides et les gaz. 2. Comment mesurer le volume d'un liquide ? Il existe au laboratoire des récipients |
|
Physique Chimie
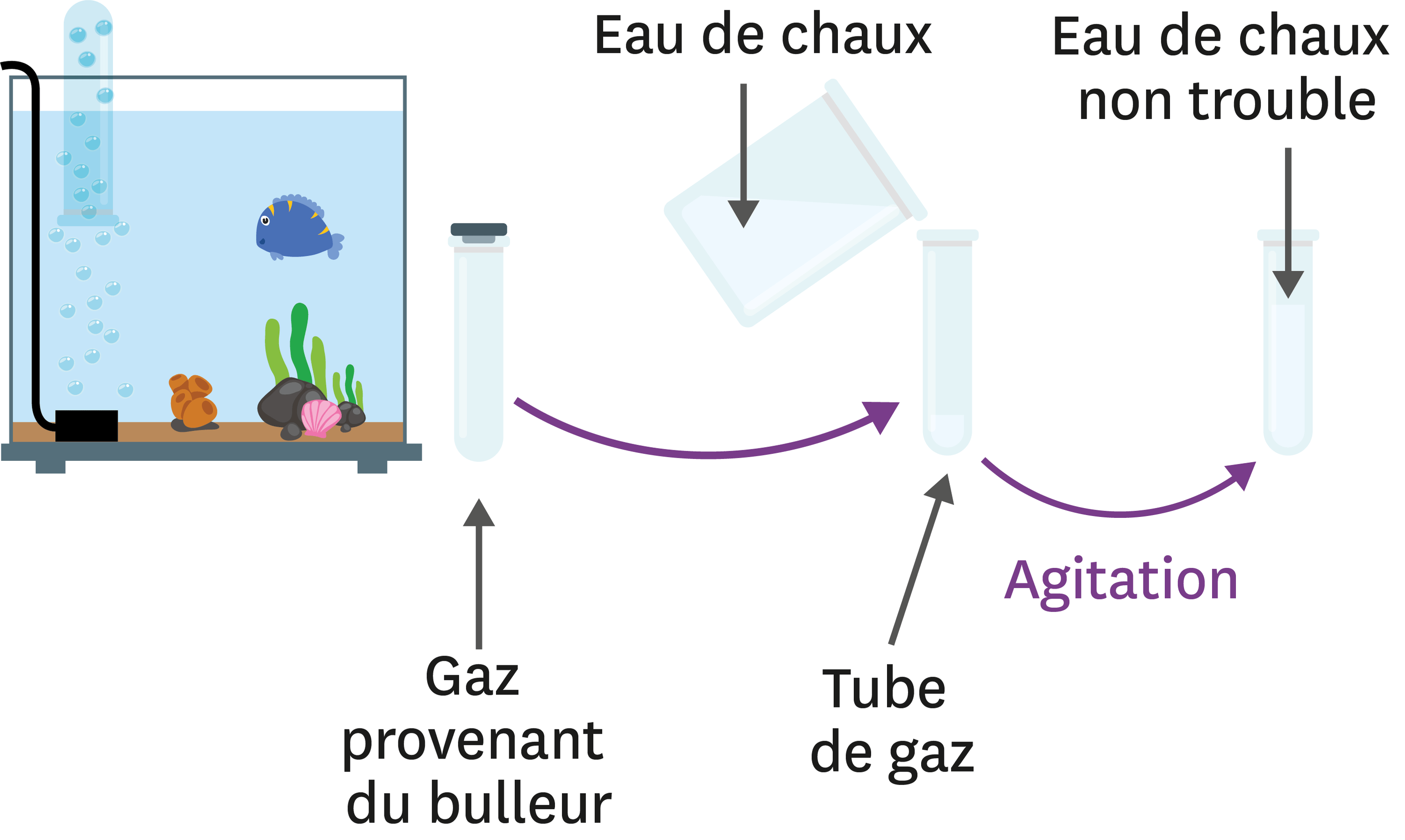
٠٨/٠٢/٢٠١٧ Quel est le gaz qui s'échappe de l'eau sous forme de bulles ? du dioxygène. du dioxyde de carbone. du gaz naturel. 1. 2. |
|
Exercices de Thermodynamique
Calculer la pression P dans le récipient et commenter. Reprendre le calcul pour un gaz parfait et commenter. Rép : 2) V = 951.10−4 m3 soit ∣∣. |
|
RISQUES LIÉS AUX ÉQUIPEMENTS SOUS PRESSION
Lorsque l'eau dans la cocotte-minute est chauffée il se forme de la vapeur d'eau |
|
Manuel des techniques de base pour le laboratoire médical
aussi bien pendant leur formation que lors de leurs activités ultérieures. Il peut également être utile pour des travaux de routine dans les laboratoires ... |
|
3 La poussée dArchimède ⃗ P P ⃗ P ⃗ FA P′ < P
Figure II.14 – Mesure du poids du liquide déplacé. Mesurons le poids apparent Certains poissons absorbent de l'air pour contrôler le volume de gaz qu'ils ... |
|
Principes directeurs pour la manipulation et laffectation sans risque
Les produits chimiques utilisés par un laboratoire clandestin pour fabriquer illicite- ment de la drogue sont généralement détournés du commerce légal et |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Écrire l'équation de la réaction support du dosage en utilisant la notation AH pour l'acide lactique. 2.1.2. Exprimer la concentration molaire CS en acide |
|
Mécanique des fluides
Chapitre 2: Giorgione le lever de soleil |
|
E DE LAIEA COLLECTION SANTÉ HUMAINE DE LAIEA
L'AIEA a promu une utilisation plus large des techniques qui reposent sur des isotopes stables pour évaluer la composition corporelle dans différents groupes de |
|
Chapitre IV Masse et volume dune substance I] Mesure du volume d
On peut l'exprimer aussi en litre ( L ) pour les liquides et les gaz. 2. Comment mesurer le volume d'un liquide ? Il existe au laboratoire des récipients |
|
RISQUES LIÉS AUX ÉQUIPEMENTS SOUS PRESSION
rencontrés dans les laboratoires Pour exprimer la pression en « MPa » à partir d'une valeur ... de gaz sous pression ne peut donner qu'un résultat. |
|
PROBL`EMES DE THERMODYNAMIQUE (L3) et leurs corrigés
comme limite l'équation d'état des gaz parfaits pour les grands volumes. 2?) Exprimer les rapports ?/Cv µ/Cp |
|
Exercices de Thermodynamique
Calculer la pression P dans le récipient et commenter. Reprendre le calcul pour un gaz parfait et commenter. Rép : 2) V = 951.10?4 m3 soit ??. |
|
Physique Chimie
8 feb 2017 Le chapitre 5 du manuel de Cycle 4 « Dissolution des gaz dans l'eau » ... Physique Chimie Nathan pour le Cycle 4. |
|
Manuel des techniques de base pour le laboratoire médical
Le litre et ses sous- multiples comme le millilitre |
|
Méthodes de mesure du débit - Cahier 7
Le cahier 7 du Guide d'échantillonnage à des fins d'analyses environnementales traite des techniques reconnues d'évaluation des débits et des volumes d'eau |
|
Génie de la Réaction Chimique: les réacteurs homogènes
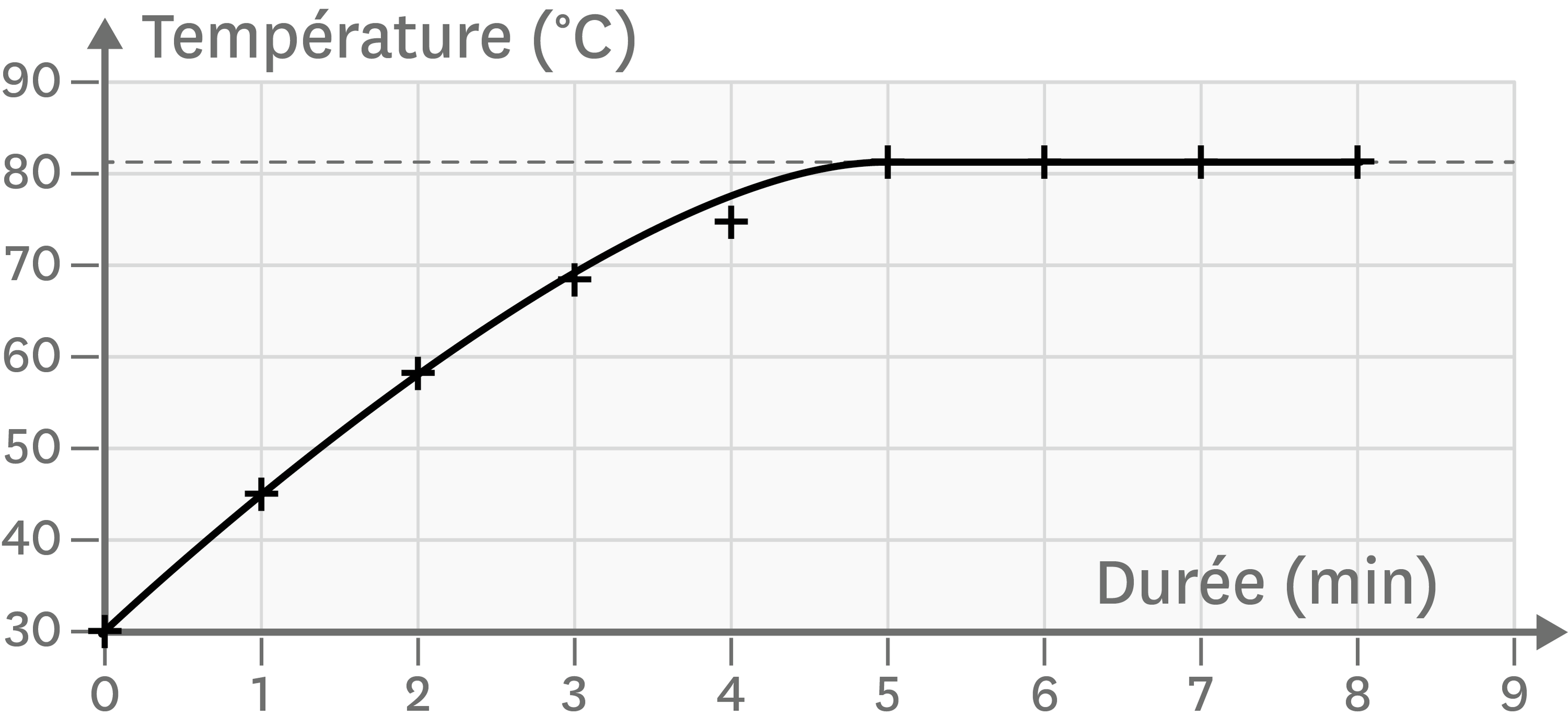
14 jul 2022 Comment évolue la concentration en réactif A en fonction du temps ? Question 2. Combien de temps faut-il pour atteindre un taux de conversion de ... |
|
5. La masse volumique
Pour mesurer la masse d'un objet il faut comparer la Cylindre gradué pour les liquides (voir Fig. 2) ;. • Récipient à trop plein et cylindre gradué pour ... |
|
I RÈGLEMENTS
31 may 2008 Dans certains cas il peut être commode de mesurer la température de ... de laboratoire à température programmable (d'un volume de 2 litres ... |
Quelle est la formule liant la quantité de matière au volume d'un gaz ?
On rappelle la formule liant la quantité de matière n au volume des gaz V : V = n imes V_m. On repère la quantité de matière n du gaz. Si nécessaire, on la convertit en mol. Le volume molaire Vm des gaz ne dépend pas de la nature des gaz mais uniquement de la pression et de la température.
Quelle est la meilleure façon de mesurer le volume d'un liquide?
• Pour mesurer le volume d'un liquide, on peut utiliser n'importe quel récipient comportant des graduations ou un trait de jauge (bêcher, erlenmeyer, fiole jaugée), mais le mieux adapté est l'éprouvette graduée. Dans une éprouvette graduée, la surface libre du liquide prend la forme d'un ménisque.
Comment calculer le volume molaire d'un gaz ?
Donnée : On rappelle que dans les conditions normales de température et de pression (CNTP), le volume molaire des gaz est de 22,4 litres par mole. On rappelle la formule liant la quantité de matière n au volume des gaz V : V = n imes V_m. On repère la quantité de matière n du gaz. Si nécessaire, on la convertit en mol.
Comment mesure-t-on la densité d'un liquide ?
Pour les liquides, une mesure précise de densité utilise un pycnomètre . La densité relative d'un corps solide par rapport à un corps fluide est le rapport de la masse du corps solide sur la masse du corps fluide de volume identique à celui du corps solide 8. On mesure cette densité relative en réalisant trois pesées et en immergeant le solide.
|
Chapitre IV Masse et volume dune substance I] Mesure du volume d
On peut l'exprimer aussi en litre ( L ) pour les liquides et les gaz 2 Comment mesurer Il existe au laboratoire des récipients gradués ( éprouvette, bécher, erlenmeyer ) ou TP n°10 : Mesure du volume d'un liquide avec une éprouvette graduée Plonge un solide dans un récipient qui contient de l'eau et fais le schéma |
|
Physique Chimie
8 fév 2017 · L' ouverture de la Partie 2 « Décrire les propriétés de la matière » ◗ Le chapitre 5 du manuel de Cycle 4 « Dissolution des gaz dans l'eau » |
|
Volume des liqu :3 Leçon n° Volume des liquides et - AlloSchool
Avec quoi on mesure le volume d'un liquide A l'aide d'une récipient gradué (Il existe au laboratoire des autres récipients grad Comment utiliser une éprouvette |
|
Les propriétés physiques des gaz
Dans ce chapitre, nous verrons d'abord la place qu'occupent les gaz dans notre Notre corps a besoin de dioxygène pour assurer les fonctions peuvent être des atomes ou des molécules) 2 Les particules de matière sont constamment en Il existe une quatrième phase de la matière, le plasma, que l'on trouve surtout |
|
Exercices de Thermodynamique
2) Calculer le volume occupé par une mole d'un gaz parfait `a la température de 0◦C sous la pression 2) Montrer qu'il existe un unique état C tel que : ( ∂P |
|
CORRECTION Séquence 6 : Masse et Volume Activité : Comment
Activité : Comment mesurer une masse et un volume ? obtenir la masse d'un litre d'eau : 10 × 100 = 1 000 g = 1 kg Pour trouver le volume de l'objet, il faut soustraire le volume de l'eau au volume total : La capacité d'un récipient est le volume maximal de liquide que celui-ci peut contenir R : 1 : c ; 2 : b ; 3 : d ; 4 : a |
|
Chap2 Lair un mélange de molécules
Masse d'un litre d'air dans les conditions usuelles de température et de C3 1 2 Mesurer des volumes ; mesurer des masses Activité 1 p 28 : Comment l' atmosphère est-elle constituée ? 2 Il y a aussi un peu de vapeur d'eau et d' ozone : contrairement à celles des gaz diazote pour 78 et du dioxygène pour 21 |
|
Exercice 10 La bouteille de butane
Une bouteille de gaz pour usage domestique contient 13,0 kg de butane C4H10 dire qu'il n'est ni complètement gazeux ni complètement liquide L'équation d 'état des gaz parfait nous permet de calculer la pression du butane Or 181 >> Pv (qui vaut 2,5) donc tout le butane ne peut pas gazeux car dès que P > PV, |