7 Transferts de protons Equilibres acide-base
|
7 Transferts de protons Equilibres acide-base
Les équilibres de transfert de proton sont décrits par des constantes d’équilibre Pour une solution diluée de l’acide acétique dans l’eau par exemple : CH 3COOH (aq) CH 3COO– (aq) + H+ (aq) K = a(H+)⋅a(CH 3COO–) a(CH 3COOH) Pour des solutions suffisamment diluées les coefficients d’activité des solutés γ ≈1 |
|
Eléments fondamentaux de chimie
5) Equilibres chimiques 6) Propriétés des solutions 7) Transferts de protons: Equilibres acide-base 8) Transferts d’électrons: Equilibres rédox électrochimie 9) Cinétique chimique 11 Contenu du cours Chimie générale quantitative Traitement macroscopique des systèmes: Introduction à la thermodynamique |
|
Chap VI: Equilibres acido
Il est important de connaitre les espèces qui fournissent des protons celles qui les acceptent et la façon d’exprimer la concentration en ions hydrogène dans la solution Selon cette théorie un acide est un donneur de proton et une base un accepteur de proton Le proton est extrêmement mobile et les acides et bases dans l’eau sont toujours en équili |
|
LES ÉQUILIBRES ACIDO-BASIQUES
Un acide est un donneur de protons : AH + H 2 O H 3 O+ + A-Une base est un accepteur de protons : B + H 2 O BH+ + OH-2 Acide et base selon Lewis (Arrhenius-Lewis) : Un acide est un corps capable d’accepter un doublet électronique : H+ : Acide de Lewis Une base est un corps capable de donner un doublet électronique : NH 3: Base 3 |
Comment calculer l'équilibre de transfert de proton ?
Les équilibres de transfert de proton sont décrits par des constantes d’équilibre. Pour une solution diluée de l’acide acétique dans l’eau, par exemple : K = a(CH3COOH) Pour des solutions suffisamment diluées, les coefficients d’activité des solutés γ ≈1. On peut donc exprimer la constante d’équilibre en termes de concentrations.
Comment calculer la constante d’acidité ?
L’expression résultante, où toutes les concentrations sont divisées par c0 = 1 mol⋅L–1 est appelée la constante d’acidité (ou constante de dissociation de l’acide) et est notée Ka : ( [H+] / c0 )⋅( [CH3COO–] / c0 ) Ka = La valeur expérimentale de Ka pour l’acide acétique est de 1.8⋅10–5.
Qu'est-ce que le transfert de proton dans l'eau ?
Le transfert de proton dans l’eau est l’une des réactions les plus rapides que l’on connaisse. L’équilibre entre H2O, H+ et OH– existe donc toujours dans l’eau et dans les solutions aqueuses. La réaction de dissociation de H2O est appelée l’autoprotolyse de l’eau. Sa constante d’équilibre est aussi appelée produit ionique de l’eau:
Quelle est la différence entre un acide et une base ?
Les définitions d’un acide et d’une base ont été généralisées par Brønsted et Lowry (1923) : Les acides sont considérés comme des composés capables de libérer un ou plusieurs protons H+, qu’ils soient en solution dans l’eau ou non. Les bases sont vues comme des composés capables de capter un ou plusieurs ions H+.
La théorie de BrønstedLowry
Il est important de connaitre les espèces qui fournissent des protons, celles qui les acceptent et la façon d’exprimer la concentration en ions hydrogène dans la solution Selon cette théorie un acide est un donneur de proton et une base un accepteur de proton Le proton est extrêmement mobile et les acides et bases dans l’eau sont toujours en équili
Acide fort Base forte Acide faible Base faible
Conservation de la matière Constantes d’équilibres Electroneutralité f2school.com
Les base fortes réagissent totalement, se protonent totalement
Il n’y a pas d’équilibre chimique, la réaction de dissolution d’une base forte dans l’eau n’a donc pas de constante d’acidité K B f2school.com
c c
B réagit totalement (se protone totalement) pour donner BH+, on peut donc négliger [B] devant [BH+] dans l’équation de conservation de la matière C= +[BH+] donne c= [BH+] Ex : NaOH, KOH, NaClO (eau de javel) hydroxydes métalliques M(OH)n Base forte f2school.com
Si l’acide est suffisamment faible donc peu dissocié
[A] est donc négligeable devant [AH] C = [AH]+[A]donne c=[AH] f2school.com
Base faible
Si la base est suffisamment faible, se protone difficilement f2school.com
Sels dissous
La mise en solution d’un sel se traduit par une dissociation totale en ions. Il n’ya pas d’équilibre (donc pas de constante d’équilibre) f2school.com
|
7. Transferts de protons Equilibres acide-base
7. Transferts de protons. Equilibres acide-base Dans l'eau les acides et les bases définis selon Arrhenius (voir §2). |
|
• Cours_EFC 06-07
7) Transferts de protons: Equilibres acide-base. 8) Transferts d'électrons: Equilibres rédox électrochimie. 9) Cinétique chimique. 11. Contenu du cours. |
|
Chap VI: Equilibres acido- basiques – Transfert de protons
Le proton est extrêmement mobile et les acides et bases dans l'eau sont toujours en équilibre avec leurs homologues protonés et déprotonés et les ions. |
|
Rappel sur les Acides et les Bases
Toute réaction acido-basique est un transfert de proton(s) mettant en jeu deux couples. Une solution est dite acide si [H3O+] > [OH-] : le pH < 7. |
|
Cours de Résidanat Sujet : 68
7. Etablir le diagnostic étiologique d'un trouble acido-basique à partir des données un acide est un donneur de protons [H+] tandis qu'une base. |
|
Chap 6 acide-base
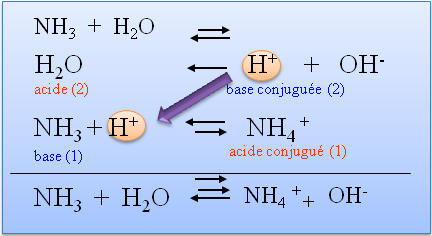
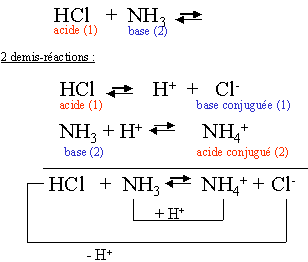
acide et si le pH > 7 la solution est basique. Ainsi il y a transfert de proton et on peut écrire la réaction entre l'acide éthanoïque et l'ammoniac :. |
|
Chapitre 1 Acides et bases
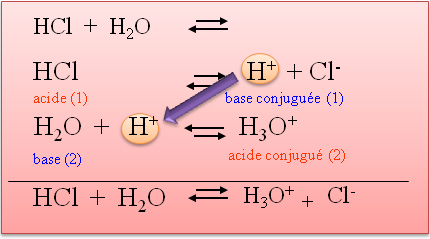
où H3O+ est l'ion hydronium ou oxonium |
|
Les acides et bases en solution aqueuse.
d'écrire la constante d'équilibre relative à une réaction ; Une réaction acide-base est une réaction de transfert de proton H. + d'un acide à. |
|
Cours et exercices de chimie des solutions
Chapitre 2: Equilibre acide-base. M r. N. HEBBAR. 12. Chapitre 2: Equilibre acido-basique. 1. Définitions des acides et des bases. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte. A est appelé nombre de masse il désigne le nombre de nucléons (protons + neutrons). |
| 7 Transferts de protons Equilibres acide-base - EPFL |
| Chap TS acide-base |
| Chap VI: Equilibres acido- basiques – Transfert de protons - F2School |
| Réactions chimiques par transfert de protons - Prof-TC |
| Transformations chimiques en solution aqueuse - Chimie en PCSI |
| Transformations chimiques en solution aqueuse - Chimie en PCSI |
| Réactions acide-base en solution aqueuse - PTSI Ginette |
| Mécanismes de transfert de proton dune réaction acido-basique en |
| Rappel sur les Acides et les Bases |
| Chapitre 13 : réaction chimique par échange de proton H+ |
|
Cours 5 - Equilibres Acido-basiques
Chap VI: Equilibres acido- basiques – Transfert de protons Objectifs : Définir un couple acide/base Exprimer une constante d'acidité K A /pK A |
|
Réactions chimiques par transfert de protons - Prof-TC
être modélisées par des transferts de protons H+ entre les espèces impliquées Si l'on note AH l'acide et A− sa base conjuguée, le transfert protonique s'écrit traduire cet équilibre, l'équation de la réaction ne s'écrit pas avec une flèche |
|
Réaction chimique par transfert de protons - JM Podvin
Les réactions par transfert de protons Réaction chimique par transfert Définition : Un couple acide/base est l'ensemble d'un acide et d'une base qui se La constante d'acidité KA est la constante d'équilibre de la réaction d'un acide |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
Un acide est un donneur de proton et une base un accepteur de proton » Cet équilibre de transfert de proton est caractérisé par sa constante d'équilibre K°, |
|
Mécanismes de transfert de proton dune réaction acido-basique en
Mots-clés : Transfert de proton, réactions acide-base, dynamique moléculaire ab- initio, concentrations initialement hors équilibre, ce sont les principes de la |
|
Chap TS acide-base
Ainsi il y a transfert de proton et on peut écrire la réaction entre l'acide La constante d'acidité KA est la constante d'équilibre associée à l'équation de la |
|
E Q U I L I B R E A C I D E – B A S E
Nous allons, dans ce chapitre appliquer les concepts d'équilibre chimique à l' étude des réactions On constate que le proton cédé par l'acide 2, l'eau, est capté par la base 1, l'ammoniaque Il y a Il y a transfert de proton d'un acide d' un |
|
Ch13 REACTION CHIMIQUE PAR ECHANGE DE PROTON
Un transfert de proton a lieu entre les 2 couples acide / base 4) Notion d' équilibre chimique Dans certaines réactions chimiques, le réactif limitant ne disparaît |