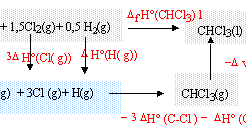
exercice loi des gaz parfaits
|
«EXERCICES ET PROBLEMES CORRIGES DE
Il comporte des exercices d'application concernant la loi du gaz parfait le premier et le second principe de la thermodynamique et les équilibres chimiques |
|
Exercice 1 : Constante des gaz parfait Calculer la constante des gaz
Exercice 2 : Loi des gaz parfaits 1 Un contenant est rempli d'un gaz parfait a- Quelle sera la pression du gaz b- A quelle température la pressi |
|
Exercices sur les gaz parfaits (chapitre 4)
1- Le méthane est considéré comme un gaz parfait Calculer le nombre de moles de méthane contenues dans cette citerne 2- Écrire l'équation- bilan équilibrée de |
|
Loi-des-gaz-parfaits-exercices-corrigespdf
loi des gaz parfait 1) Enoncer la loi de Boyle-Mariotte 2) Enoncer la loi du gaz parfait 3) On remplit un ballon de volume V = 4 L avec de l'Hélium La |
|
Série 1
Exercice 1 Les conditions sur la planète Mars sont très différentes de celles Utiliser la loi du gaz parfait Exercice 4 Considérer l'explosion de 23 4g |
Comment appliquer la loi des gaz parfaits ?
Une mole d'un gaz a le même volume qu'une mole d'un autre gaz à la même température et à la même pression.
L'équation du gaz parfait s'exprime ainsi : P V = n R T où est la pression, le volume, le nombre de moles, la constante des gaz et la température.Le physicien italien Amadeo Avogadro a déclaré en 1811 que le volume des gaz était proportionnel au nombre de molécules (moles, symbole « mol ») qu'ils contiennent.
Si on augmente la quantité d'un gaz, son volume augmentera aussi.
Quel est le volume V occupé par une mole de gaz parfait à θ 20 C et sous une atmosphère ?
Il s'agit d'une grandeur molaire.
Le volume molaire d'un gaz parfait est de 22,414 l/mol (soit 0,022 414 m3/mol ) dans les conditions normales de température et de pression (CNTP : 0 °C et 101 325 Pa ) et de 24,055 l/mol à 20 °C sous 1 atm .
Quelle est l'équation des gaz parfaits ?
D'où vient l'équation des gaz parfaits : PV = nRT.
|
Exercices de Thermodynamique
Rép : 1) UH2O(g) ne vérifie pas la première loi de Joule : H2O(g) ne se comporte pas comme un gaz parfait. Modélisation de VdW : a = 923.10?1 J.m?3.mol?1 et |
|
EXERCICES DE CHIMIE GÉNÉRALE
Utiliser la loi du gaz parfait. Exercice 4. Considérer l'explosion de 23.4g de nitroglycérine à 25°C: 4 C3H5(NO3)3(l) |
|
«EXERCICES ET PROBLEMES CORRIGES DE
Exercices et problèmes corrigés de thermodynamique chimique. 11. CHAPITRE I. LOI DES GAZ PARFAITS ET LE PREMIER. PRINCIPE DE LA THERMODYNAMIQUE |
|
Santé
Mélange de gaz parfaits – Loi de Dalton (1801). La pression totale exercée par un mélange de gaz parfaits est égale à la somme des. |
|
Exercices sur les gaz parfaits (chapitre 4)
Données pour tous les exercices: Constante des gaz parfaits R = 8314 Donner l'équation d'état d'un gaz parfait en indiquant le nom et l'unité de chaque ... |
|
1 Premier exercice : Gaz parfait 2 Second exercice : Mélange idéal 3
Choisissez vous-même la valeur de la constante R des gaz parfaits (n'essayez pas d'être trop précis). 3 Troisi`eme exercice : Loi de Laplace. Un gaz parfait |
|
Chapitre 13 : Les gaz parfaits
Loi des gaz parfaits : P×V = n×R×T. 3) Exercices d'application : a. Un récipient de 200 L contient 1 |
|
Génie de la Réaction Chimique: les réacteurs homogènes
14 juil. 2022 Exercice : QCU - Débit volumique en phase gazeuse ... espèces la loi des gaz parfaits peut être appliquée à plus haute pression). |
|
Physique Statistique Exercices de Travaux Dirigés
4.1 Gaz parfait classique monoatomique – Formule de Sackur-Tetrode . même loi universelle Pt(x) dans la limite d'un grand nombre de pas. |
|
Série de TD n°01 Thermodynamique
Exercice 2. 1. Citer les lois des gaz parfaits. 2. Un cylindre contient 765 mL de gaz de propane à la pression de 125·105 Pa. Quel serait le. |
|
EXERCICES DE CHIMIE GÉNÉRALE
Exercice 1 Les conditions sur la Utiliser la loi du gaz parfait Exercice 4 proviennent de l'explosion, qu'ils se comportent comme des gaz parfaits et que la |
|
Exercice 2 Etude dun mélange de gaz parfaits
Exercice 2 Etude d'un mélange de gaz parfaits Mélange initial pour l'ensemble des 2 expériences : Un mélange gazeux est constitué de diazote N2 et de |
|
Exercices sur les gaz parfaits - [Physiqueenstifreefr]
En négligeant la variation de volume, calculer la pression absolue à l'intérieur du pneu Exercice n°4: citerne de gaz (AE 1998) Une citerne est remplie de |
|
Les gaz parfaits - Physagreg
La loi de Boyle Mariotte est historiquement l'ancêtre de la loi des gaz parfaits : Elle dit : A température constante et pour une quantité de matière donnée on a : |
|
Gaz parfait
Exercice On considère un gaz enfermé dans un récipient de volume V = 48,7 L Le 2) Donner l'expression du volume V en utilisant la loi des gaz parfaits ? |
|
Quest-ce quun gaz parfait - Dunod
Mélange de gaz parfaits – Loi de Dalton (1801) La pression totale On a vu que la pression cinétique est donnée par (voir exercice 4 11) : P = 1 3 N V mu2 |
|
La loi des gaz parfaits
Loi des gaz Exercices AdM 1 La loi des gaz parfaits 1 a) A la surface de Vénus,la pression atmosphérique est de 75 atm Transformer cette pression en torrs |
|
La loi des gaz parfaits - Physicus
Le Sport – Chapitre 9 – La loi des gaz parfaits Un gaz contenant n (en mol) moles de molécules, à la pression p (en pascal), occupant un Exercice 10 p 300 |
|
Exercices PP349-357
1 La pression d'un gaz augmente si la fréquence APPLICATION • Sur le modèle de l'exercice résolu Utiliser la loi du gaz parfait et les unités Si dans le |