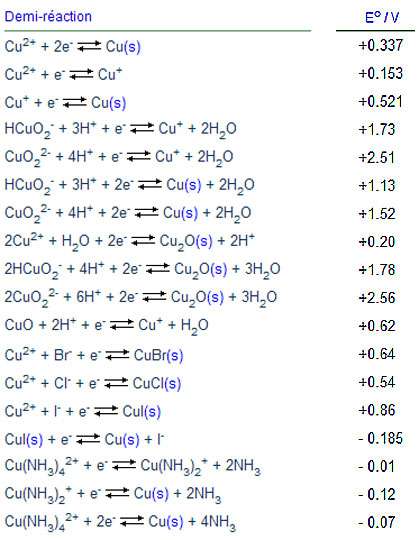réaction d'oxydoréduction fe2+/fe3+
|
EXERCICE RÉSOLU 2 - Action du permanganate sur les ions fer (II)
Chapitre 19 – Piles et oxydoréduction s'écrit comme la réaction de l'oxydant ... La demi?équation rédox pour le couple Fe3+ (aq)/Fe2+ (aq) s'écrit :. |
|
Étude dune réaction : titrage des ions fer II par les ions permanganate
violet et les ions fer II Fe2+ réagissent ensemble pour donner des ions manganèse Mn2+ |
|
Loxydo-réduction
On a donc un couple redox: oxydant/réducteur. (Fe3+/Fe2+). Chaque couple redox est représenté par la demi-réaction : Oxydant ne. Réducteur. |
|
Les réactions doxydo-réduction
Les réactions d'oxydo-réduction une réaction d'oxydoréduction correspond à un transfert d'électron(s) entre un ... équation du couple Fe2+ / Fe3+) :. |
|
Ecrire une équation bilan d
Ecrire une équation bilan d'oxydo réduction à partir des demi- Fe2+ ). (Zn. Zn2+ + 2e- ). 4. On ajoute ensuite membre à membre 2 Fe3+ + Zn. |
|
Cinétique de réaction du diiode oxydoréduction
Une réaction d'oxydoréduction met en jeu deux couples d'oxydoréduction : Ox1/Red1 et Ox2/Red2. 1/2 équation de réduction : ( Fe3+ + 1 e- ? Fe2+ ) x 2 ... |
|
TP de potentiométrie : éléments de correction 1 Question
Fe2+ = Fe3+ + e–. Cr2O7. 2– +6e– + 14 H+ = 2 Cr3+ +7H2O. Et l'équation-bilan de la réaction support du dosage potentiométrique s'écrit : 6 Fe2+ + Cr2O7. |
|
Définitions et équations redox
l'ion Fe2+ est le réducteur du couple Fe3+/Fe2+ mais il est l'oxydant du couple On notera à ce sujet |
|
Définitions et équations redox
l'ion Fe2+ est le réducteur du couple Fe3+/Fe2+ mais il est l'oxydant du couple On notera à ce sujet |
|
Les piles et loxydo-réduction :
solution d'ions ferriques Fe3+ et d'ions ferreux Fe2+ ; les concentrations respectives 3 - Décrire la nature des réactions d'oxydation et réduction se ... |
|
Les réactions doxydo-réduction - Physique - Chimie
Les réactions d'oxydo-réduction une réaction d'oxydoréduction correspond à un transfert d'électron(s) entre un équation du couple Fe2+ / Fe3+) : |
|
Cours-Réaction-redoxpdf
Dans les réactions d'oxydoréduction les électrons sont Fe3+/ Fe2+ Fe3+ + 1 e- Fe2+ Couple d'Oxydoréduction E0(Fe3+/Fe2+) = 0 77 ev |
|
1 Généralités sur loxydo-réduction
Si K est très grande on parle alors de réaction d'oxydoréduction Exemple : Ce4+ + Fe2+ ? Ce3+ + Fe3+ ; K?60 104 Par analogie avec les couples acido- |
|
Étude dune réaction : titrage des ions fer II par les ions permanganate
Les ions permanganate MnO4 - violet et les ions fer II Fe2+ réagissent ensemble pour donner des ions manganèse Mn2+ incolores et des ions fer III Fe3+ |
|
Chapitre 3 : Réactions doxydoréduction I Couple oxydant-réducteur
La réaction est totale à pH faible Le fer peut disparaître entièrement si l'acide est en excès Il y a CORROSION du fer • Fe2+ Fe3+ Fe |
|
Chapitre 1 - Définitions et équations redox
RÉACTION D'OXYDORÉDUCTION 15 Il en est de même pour l'ion Fe3+ et l'hydroxyde Fe(OH)3 Une espèce chimique qui est la forme oxydée (ou l'oxydant) dans un |
|
Chapitre 3 :Oxydoréduction - Melusine
I Réactions d'oxydoréduction 2NH3(s) = 3H2(g) + N2(g) est une réaction d'oxydoréduction sans échange réel Exemple : Fe3+/Fe2+ ; Fe3+ + e- = Fe2+ |
|
Cinétique de réaction du diiode oxydoréduction
Une réaction d'oxydoréduction met en jeu deux couples d'oxydoréduction : Ox1/Red1 et Ox2/Red2 1/2 équation de réduction : ( Fe3+ + 1 e- ? Fe2+ ) x 2 |
|
Oxydoréduction - cpge paradise
Les potentiels standard des couples du fer et de l'étain sont très différents (?E ? 0 6) La réaction 2 Fe3+ + Sn2+ 2 Fe2+ + Sn4+ sera donc totale Le |
|
Chapitre 2 : Réactions doxydoréduction - Lycée dAdultes
Les réactions d'oxydoréduction sont des réactions chimiques au cours desquelles il y a un échange d'un ou plusieurs électrons entre deux espèces chimiques 2 1 |
Quelle est la forme oxydée du couple rédox Fe3 +/ Fe2+ ?
La demi?équation rédox pour le couple Fe3+ (aq)/Fe2+ (aq) s'écrit : Fe3+ (aq) + e– = Fe2+ (aq). Fe2+ (aq) est donc une esp? chimique susceptible de céder des électrons, il joue donc le rôle de réducteur dans ce couple. ? (aq) est l'oxydant.Quelle est l'équation bilan de la réaction de l'ion Fe3+ sur le plomb pb ?
2 Fe3+(aq) + Pb(s) ? 2 Fe2+(aq) + Pb2+(aq). 3. La demi-équation du couple (aq)/Mn2+(aq) est : B.Comment écrire l'équation d'une réaction d'oxydoréduction ?
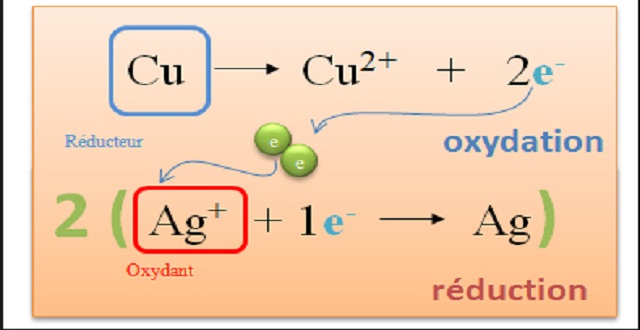
L'équation d'oxydoréduction s'obtient finalement en combinant les deux demi-équations et consiste en un transfert d'un ou plusieurs électrons du réducteur de l'un des couples à l'oxydant de l'autre couple. Les électrons n'apparaissent donc pas dans le bilan. écrire les demi-équations des deux couples impliqués.- Les couples redox
Un oxydant et un réducteur forment un couple redox si on peut passer de l'un à l'autre par gain ou perte d'électrons. Par convention, un tel couple est noté Ox / Red. L'ion Cu2+ et l'atome de cuivre Cu forment un couple redox noté : Cu2+ / Cu.
|
Les réactions doxydo-réduction - Physique - Chimie
une réaction d'oxydoréduction correspond à un transfert d'électron(s) entre un Fe2+ : réducteur du couple 1 MnO4 - : oxydant du couple 2 Fe2+ Fe3+ + e- |
|
Loxydo-réduction
Une réaction chimique qui modifie le degré d'oxydation d'un des éléments Exemple: Solution contenant 10-2 mole/l d'ions Fe2+ et 10-1 mole/l d'ions Fe3+ 3 |
|
Retour II - Le fer aux degrés +II et +III en solution III - La corrosion du
Quelques réactions: Milieu basique Fe2 I Fe2 I2 Milieu acide : OH2 Fe3)g( ON H4 ON Fe3 2 3 II 3 V 2 + + + + + ← → + − + anodique (ou par Cl2) de suspension d'oxydes ou par fusion du fer dans KNO3 Ils ont un caractère |
|
Cinétique de réaction du diiode oxydoréduction
Une réaction d'oxydoréduction met en jeu deux couples d'oxydoréduction : Ox1/ Red1 et Ox2/Red2 1/2 équation de réduction : ( Fe3+ + 1 e- → Fe2+ ) x 2 |
|
Titrage des ions fer II par les ions permanganate
Étude d'une réaction : titrage des ions fer II par les ions permanganate -(aq) + 8 H+ + 5 Fe2+(aq) → 5 Fe3+(aq) + Mn2+(aq) + 4 H2O(l) 5) Bilan des grandeurs |
|
Réactions doxydo-réduction : - pontonniers-physique
Le couple Fe3+/Fe2+ est situé en dessous du couple Ag+/Ag On met en présence des ions Fe2+ et des ions Cu2+ Aucune réaction n'a lieu Fe3+ est un oxydant |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
EQUATION DE LA DROITE FRONTIERE ENTRE FE(OH)3(S) ET FE2+ ions Fe3+ ou Fe2+, et quels sont les domaines d'existence des solides Fe(OH)2(s), élément chimique en fonction du pH (voire pL) et du potentiel E d'oxydoréduction |
|
Fe3+ Fe2+
La partie rouge correspond à une lave oxydée, riche en Fe3+ alors que la partie -Etude des cinétiques in situ d'oxydo-réduction -Mécanismes et réactions |
|
Réactions doxydoréduction I- Mise en évidence 1) Réaction entre le
Fe2+ cuivre Cu ions sulfate SO 4 2- (aq) Etat initial : cuivre Cu ions argent Ag+ (aq) Fe3+ (aq) ions chlorure Cl- (aq) ions iodure I- (aq) ions potassium K+ (aq) Une réaction d'oxydo-réduction fait intervenir deux couples oxydant |
|
Réactions doxydoréduction - Lycée dAdultes
l'équation bilan suivante : 5 Fe2+ (aq) + MnO4 – (aq) + 8H+ (aq) 5 Fe3+ (aq) + Mn2+ (aq) + 4H2O(l) 2 4 Equilibre d'oxydoreduction en milieu basique |