autoprotolyse de l'eau
|
3/ AUTOPROTOLYSE DE LEAU :
La réaction entre deux molécules d'eau (appelée autoprotolyse de l'eau et d'équation 2 H2O(ℓ) ⇌ H3O+ (aq) + HO− (aq)) est très limitée et mène à un |
|
Activité : Autoprotolyse de leau
L'autoprotolyse de l'eau L'eau pure ne contient pas uniquement des molécules d'eau H2O L'eau même très pure contient toujours des |
|
AUTOPROTOLYSE DE LEAU-pH DUNE SOLUTION AQUEUSE
AUTOPROTOLYSE DE L'EAU-pH D'UNE SOLUTION AQUEUSE- INDICATEURS COLORES Exercice 1 : Les questions sont indépendantes 1) Calculer le pH d'une solution |
|
Équilibre de lautoprotolyse de leau
L'eau réagit selon une réaction d'autoprotolyse pour former les ions H3O+ et OH- Il y a donc des ions libres dans l'eau La conductivité est cependant très |
|
Fiche 2 : équilibres acidobasiques
Autoprotolyse de l'eau : dans toute solution aqueuse il existe au moins un équilibre appelé autoprotolyse de l'eau qui résulte de la réaction acide base |
|
IIILeau
L'eau Chapitre III 25 3) Le produit ionique de l'eau Appliquons la loi de Guldberg et Waage à l'équilibre d'autoprotolyse de l'eau : En principe les |
|
PH DUNE SOLUTION AQUEUSE AUTOPROTOLYSE DE LEAU
pH D'UNE SOLUTION AQUEUSE AUTOPROTOLYSE DE L'EAU PRODUITS IONIQUE INDICATEURS COLORÉS I pH d'une solution aqueuse : 1 Définition : |
C'est quoi la réaction d Autoprotolyse de l'eau ?
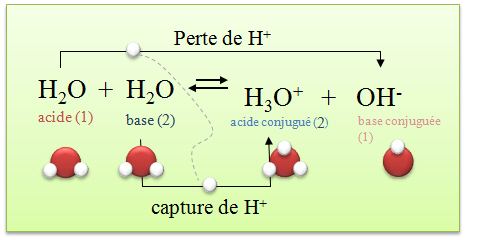
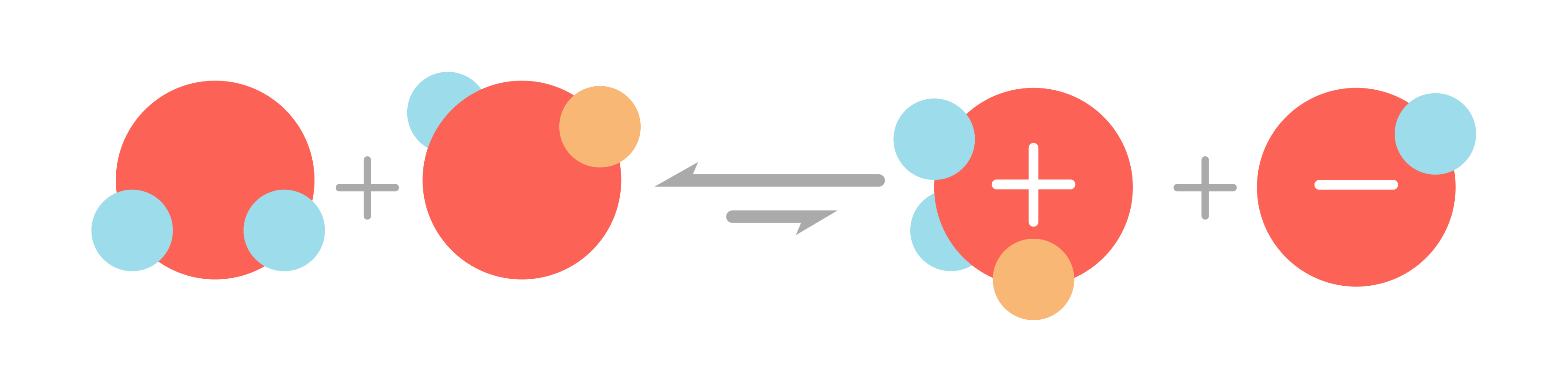
Comme les acides et les bases réagissent entre eux, l'eau peut réagir avec elle-même En fait, des molécules d'eau échangent des protons entre elles, en toute petite quantité.
On appelle cette réaction l'autoprotolyse de l'eau.Quel est l'équation d Autoprotolyse de l'eau ?
Selon l'équation d'autoprotolyse de l'eau : ✅ H2O + H2O ⇌ H3O+ + OH-
Quand on néglige l Autoprotolyse de l'eau ?
Si la concentration d'un acide ou d'une base en solution est suffisamment grande, la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH– peut être négligée.
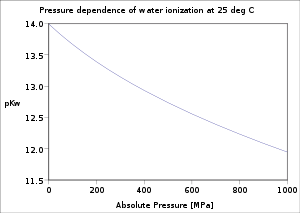
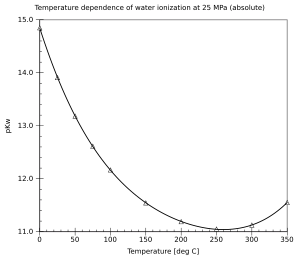
Dans le cas de la solution d'un acide suffisamment concentré, [OH–] peut être négligée dans l'expression du bilan de charges.- Le processus est endothermique, de sorte que l'étendue de l'ionisation et les concentrations d'ions hydronium et d'ions hydroxyde qui en résultent augmentent avec la température.
Par exemple, à 100 °C, la valeur de Kw est d'environ 5,6 × 10-13, soit environ 50 fois plus que la valeur à 25 °C.
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide ou d'une base en solution est suffisamment grande la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH–. |
|
30 1. a. La réaction dautoprotolyse de leau est : 2 H O (?) H O+ (aq
= 10 × 10?7 mol · L?1. pH = ? log (1 |
|
TP no10 - Calorimétrie I Matériel disponible II Mesure de lenthalpie
lyse de l'eau : 2 H2O = HO? + H3O+ de la comparer à la valeur théorique |
|
Fiche Chimie - Acide fort base forte et pH
3 + initiaux proviennent de l'autoprotolyse de l'eau donc ?i = i = 10?7 . • La simple fl`eche « ? » implique que la réaction - + 3 +. |
|
Chap 6 acide-base
Comme l'eau est une espèce chimique qui peut être soit acide soit basique c'est un ampholyte. III. Autoprotolyse de l'eau : 1) pH de l'eau pure. |
|
III..Leau
Les ions hydronium ou hydroxyde ont en effet dans ce cas |
|
TS1 cours chimie 2
19 nov. 2009 Savoir que Ke est une constante d'équilibre associée à l'équation de la réaction d'autoprotolyse de l'eau. •. Connaissant la valeur du pH d'une ... |
|
3/ AUTOPROTOLYSE DE LEAU :
3/ AUTOPROTOLYSE DE L'EAU : Activité de découverte correction. ? Rappeler les couples acide/base de l'eau : H2O/HO? et H3O+/H2O. |
|
7. Transferts de protons Equilibres acide-base
L'ammoniac NH3 capte un proton H+ de l'eau pour former NH4+. La réaction de dissociation de H2O est appelée l'autoprotolyse de l'eau. Sa. |
|
3/ AUTOPROTOLYSE DE LEAU :
3/ AUTOPROTOLYSE DE L'EAU : Activité de découverte correction ? Rappeler les couples acide/base de l'eau : H2O/HO? et H3O+/H2O |
|
1 – Leau solvant des réactions acido-basiques
L'autoprotolyse de l'eau 2 Le produit ionique de l'eau 3 L'échelle de pH B : Acides et bases selon Bronsted 1 Définition 2 Les couples acide/base |
|
Autoprotolyse de leau et le pH - Lachimienet
L'autoprotolyse de l'eau Mesurons la conductivité d'une solution d'eau déminéralisée ( qui à priori ne contient pas d'ions) La mesure de conductivité obtenue |
|
PH DUNE SOLUTION AQUEUSE AUTOPROTOLYSE DE LEAU
Autoprotolyse de l'eau : La présence des ions H3O+ dans l'eau résulte de l'ionisation partielle de l'eau selon l'équation : |
|
Autoprotolyse-de-l-eaupdf - E-monsite
AUTOPROTOLYSE DE L'EAU-pH D'UNE SOLUTION AQUEUSE- INDICATEURS COLORES 2) Quelles sont les concentrations en ions hydronium et en ions hydroxyde d'une |
|
[ ] [ [ ]éq - AlloSchool
Cette réaction dans le sens (1) s'appelle la réaction d'autoprotolyse de l'eau ?Le pH de l'eau pure à 25 o C est : pH=7 donc l'eau pure est |
|
IIILeau
[H2O]o = 5536 mol/l Equation 1: concentration formelle de l'eau dans l'eau pure H2O + H2O H3O+ + OH- Equation 2 : autoprotolyse de l'eau |
|
I Réaction dautoprotolyse de leau et produit ionique de leau II
On définit le pKe de l'eau par pKe=?log Ke Remarque : La réaction d'autoprotolyse de l'eau a lieu dans toute les solutions aqueuses Donc la relation Ke=[H3 |
|
Activité : Autoprotolyse de leau
Activité : Autoprotolyse de l'eau Les solutions sont acides si elles contiennent majoritairement des ions oxonium H3O + et basiques si elles |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
Si la concentration d'un acide ou d'une base en solution est suffisamment grande la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH– |
Quelle est l'équation de l autoprotolyse de l'eau ?
. Nous pouvons donc retrouver les concentrations de ces ions.
Pourquoi négliger l autoprotolyse de l'eau ?
. Dans le cas de la solution d'un acide suffisamment concentré, [OH–] peut être négligée dans l'expression du bilan de charges.
C'est quoi le Pke ?
C'est quoi le produit ionique de l'eau ?
|
Acide fort, base forte et pH - Fiche Chimie
3 + initiaux proviennent de l'autoprotolyse de l'eau, donc ℎi = i = 10 −7 • La simple fl`eche « → » implique que la réaction - + 3 + |
|
PH dune solution Autoprotolyse de leau Produit - Numeriksciences
Autoprotolyse de l'eau C'est la réaction entre deux molécules d'eau Il y a transfert de proton H+ entre la forme acide de l'eau et sa forme basique Les couples |
|
Réactions acido-basiques I Autoprotolyse de leau Inévitablement a
I Autoprotolyse de l'eau Inévitablement a lieu dans l'eau pure l'équilibre dépendant de la Pour l'eau pure h = oh = √Ke soit pH = pOH = ½ pKe = 7 • Solution |
|
IIILeau
[H2O]o = 55,36 mol/l Equation 1: concentration formelle de l'eau dans l'eau pure H2O + H2O H3O+ + OH- Equation 2 : autoprotolyse de l'eau [H3O + ] = [OH |
|
Wwwlachimieorg 1 La constante dautoprotolyse de leau, KW, est
La constante d'autoprotolyse de l'eau, KW, est égale au produit de Ka par Kb pour un couple acide/base donné : KW = [H3O+] [OH-] = 10-14 = KaKb à 25°C |
|
E Q U I L I B R E A C I D O B A S I Q U E
HO = produit ionique de l'eau Il s'agit de l'autoionisation ou autoprotolyse de l' eau Cette réaction acide-base résulte de l'interaction entre le couple H 3 O+ /H |
|
Cours 5 - Equilibres Acido-basiques
L'autoprotolyse de l'eau : l'eau est une espèce amphotère, elle réagit sur elle- même selon la réaction : 2 H O (l) = H O+ (aq) + OH- (aq) □ L'autoprotolyse de |
|
Solution et ph terminale autoprotolyse acide base - E-monsite
2) A 37°C, le produit ionique de l'eau pure est tel que pKe=13,6 a) Définir à cette température ce qu'est une solution neutre, acide et basique b) La salive |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH– peut être négligée Dans le cas de la solution d'un acide suffisamment concentré, |