Mise en solution des sels
|
La chimie des sels fondus applications au CEA Marcoule
Service modélisation et chimie des procédés de séparation sels fondus activités au CEA Marcoule PAGE 1 E Mendes J Serp L Diaz D Quaranta G Serve M Bertrand La chimie des sels fondus applications au CEA Marcoule D irection de l’ E nergie N ucléaire D épartement de R adio C himie et P rocédés S ervice de M odélisation et C |
|
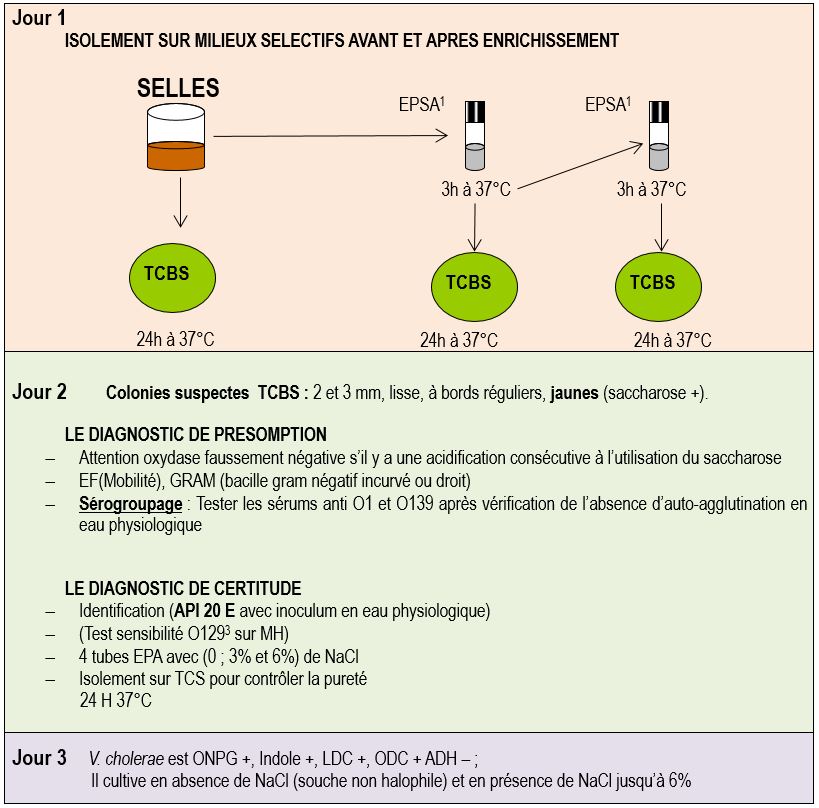
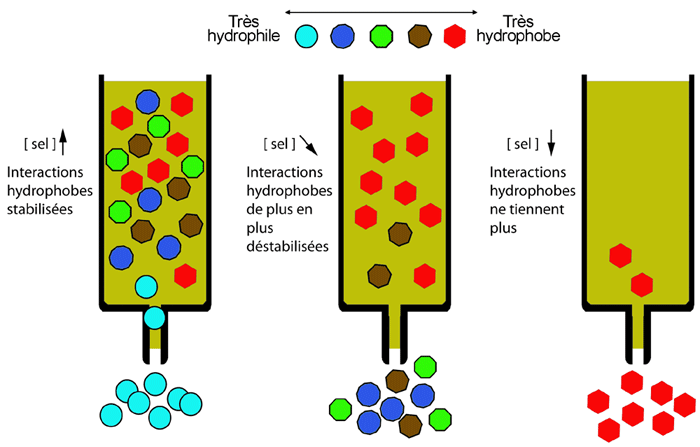
MISE EN SOLUTION
MISE EN SOLUTION 1- SOLVATATION La mise en solution a pour effet d’étendre le volume du soluté à celui du solvant Ce dernier a pour fonction principale de disperser les composés introduits en exerçant une réactivité chimique aussi limitée que possible à leur encontre Mis à part l’eau ou la plupart |
|
Solvatation
-Mise en solution A/ d'un composé Vocabulaire 3 B/ Disolution d'espèces non ionisables |
|
© 2000 Université de Liège Section de Chimie Groupe
par les solutions aqueuses Il observe que les solutions de sels d’acides et de bases conduisent le courant Il énonce sa «théorie des ions » (1884) ce qui l’amène à proposer les définitions suivantes pour les acides et les bases : ″ Un acide est une substance qui en solution aqueuse libère des ions H + ″ eau ex |
Comment est formé le sel ?
Le sel, dans chaque cas, est formé en combinant l’anion de l’acide et le cation de la base. Pour nommer un sel, le nom de l’anion est écrit en premier, et on lui donne le suffixe -ure pour les ions avec un seul élément, ou -ite ou -ate pour les ions polyatomiques contenant de l’oxygène.
Comment préparer un sel soluble ?
L’anion de l’acide et le cation de la base forment le sel soluble nitrate de cuivre (II) ( C u ( N O) () 3 2 a q ), et les ions hydrogène de l’acide ainsi que l’ion oxyde de la base se lient pour former de l’eau. Un élève veut préparer un sel en utilisant de l’oxyde de cuivre (II), une base insoluble et de l’acide sulfurique.
Quels sont les différents types de réactions qui produisent des sels ?
Il y a de nombreuses réactions qui produisent des sels, dont les suivantes : Le tableau suivant montre une sélection de sels qui peuvent être formés à partir de réactions acido-basiques. L’anion de chaque acide est représenté en rouge et le cation de chaque base en bleu.
Quels sont les différents types de sels ?
Aussi appelés sels acides. Ils sont produits à partir de tels acides dans lesquels tous les atomes d’hydrogène n’ont pas été remplacés par des cations métalliques. Les sels basiques sont des sels dans lesquels tous les atomes d’hydroxyde n’ont pas été remplacés par des anions radicaux acides.
II
-Mise en solution A/ d'un composé Vocabulaire . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . . 3 . . . . . . . B/ Disolution d'espèces non ionisables . . . . . . . . . . . . . . . . . .
Introduction
sique, recteur, énoncées. pédagogique Ce des cours solutions, fait appel à thermodynamique, des .). notions de Il utilise nombreux l'eau domaines de comme exemple la di- chimie chimie parce que ce solvant présente un grand nombre de propriétés qui vont Dicultés : diérence diérence entre entre polarité disolution et et caractère disociant ; solvatat
Dénition
les solutés. Il Solvatation : s'agit généralement d'interactions électrostatiques, de van der Waals, voire de liaisons H. Les solutés sont alors dits Dans ce cours, on se focalisera sur le intérêt réside dans ses propriétés exceptionneles, solvant que nous le plus important développerons en chimie et : l'eau. Son ce cours. I - déterminer perso.ens-lyon.fr
Objectifs
particulier de l'eau. Connaître Déterminer le et mécanisme calculer de une disolution enthalpie d'un de composé. disolution. Caractéristiques du solvant An caractéristiques. de choisir un solvant pour une synthèse ou une extraction, il est ses le solvant. création d'interactions stabilisantes entre le solvant et solvatés . en biolo-Connaître les ca
Classication
On des solvants peut ainsi claser solvants polaires, solvants polaires, posé. En solvants solvants Remarque protique. eet, Cete la les disociants disociants solvants et et en plusieurs catégories : protiques (eau) ; aprotiques (acétone) ; polaires, non disociants et aprotiques (acétate d'éthyle) ; apolaires, non disociants et aprotiques (cyclohexan
Vocabulaire
an de ne Il existe pas les de nombreux termes autour de la solvatation, qu'il est nécesaire de dénir confondre. perso.ens-lyon.fr
Dénition
d'une Dissolution : mélange de deux phases aboutisant à la formation unique phase homogène. B/ Solubilité : que peut Miscibilité : avoir ce soluté dans proches). Dissolution d'espèces le solvant considéré. concentration du soluté solubilité appliquée d'une solution saturée, à deux solvants (deux concentration maximale liquides dans des proportions
Dénition
à des Electrolyte solvatés. d'un . à composé être disocié en utilisant la notion fort : ions composé dont la disolution conduit totalement perso.ens-lyon.fr
Exemple
Dénition équilibre entre des ions Electrolyte solvatés et faible : le composé Le nitrate d'ammonium : NH non Exemple 3) Sphère de solvatation La réorganisation des molécules de solvant autour disocié solvaté. L'acide éthanoïque : CH de solvatation . sphère grande Ele est d'autant plus grande que la densité de de que solvatation cele autour de l'ion
0. En
soluté et le solvant. On peut de même dénir l' entropie standard de dissolution . Pour un solide ionique, de la on s'atend à disolution. ce qu'ele soit positive car on brise l'ordre du solide cristalin lors B/ Calcul des grandeurs standard de dissolution On considère la disolution de la soude dans l'eau : NaOH perso.ens-lyon.fr
Conclusion
Un solvant est caractérisé par sa polarité, liée à son moment disociant, lié à acide de Brønsted. son du solvant Le dans constante mécanisme lequel il diélectrique de est disolution disous. d'un S'il composé ne dipolaire , son caractère r, et son éventuele proticité s'il s'agit d'un dépend de peut être disociant, on asiste en 3 étapes : à une ionis
|
Réactions de dissolution ou de précipitation - Table des matières
Mise en solution d'un solide moléculaire......... C. Mise en solution d'un gaz ... Comment peut-on qualifier la réaction de dissolution du sel? |
|
Comparaisons entre différentes méthodes dextraction des sels
pas de mise en solution du gypse et n'extraient donc que les sels solubles de sodium. Pour l'extraction des cations échangeables dans. |
|
Les acides et bases en solution aqueuse.
La réaction de l'acide avec la base donne lieu à la formation d'un sel et d'eau. L'équation globale de mise en œuvre est donc :. |
|
La dissolution du carbonate de calcium
sels étrangers non homoïoniques accélèrent la dissolution surtout du fait velle mise en solution du CaCO |
|
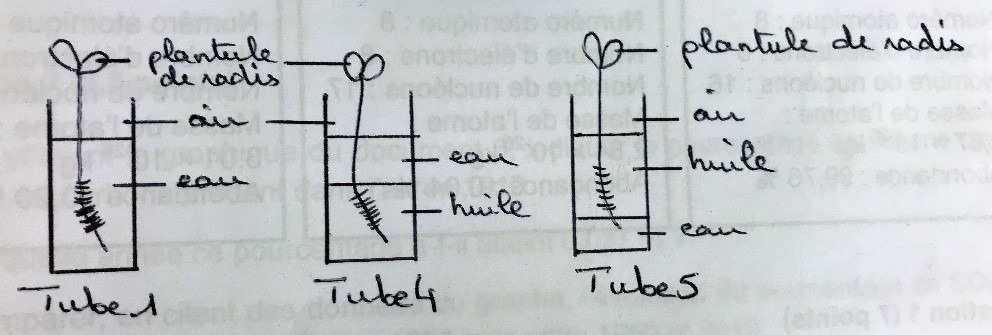
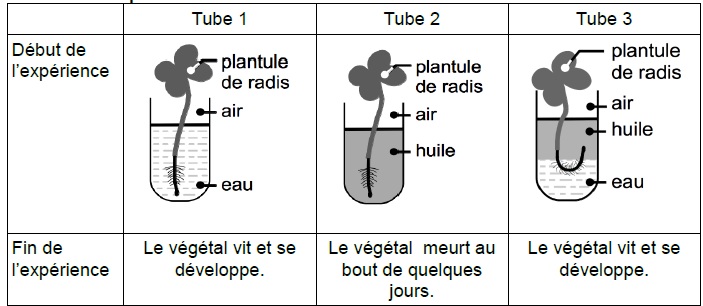
Production de la matière organique et flux dénergie
Mise en évidence des échanges d'eau chez les plantes chlorophyllienne 20 ml d'une solution de saccharose avec des concentrations croissantes allant de. |
|
Guide des bonnes pratiques dépandage
De façon générale l'eau liquide nécessaire à la mise en solution du sel est extraite du milieu environnant |
|
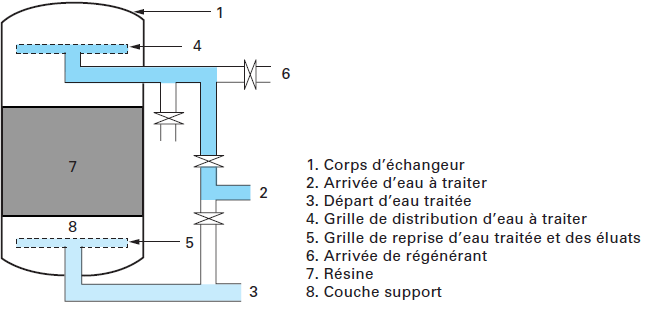
RÉACTEURS A SELS FONDUS
Après mise en solution du sel par un mélange HNOg 15 M -. AL(N0g)3 0 |
|
Guide traitement thermique
5.5.1.1 La mise en solution de l'alliage Al – Cu5 % (ASTM 204 ou AFNOR A-U5 GT). sera sursaturée et il y aura apparition d'un précipité ou excès de sel. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
La fonction ? n l |
|
La Chimie en solution
du type : acide + base? sel + solvant. II - Calculs de pH en milieu aqueux (Rappels). Utilisation des logarithmes décimaux : log(a b) log a log b. |
|
Comparaisons entre différentes méthodes dextraction des sels
pas de mise en solution du gypse et n'extraient donc que les sels solubles de sodium Pour l'extraction des cations échangeables dans les horizons sulfatés et |
|
Études relatives à la décomposition des sels métalliques - Numdam
proportion d'acide mis en liberté atteigne une certaine valeur limite A partir de ce du sel double quand la solution contient par litre plus de ^5 grammes |
|
Chimie
Résolution On admet que le sel sec est une solution à ω2 = 100 On Les cellules plasmolysées mises dans une solution isotonique gonflent de nouveau |
|
Détermination de la formule du sel de Mohr - AC Nancy Metz
Le sel de Mohr a pour formule FeSO4,(NH4)2SO4, x H2O Le but du dosage On réalise le dosage des ions Fe2+ d'une solution S1 obtenue par dilution de S0 par une solution de Mise en service : ajustage du zéro, absence de bulle d'air |
|
METHODES DANALYSE DE CONTROLE DE LA QUALITE DU SEL
solubilité dans une solution saturée de sel est inférieure à 6 grammes par litre ou Mode de mise en solution des échantillons - Prise de 1g ou 15 g agitée |