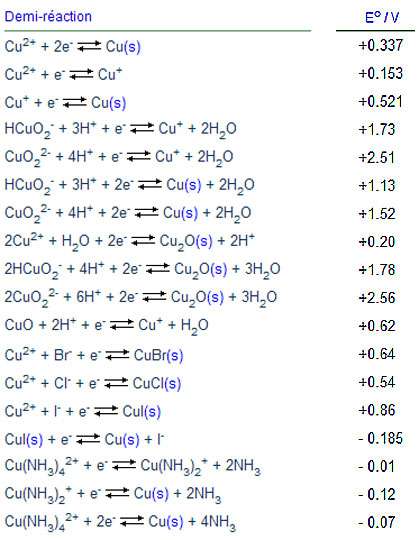demi equation redox i2/i-
|
Chapitre 3 :Oxydoréduction
Couple redox/oxydant réducteur : Ox/Red Notation : Red e Ox réduction oxydation = + − → ← n correspond à la demi équation |
|
Cinétique de réaction du diiode oxydoréduction
par une demi-réaction d'oxydoréduction : Ox + n e- → Red Une réaction d Equation bilan : 2 Fe3+ + 2 I- → 2 Fe2+ + I2 Seconde équation : 1/2 équation de |
|
Cours-Réaction-redoxpdf
Écriture des demi réaction du couples redox Ox + ne- Red On équilibre du I2 119 O2 H2O 123 Cr2O7 2- (ion dichromate) Cr 3+ (ion chromique) 1 |
|
Encre sympathique
I2(aq) et acide ascorbique C6H8O6(aq) Couples mis en jeu : I2(aq) / I-(aq) et C6H6O6(aq) / C6H8O6(aq) b) (4 pts) Demi-équations d'oxydoréduction : )(2 2)( 2 |
|
Loxydoréduction
Exemple : Cu2+ / Cu où Cu2+ est l'oxydant et Cu le réducteur La demi-équation est écrite pour les deux membres d'un même couple Ox / Red Ox + n e- = Red L' |
|
La réaction doxydoréduction
Etablr la demi-équation du couple : HclO(aq)/Cl2(aq) Etape n°1 : A partir de la définition précédente on peut écrire pour un couple Ox/Red la relation |
|
Les réactions doxydo-réduction
➔ Pour s'entraîner : « TS oxydoréduction demi équation » 4/ Les réactions d'oxydoréduction ➔ Le réducteur d'un couple (noté 1) peut participer à une |
|
Les réactions doxydo-réduction
Méthode d'équilibre d'une demi équation redox en milieu basique : - Equilibrer la demi-équation en milieu acide - Ecrire l'autoprotolyse de l'eau avec |
|
Réactions doxydo-réduction
Considérons les 2 couples Ox1/Red1 et Ox2/Red2 Écriture d'une réaction redox entre Ox1 et Red2 • Écrire la demi-équation du couple redox 1 dans le sens : Ox1 |
Comment faire une demi-équation redox ?
Une demi-équation d'oxydoréduction est une équation chimique représentant la transformation de la forme oxydée d'un couple en sa forme réduite conjuguée sans qu'intervienne un second couple rédox.
Qu'est-ce qu'une demi-équation redox ?
Le fer est essentiellement réduit (Fe2+) à haute température.
La partie rouge (centre du cône) correspond à de la lave qui a été réchauffée pendant l'éruption.
Cette lave est restée longtemps à 700-900°C et c'est oxydée, riche donc en Fe3+.Comment passer de Fe2+ à Fe3+ ?
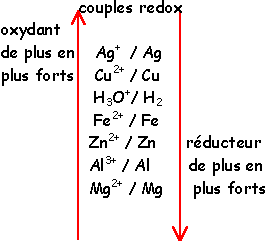
Un oxydant est une espèce chimique capable de capter des électrons alors qu'un réducteur est une espèce chimique capable de les céder.
|
La réaction doxydoréduction
Les halogènes (F2; I2; Cl2;. O2) sont de puissants oxydants. 1.5)Etablir la demi-équation d'un couple. On étudie dans cet exemple le couple MnO4. |
|
Correction de lexercice « Encre sympathique »
C'est l'oxydant du couple I2(aq) / I-(aq). L'acide ascorbique présent dans le b) (4 pts) Demi-équations d'oxydoréduction : )(2. 2)(. 2. aqI e. aqI. −. − = +. |
|
Cinétique de réaction du diiode oxydoréduction
On fait la somme des 2 demi-équations pour obtenir l'équation bilan. 4 x (Cr2O7. 2-+ Equation bilan : 2 Fe3+ + 2 I- → 2 Fe2+ + I2. Seconde équation : 1/2 ... |
|
Les réactions doxydo-réduction
➔ Pour s'entraîner : « TS oxydoréduction demi équation ». 4/ Les réactions d'oxydoréduction. ➔ Le réducteur d'un couple (noté 1) peut participer à une |
|
CORRIGÉ
1 août 2020 (1) et (2). C'est la même demi-équation pour le couple I2/I- qui intervient : ... 10- Écrire les demi-équations redox dans lesquelles ... |
|
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Ecrire les demi-équations relatives aux couples Redox suivants : Cu2+/Cu. Fe2+/Fe. S4O6. 2–/S2O3. 2–. I2/I–. MnO4. –/Mn2+. O2/H2O2. Ag+/Ag. Fe3+/Fe. Corrections. |
|
école numérique - thème : oxydoréduction titre de la leçon : couples
L-1 en milieu acide. 1. Écris les demi- équations électroniques et l'équation- bilan. 2. Calcule la concentration en diiode I2 et en ions |
|
CM80 : Examen final — corrigé 1 Aspartame et neotame (667pts)
D'où la demi-équation redox : I2 + 2e– = 2I– . — couple RCHO/RCO2. – : n.o. (C/RCHO) = +I ; n.o. (C/RCO2. – ) = +III. D'où la demi-équation redox : RCO2. – + |
|
Chapitre 5 : diagrammes potentiel-pH (E-pH) et potentiel-pL
Oxydoréduction (entre des espèces de n.o. différents). Ecriture de la demi-équation rédox utilisation de la formule de. Nernst puis de la convention de |
|
Loxydoréduction
La demi-équation est écrite pour les deux membres d'un même couple Ox / Red + 5.I2 + 16.HO- à gauche H+ + HO- donne H2O : 2.MnO4. - +16.H2O +10.I-. 2Mn. |
|
La réaction doxydoréduction
Soit le couple I2/I- (diiode/ion iodure) établir la demi-équation de ce couple : qui cède des électrons et l'oxydant d'un autre couple redox qui les. |
|
Correction de lexercice « Encre sympathique »
a) (1 pt) Le diiode I2 de couleur brune en solution aqueuse |
|
CORRIGÉ
1 août 2020 C'est la même demi-équation pour le couple I2/I- qui intervient : ... 10- Écrire les demi-équations redox dans lesquelles interviennent les ... |
|
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
b) Il s'agit d'une réaction d'oxydoréduction car il a un échange d'électrons entre deux espèces (I2 l'oxydant et S2O3. 2- le réducteur). c) Volume de solution |
|
CM80 : Examen final — corrigé 1 Aspartame et neotame (667pts)
couple I2/I– : n.o. (I/I2) = 0 ; n.o. (I/I– ) = -I. D'où la demi-équation redox : I2 + 2e– = 2I– . — couple RCHO/RCO2. – : n.o. (C/RCHO) = +I ; n.o. (C/RCO2. |
|
Cinétique de réaction du diiode oxydoréduction
On multiplie la demi-équation d'oxydation par le nombre d'électrons intervenant dans la demi- Equation bilan : 2 Fe3+ + 2 I- ? 2 Fe2+ + I2. |
|
LES THIOLS.pdf
L'équation bilan s'écrit : Les couples oxydant /réducteur présents sont : - Diiode / ion iodure : I2 / I-. Demi équation : I2 + 2 e- = 2I- (1). |
|
école numérique - thème : oxydoréduction titre de la leçon : couples
captant des électrons selon la demi-équation électronique : est un réducteur et ils forment le couple redox ... On donne les couples redox I2 I?. |
|
Les réactions doxydo-réduction
On décrit cette double possibilité par une « demi-équation » électronique : oxydant + n e- Pour s'entraîner : « TS oxydoréduction demi équation ». |
|
Loxydoréduction
2) Établir l'équation en milieu acide |
|
Lecture 11 Redox Chemistry - Stanford University
Redox reactions are written as half-reactions which are in the form of reductions (which means an element is transformed from a higher oxidation state (e g +II) to a lower oxidation state (e g +I)): Ox + ne- = Red; Where the more oxidized form of an element is on the left and the reduced form is on the right n is the number of electrons |
|
7014 Redox Chemistry Handout - Massachusetts Institute of
There are three ways to represent a redox reaction; these are shown below with a representative biological redox reaction: acetaldehyde + NADH + H + ethanol + NAD + (1) Overall Reaction: (2) Electron-transfer diagram: acetaldehyde NADH + H + e-NAD + ethanol (3) Half-reactions: acetaldehyde + 2 H + + 2 e-ethanol + NADH NAD + + H + + 2 e- |
|
Balancing REDOX Reactions: Learn and Practice
Apr 17 2013 · Here the equation is already written in an ionic equation format so we must do some more work to assign oxidation numbers (see ebook rules) ClO3¯ (aq) + I2 (s) à IO3¯ (aq) + Cl¯(aq) Oxidation Numbers: +5 -2 0 à +5 -2 -1 Yes the Iodine (I) has been oxidized and the Chlorine (Cl) has been reduced |
|
Oxidation- Reduction Chemistry - WRUV
Half-Reactions ØConsider each process indivually: Oxidation Cu (s) ? Cu2+ (aq) + 2 e-Reduction [Ag+ + e-? Ag (s) ] x 2 Overall: Cu (s) + 2Ag+ (aq) ? Cu2+ (aq) + 2Ag (s) Oxidized (reducing agent) Reduced (oxidizing agent) 4 Balancing Redox Reactions Ø The Half-Reaction Method Three Steps: 1 Determine net ionic equations for both half |
|
Searches related to demi equation redox i2/i PDF
During a REDOX reaction electrons are transferred directly from the reducer to the oxidizer with no separation of the two reactions • If we were able to isolate the half reactions into separate containers and connected the two containers electrically using platinum wire electrodes and a volt meter we could then measure that potential • |
What are half-equations in a redox reaction?
These two equations are described as "eelectron-half-equations," "half-equations," or "ionic-half-equations," or "half-reactions." Every redox reaction is made up of two half-reactions: in one, electrons are lost (an oxidation process); in the other, those electrons are gained (a reduction process).
How do you determine the direction of a redox reaction?
Note: to determine the direction of a redox reaction, you do not need to use the Nernst equation. You only need to know the sign of ?E'?. you must reverse the sign of E'? for a reaction if you reverse the direction of the reaction. Here reaction (2) must be reversed.
What is a redox reaction?
Redox reactions are a major determinant of chemical species present in natural environments. Znº - 2e- Zn2+ (an oxidation half reaction, electrons lost) Cu2++ 2e- Cuº (a reduction half-reaction, electrons gained) The two species comprising half-reactions (e.g. Znº & Zn2+) are referred to as a “couple”.
Can a redox titration be applied to a mixture of analytes?
As with acid–base titrations, we can extend a redox titration to the analysis of a mixture of analytes if there is a significant difference in their oxidation or reduction potentials. Figure 9.42 shows an example of the titration curve for a mixture of Fe 2+ and Sn 2+ using Ce 4+ as the titrant.
| Redox Chemistry April 1992 - University of Texas at Austin |
| Review: Balancing Redox Reactions |
| Méthode : cas du couple Cr2O72-/Cr3 - wifeocom |
| Les réactions d’oxydoréduction |
| 5 Oxidation and reduction: redox (Topic 3) |
| Section 92: Balancing Redox Reaction Equations Tutorial 1 |
| Searches related to demi equation redox i2/i filetype:pdf |
|
On obtient un couple oxydant / réducteur: H+ / H2 - Free
4 Des demi-équations rédox à l'équation d'oxydoréduction Expérience : Fe3+ / Fe2+ : Fe3+ + e = Fe2+ |
|
MÉTHODE POUR ÉCRIRE UNE ÉQUATION DOXYDO-RÉDUCTION
On écrit les demi-équations d'oxydoréduction dans le sens de la réduction pour l' oxydant 1 et dans le sens de l'oxydation pour le réducteur 2 On les additionne |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
Pour écrire la demi-équation d'un couple oxydant-réducteur en milieu basique, il faut : ➢ Écrire la demi –équation du couple en milieu acide donc avec des ions |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
Méthode : 1) Toujours commencer par écrire les demi-équations de chacun des couples en mettant à gauche du signe = le réactif effectivement introduit lors de |
|
Chapitre 3 :Oxydoréduction
Couple redox/oxydant réducteur : Ox/Red Notation : Red e Ox réduction oxydation = + − → ← n , correspond à la demi équation redox |
|
Oxydoreduction - Lycée Ismael Dauphin
A partir de ces deux demi-équations d'oxydoréduction, donner une équation chimique ayant pour seuls réactifs Cl2(g) et H2O Corrigé Exercice 1 : Ecrire les demi |
|
Solutions aqueuses 2 : réactions doxydo-réduction - UNF3S
Partie sur les piles : partie introductive à la notion de potentiel redox et de potentiel standard Formule de Nernst Savoir équilibrer des demi-équations et des |
|
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Cr2O7 2- + 14 H+ + 6 e-= 2Cr3+ + 7 H2O Applications Ecrire les demi- équations relatives aux couples Redox suivants : Cu2+/Cu Fe2+/Fe S4O6 2–/ S2O3 2– |