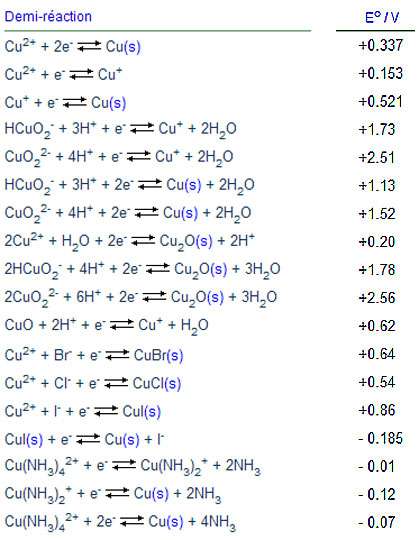couple redox clo-/cl-
|
Demi-equation-OxRed-basiquepdf
Exemple avec le couple (aq) (aq) - - ClO Cl (ion hypochlorite / ion chlorure) : Étape 1 : Écrire la demi-équation du couple en milieu acide 2 (aq) (aq) |
|
OXYDO
Na+ + e Oxydant : '' '' '' '' accepter '' Cl2 + 2e ! 2Cl Na est un réducteur ; Na+ est un oxydant ; couple rédox Na+ /Na Cl est un réducteur ; Cl2 est un |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
Exemple avec le couple. (aq). (aq). -. -. ClO. Cl (ion hypochlorite / ion chlorure) : Étape 1 : Écrire la demi-équation du couple en milieu acide. 2. (aq). (aq). |
|
BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
L'eau de Javel apporte les ions hypochlorite ClO–(aq). C'est un oxydant puissant formant |
|
FALA Tuto
14 avr. 2020 D) Pour le couple ClO-/Cl- en milieu basique |
|
Hypochlorites et eaux de Javel
Justifier le rôle oxydant de l'ion hypochlorite. On commence par établir les demi-équations rédox : CℓO-(aq) / Cℓ-(aq) : CℓO- + … C. ⇌ ℓ- + … on est en |
|
5 Diagramme E - pH du chlore
= + I sont un couple acide base HClO/ClO− puisque : HClO = ClO− + H+. On en La frontière 2 correspond au couple rédox HClO / Cl−. L'équa- tion de la ... |
|
Partie A Leau de Javel
Comparer le résultat à l'indication du berlingot. Données. • M(Cl) = 355 g·mol–1. • M(O) = 16 |
|
Table des potentiels standards
ClO. −. 3. ClO. 120. −. 2. NO. NO. 1 |
|
Diagrammes potentiel-pH
2 mai 2018 En pointillés sont représentées les droites frontières relatives aux couples redox de l'eau. ... Outre le couple ClO–/Cl– |
|
Exercices sur le chapitre 2
14 sept. 2021 ... l'eau elle-même. On peut modéliser cette transformation à partir des deux couples oxydant -réducteur suivants : CℓO− /Cℓ− et O2/H2O. Cette ... |
|
6065-oxydoreduction.pdf
Les ions cuivre (II) ( Cu2+ ) et le métal fer (Fe) constitue un couple oxydant/réducteur. Dans une réaction d'oxydoréduction l'espèce chimique oxydante est |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
ClO. Cl (ion hypochlorite / ion chlorure) : Étape 1 : Écrire la demi-équation du couple en milieu acide. 2. (aq). (aq). |
|
BREVET DE TECHNICIEN SUPÉRIEUR TRAITEMENTS DES
C'est un oxydant puissant formant |
|
Step 4: (Balance O) ClO- ? Cl
Step 1: Chlorine Cl+ Cl-. Step 2: ClO- ? Cl-. Step 3: ClO- ? Cl-. Step 4: (Balance O) ClO- ? Cl- Redox Reaction Zn(s) + Fe2+(aq) ? Zn2+(aq) + Fe(s). |
|
Hypochlorites et eaux de Javel
Justifier le rôle oxydant de l'ion hypochlorite. On commence par établir les demi-équations rédox : C?O-(aq) / C?-(aq) : C?O- + … |
|
V- EXERCICES :
Quels sont les couples redox présents dans l'extrait de la met en jeu les deux couples donnés ci-dessous. ClO-. (aq) / Cl2(g) et Cl2(g) / Cl-. |
|
FALA Tuto
14 avr. 2020 C) Pour le couple O2/H2O2 2 électrons sont échangés. D) Pour le couple ClO-/Cl- |
|
Oxydant Réducteur E0 (Volt)
Hg(l)+ H2O. 0.93. 2Hg2+. (aq) +2 e-. Hg2. 2+. 0.91. NO2(g) +8H++7 e-. NH4. ++ H2O. 0.90. NO2. -+8 H++6 e-. NH4. ++2 H2O. 0.90. ClO-+2 H++2 e-. Cl-+ H2O. |
|
TP 10 : Dosage des ions hypochlorites dune eau de Javel
en excès. La réaction a lieu en milieu basique car l'eau de Javel est basique et implique les couples d'oxydoréduction ClO-/Cl- et IO. |
|
Chimie PCSI
L'anion hypochlorite est un oxydant puissant qui intervient dans le couple ClO-/Cl-. L'eau de Javel est commercialisée sous plusieurs niveaux de dilution. Elle |
|
Untitled
L'eau de Javel est un mélange équimolaire de chlorure de sodium (Na+(aq) + Cl–(aq)) Couples rédox : ClO–(aq)/Cl–(aq) I2(aq)/I–(aq) |
|
1121: Redox Couples - Chemistry LibreTexts
The two species comprising half-reactions (e g Znº & Zn2+) are referred to as a “couple” Redox half-reactions Redox reactions are written as half-reactions which are in the form of reductions (which means an element is transformed from a higher oxidation state (e g +II) to a lower oxidation state (e g +I)): Ox + ne-= Red; |
|
Balancing REDOX Reactions: Learn and Practice
Apr 17 2013 · Balancing REDOX Reactions: Learn and Practice Reduction-Oxidation reactions (or REDOX reactions) occur when the chemical species involved in the reactions gain and lose electrons Oxidation and reduction occur simultaneously in order to conserve charge We can “see” these changes if we assign oxidation numbers to the reactants and products |
|
ClO (aq) + Cr(OH)3(s) CrO42-(aq) + Cl (aq) Reduction
Step 1: Chlorine Cl+ Cl-Step 2: ClO-ÆCl-Step 3: ClO-ÆCl-Step 4: (Balance O) ClO-ÆCl-+ H 2O (Balance H) ClO-+ 2H 2OÆCl-+ H 2O + 2OH-Step 5: ClO-+ H 2O +2e-ÆCl-+ 2OH-Oxidation Step 1: Chromate Cr3+ Cr6+ Step 2: Cr(OH) 3 ÆCrO 4 2-Step 3: Cr(OH) 3 ÆCrO 4 2-Step 4: (Balance O) Cr(OH) 3 + H 2OÆCrO 4 2-(Balance H) Cr(OH) 3 + H 2O + 5OH-ÆCrO 4 |
|
Searches related to couple redox clo /cl PDF
-2- CH 141 Lab: Redox An Example Analysis: The approach used in this experiment can be illustrated with a parallel example using perchlorate ion ClO4- as the oxidizing agent In the titration of Fe2+ with ClO4- the two possible chlorine- containing products are Cl2 and Cl- |
What are redox couples arranged in order of reducing strength?
TABLE 11.21. 1: Selected Redox Couples Arranged in Order of Decreasing Strength of Oxidizing Agent. An oxidizing and reducing agent which appear on opposite sides of a half-equation constitute a redox couple. Redox couples are analogous to conjugate acid-base pairs and behave in much the same way.
Which is an example of disproportionation redox reaction?
Therefore, this may be called as displacement redox reaction. The reaction (d) involves disproportionation of NO 2 (+4 state) into NO 2 –(+3 state) and NO 3 (+5 state). Therefore reaction (d) is an example of disproportionation redox reaction.
Why does the concentration of MnO 4 – decrease in redox couples?
The concentration of MnO 4– decreases because of the reaction This page titled 11.21: Redox Couples is shared under a CC BY-NC-SA 4.0 license and was authored, remixed, and/or curated by Ed Vitz, John W. Moore, Justin Shorb, Xavier Prat-Resina, Tim Wendorff, & Adam Hahn.
What is a reduction-oxidation reaction?
Reduction-Oxidation reactions (or REDOX reactions) occur when the chemical species involved in the reactions gain and lose electrons. Oxidation and reduction occur simultaneously in order to conserve charge. We can “see” these changes if we assign oxidation numbers to the reactants and products.
| Reversible Chlorite/Chlorine Dioxide Anion Redox Couple for |
| Classification des couples RÉDOX &# Potentiels normaux d |
| Oxidation-Reduction (Redox) Reactions - University of Washington |
| Balancing REDOX Reactions: Learn and Practice |
| Redox equilibria in natural waters - Chem1 |
| Platinum as a Chlorine Dioxide/Chlorite Redox Electrode in |
| Searches related to couple redox clo /cl filetype:pdf |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
ClO Cl (ion hypochlorite / ion chlorure) : Étape 1 : Écrire la demi-équation du couple en milieu acide 2 (aq) (aq) (aq) (l) - + - - ClO + 2 H + 2 e = Cl + H O |
|
Classification des couples RÉDOX &# Potentiels - MSLP-Dijon
Classification des couples RÉDOX # Potentiels normaux d'oxydoréduction ClO − + 2 H3O + + e− ½ Cl2 + H2O + 1,63 MnO4 − + 8 H3O + + 5 e− |
|
Les réactions doxydoréduction - pontonniers-physique
2-/ S2O3 2- I2/I- Cl2/Cl- H+/H2 H2O2/H2O O2/H2O 3 Méthode : établir la demi-équation relative à un couple rédox - Equilibrer les éléments autre que O et |
|
I LEAU DE JAVEL (6,5 points)
On rappelle ci-dessous les demi-équations électroniques relatives aux couples oxydant/réducteur liés à l'eau de Javel : 2 ClO- + 4 H+ + 2 e- Cl2 + 2 H2O 2 Cl- |
|
Réactions doxydo-réduction
Comment déterminer si une réaction Redox est possible ? ClO Cl E V I I E V - - - = + = + 3) Disposer les couples par valeur décroissante de E o 2 0 89 |
|
I Ecrire les demi-équations doxydo-réduction avec lélément chlore
L'ion hypochlorite ClO − (aq) peut réagir en milieu acide avec les ions chlorure Cl − Quels sont les couples oxydant/réducteur mis en jeu ? 2 |
|
Oxydoreduction - Lycée Ismael Dauphin
Quels sont les couples redox présents dans l'extrait de la d'oxydoréduction met en jeu les deux couples donnés ci-dessous ClO- (aq) / Cl2(g) et Cl2(g) / Cl- |
|
Travail dirigé : Loxydo-réduction
O2 , OF2 , ClO - , KClO3 , Cl2O7 , CS2 , Mn(ClO4)3 , Na2S2O3 , CrI3 , IO3 9/ On considère les couples rédox ClO3 -/Cl- et ClO4 + 8 H+ → 4 Cl- + 16 H2O |
|
Solutions aqueuses 2 : réactions doxydo-réduction - UNF3S
Ils forment un couple d'oxydo-réduction Ox/Red dit couple redox ClO 4 – I 2) Nombre d'oxydation Le nombre d'oxydation (ou degré d'oxydation) d'un atome |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
réaction (pour un des couples il s'agit du réducteur, pour l'autre couple de l' oxydant) 2) Si on se trouve en milieu basique (et uniquement dans ce cas), ajouter |