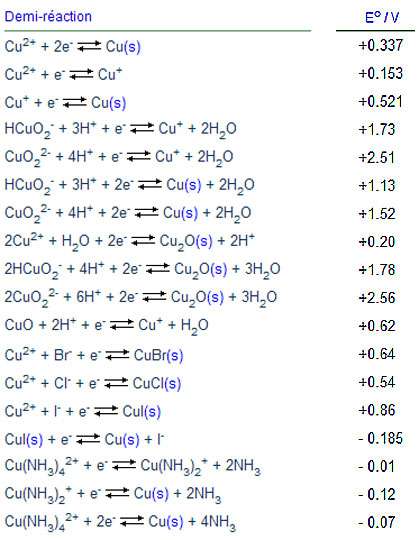demi equation redox sn2+/sn
|
1 équation-bilan dune oxydoréduction 2 Sens dune réaction rédox
c) On réalise la pile Cu Cu2+ Ag+ Ag et on trouve 046 V Quel est le potentiel rédox du couple Cu Cu2+ ? 6 Couple Sn2+/Sn a) Une solution de |
|
TD n°6 : équilibre doxydoréduction et électrochimie
Quels sont les couples redox mis en jeu ? - écrire les demi équations électroniques - Ecrire l'équation de la réaction Quelle est la masse du dépôt de |
Comment faire une demi-équation redox ?
Une demi-équation d'oxydoréduction est une équation chimique représentant la transformation de la forme oxydée d'un couple en sa forme réduite conjuguée sans qu'intervienne un second couple rédox.
Qu'est-ce qu'une demi-équation redox ?
L'ion zinc Zn^2+ et le zinc métallique constituent le couple rédox de demi-équation : Zn^2+ + 2e^− = Zn : a) Zn2+ est un oxydant car il peut gagner des électrons. b) Zn est un réducteur car il peut céder des électrons.
Quelle est la demi-équation électronique du couple Zn2 +/ Zn ?
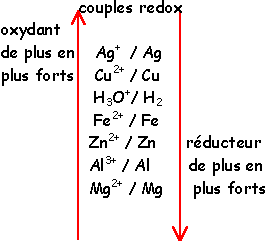
Un oxydant et un réducteur forment un couple redox si on peut passer de l'un à l'autre par gain ou perte d'électrons.
Par convention, un tel couple est noté Ox / Red.
L'ion Cu2+ et l'atome de cuivre Cu forment un couple redox noté : Cu2+ / Cu.
|
Etude quantitative de lévolution dun système Constante déquilibre
En déduire le potentiel rédox des couples en solution. V150). Sn/. Sn(E Les demi-équations électroniques et les formules de Nernst des deux couples ... |
|
Diagrammes potentiel-pH
2 mai 2018 Les espèces prises en compte sont Sn(s). SnO2(s) |
|
V- EXERCICES :
Ecrire l'équation bilan de la réaction chimique traduisant le dépôt métallique. Exercice 4 : Ecrire les demi-équations d'oxydoréduction relatives aux |
|
Oxydant Réducteur E0 (Volt)
Sn(s). 0.05. HOCN+2H++2 e-. HCN(aq)+ H2O. 0.02. NO3. -+ H2O +2 e-. NO2. -+2OH-. 0.01. 2 H++2 e-. H2(g). 0.00. HOCN+2 H++2 e-. HCN(g)+ H2O. -0.02. Fe3++3 e-. |
|
Faculté de médecine 2011/
Quels sont les couples redox mis en jeu ? - écrire les demi équations électroniques. - Ecrire l'équation de la réaction. Quelle est la masse du dépôt de cuivre |
|
Correction exercice n°2
2) Demi-équations : SnO2(s) + 4 H+ b) D'après l'équation bilan : n (Sn2+) = n (Pb2+) = 19 × 10-3 mol. Partie 2 : ... on en déduit : n (Sn. |
|
Les réactions doxydo-réduction
3/ Les demi-équations électroniques. ? Chaque couple oxydant-réducteur représente un transfert d'électron(s) réalisable dans les 2 sens. |
|
Etude cinétique d’une réaction d’oxydoréduction
des ions Sn. 2+ à la concentration 10-2 mol.L-1 le temps de demi-réaction T est de 2 |
|
Les piles et loxydo-réduction :
1 - Quel type d'électrodes (ou demi-piles) sont en présence ? Donner l'expression du La demi-pile (B) est du type redox |
|
Oxydoréduction – corrigé des exercices Table des matières
Comment équilibrer les équations des réactions rédox Sn + HNO3 ... Pb(NO3)2 1 mol·L-1 et la deuxième demi-pile avec une solution aqueuse de nitrate. |
|
Oxidation- Reduction Chemistry - WRUV
1 Write Skeleton Half-Reactions Oxidation SO32-? SO 4 2-Reduction MnO4-? Mn2+ 2 Mass Balance SO3 2-+ H 2O? SO42-+ 2H+ MnO4-+ 8H+ ? Mn2+ + 4H 2O •Add H2O to side needing oxygen •Add H+ to balance hydrogen 6 Example: Continued 3 Charge Balance (use electrons) SO3 2-+ H 2O ? SO42-+ 2H+ + 2e-MnO4-+ 8H+ + 5e-? Mn2+ + 4H 2O 4 |
|
Example Exercise 171 Calculating Oxidation Numbers for Carbon
A redox reaction occurs when the tin(II) ion reacts with the iodate ion as follows: Indicate each of the following for the preceding redox reaction: (a) substance oxidized (b) substance reduced (c) oxidizing agent (d) reducing agent Answers: (a) Sn2+; (b) IO 3 –; (c) IO 3 –; (d) Sn 2+ Practice Exercise |
|
Searches related to demi equation redox sn2+/sn PDF
In our reaction the product formed from Fe2+(aq) is Fe3+(aq) and possible products from the MnO4– ion are Mn2+(aq) Mn3+(aq) MnO2(s) or MnO42– The reaction product and the number of electrons gained by KMnO4 must be known before using the reagent in analytical determinations |
How do you balance a redox reaction?
Balance each redox reaction by writing appropriate half reactions and combining them to cancel the electrons. Pb (s) + Pb 4+ (aq) ? Pb 2+ (aq) (Hint: both half reactions will start with the same reactant.) 11.5: Half-Reactions is shared under a CC BY-NC-SA 4.0 license and was authored, remixed, and/or curated by LibreTexts.
How is cell potential calculated if a redox reaction is reversed?
Note that reversing the direction of a redox reaction effectively interchanges the identities of the cathode and anode half-reactions, and so the cell potential is calculated from electrode potentials in the reverse subtraction order than that for the forward reaction.
How redox potentials are used in a galvanic cell?
To use redox potentials to predict whether a reaction is spontaneous. To balance redox reactions using half-reactions. In a galvanic cell, current is produced when electrons flow externally through the circuit from the anode to the cathode because of a difference in potential energy between the two electrodes in the electrochemical cell.
Why does a balanced redox reaction have two electrons on each side?
Because we have two electrons on each side of the equation, they can be canceled. This is the key criterion for a balanced redox reaction: the electrons have to cancel exactly. If we check the charge on both sides of the equation, we see they are the same—2+.
| Redox Reaction - the basics - California State University |
| Review: Balancing Redox Reactions |
| Academic Resource Center - Illinois Institute of Technology |
| OXIDATION/REDUCTION REACTIONS - Federal University of Juiz de |
| SN1 and SN2 Reactions - Illinois Institute of Technology |
| Chapter 20 Worksheet Redox - Beverly Hills High School |
| Searches related to demi equation redox sn2+/sn filetype:pdf |
|
Correction exercice n°2 - physique chimie terminale S
2) Demi-équations : SnO2(s) + 4 H+ b) D'après l'équation bilan : n (Sn2+) = n ( Pb2+) = 1,9 × 10-3 mol Partie 2 : 1) Pb2+ (aq) + 3 Sn 2+ (aq) + 2 H + |
|
RAPPELS SUR LOXYDOREDUCTION - Correction - Bougaud
16 sept 2013 · Ecrire la demi-équation d'oxydoréduction correspondante : Hg2+ (aq) + 2 e – = Hg(l) 2) Retrouver trois couples oxydant/réducteur parmi les |
|
Chapitre 3 :Oxydoréduction
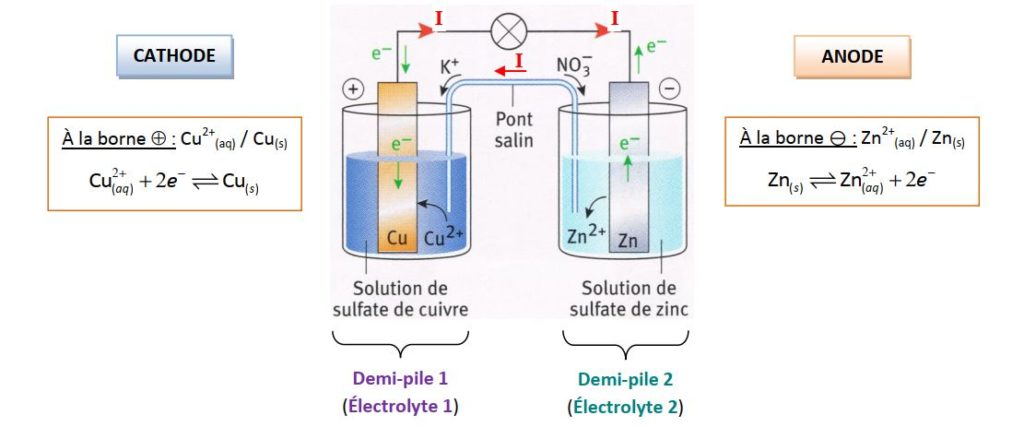
correspond à la demi équation redox Dans une cellule ou demi pile : e2 Zn Zn 2 ) • Pont salin : Le courant I circule de la solution de Zn2+ vers celle de |
|
CHIMIE DS 4 PSI 2014-15
+ 3 H+ + 2 e− = Sn(s) + 2 H2O E°3 = 0,33 V SnO2(s), Sn2+, Sn(s), SnO3 2) Comment s'écrit la demi-‐équation redox correspondant au couple H+ |
|
Classification des couples RÉDOX &# Potentiels - MSLP-Dijon
H2 + 2 H2O 0,00 CH3CO2H + 2 e− CH3CHO − 0,12 Pb2+ + 2 e− Pb − 0, 13 Sn2+ + 2 e− Sn − 0,14 Ni2+ + 2 e− Ni − 0,23 Fe2+ + 2 e− Fe − 0,44 |
|
Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir
La réaction associée au couple est appelée ½ équation redox Exemple : pour On écrit les 2 demi-équations redox des 2 couples mis en jeu : ✓ On assure la |
|
Semestre 2 – Chapitre 5 : Loxydoréduction Loxydoréduction, qui s
2- Ecrire la demi-équation électronique correspondant à la demi-pile (2) contenant le dioxygène et en déduire l'expression du potentiel de Nernst E2 |
|
1 équation-bilan dune oxydoréduction 2 Sens dune réaction rédox
Quels sont les couples rédox qui sont mis en jeu a) Ecrivez la demi-réaction de réduction de l'ion permanganate b) Quel métallique oxydant l'étain Sn 7 |
|
Exercices sur les piles et loxydore duction Exercices sur les piles et
Corrigé de l'exercice 1 : 1 Demi-équations : Couple H+/H2 : 2H+ + 2 e- = H2 Couple Sn2+/Sn : Sn = Sn2+ + 2 e- Equation d'oxydoréduction : Sn + 2H+ → H2 + |