etalonnage d 'une solution de soude par mise en solution d 'acide
|
ETALONNAGE D’UNE SOLUTION DE SOUDE PAR MISE EN
I ETALONNAGE DE LA SOLUTION DE SOUDE 1 Préparation de la solution d’acide oxalique L’acide oxalique est un solide blanc : H2C2O4 2H2O H2C2O4 C2O4 2- + 2 H+ On désire étalonner une solution de soude (NaOH) à environ 01 mol L-1 à l’aide de l’acide oxalique (chute de burette désirée : environ 20 mL) |
|
Etalonnage de la soude par de l’acide oxalique
Préparation de la solution de soude Pour une solution de soude proche de 01 mol/L (réadapter le protocole si on veut une solution de concentration diférente ne pas oublier de réajuster la concentration en acide oxalique) peser 1 g d’hydroxyde de sodium et dissoudre dans 250 mL d’eau |
|
Travaux Pratiques de Chimie Générale Acidimétrie
Dosage volumétrique d’une solution d’acide sulfurique H2SO4 par une solution titrée de soude NaOH 1 – L’objectif: L'étalonnage d'une solution d’acide sulfurique par une solution de soude Détermination de titre (normalité moralité et concentration massique) d’une solution d’acide sulfurique (H2SO4) |
Comment corriger l’acidité du sol ?
Corriger l’acidité du sol, ou son pH, avant les semis. Épandre de la chaux sur un sol trop acide pour en élever le pH. Des consultants privés et des fournisseurs de produits agricoles sont en mesure de donner aux éventuels producteurs une interprétation de l’analyse de sol et des conseils sur les mesures de correction à prendre.
Comment déterminer la concentration d'une solution de soude ?
Je ne comprends pas l'intitulé de cette question : La concentration d'une solution de soude sera déterminée par pesée et mise en solution d'un acide cristallisé et dosage de cette solution acide en présence de phénolphtaléine. Le même protocole expérimental sera suivi pour déterminer la masse molaire d'un acide cristallisé.
Comment étalonner une solution de soude ?
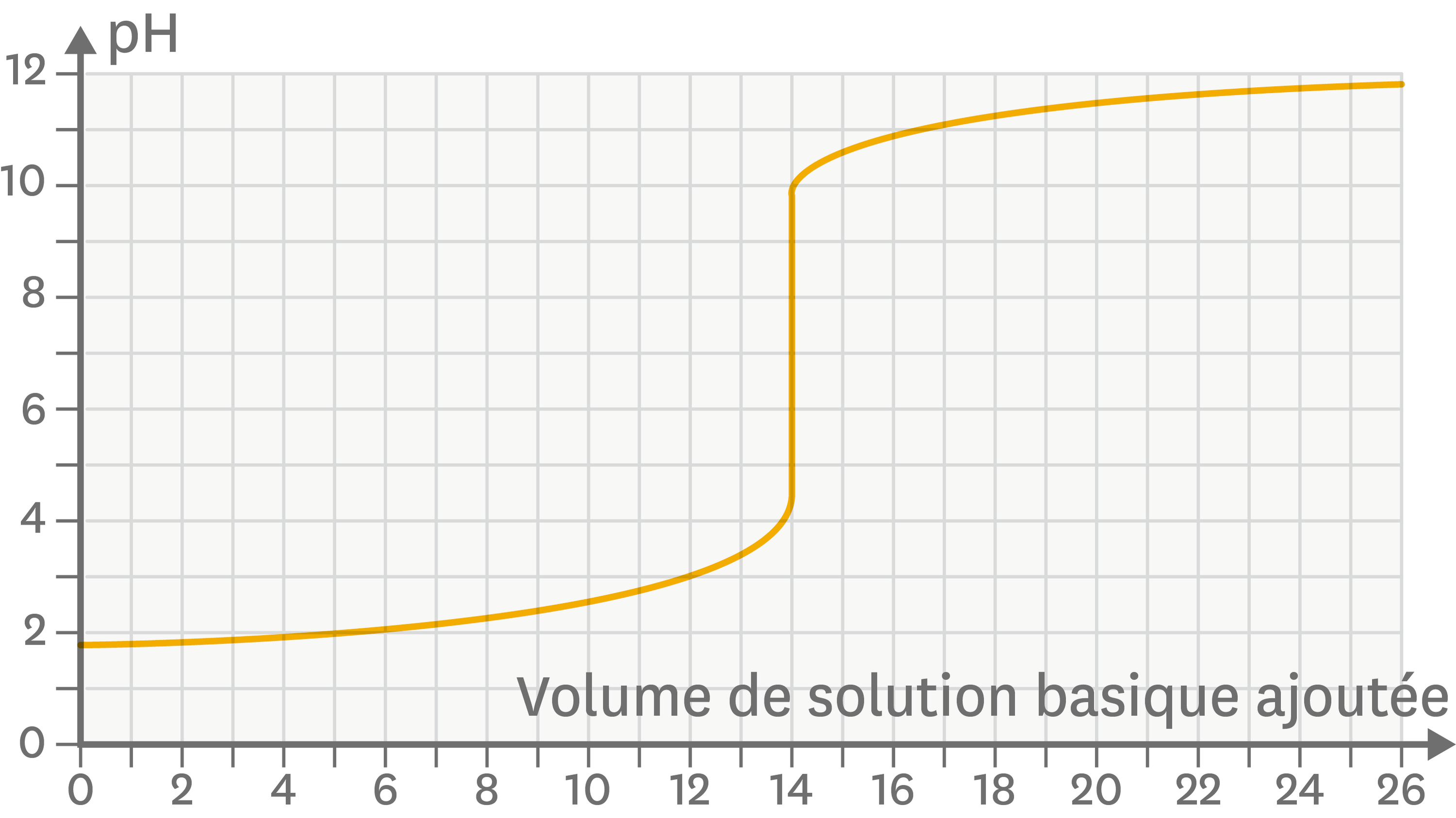
On désire étalonner une solution de soude (NaOH) à environ 0,1 mol.L-1à l’aide de l’acide oxalique (chute de burette désirée : environ 20 mL). - Répondre aux questions 1) et 2) du compte-rendu. - Peser précisément une masse m voisine de ………………………… d’acide oxalique.
Est-ce que la solution est acide ?
1)a) Cette solution contient NaCl, quand NaCl est dissous dans de l’eau, on obtient de l’eau salée, ce qui n’est pas basique, la solution est donc acide. b) Ce fait expérimental est justifié pas la présence de CO2 (dioxyde de carbone) dans les produits de la solution. Na2CO3 + 2 ( H3O+/Cl-) ======> 2 NaCl + CO2 + 3 H2O .
|
ETALONNAGE DUNE SOLUTION DE SOUDE PAR MISE EN
- Vérifier que l'acide oxalique est complètement dissout. 2. Etalonnage (2 essais). - Remplir la burette de solution de soude. - Ajouter 3- |
|
Étalonnage dune solution dhydroxyde de sodium par pesée d
Dosage par pHmétrie d'une solution d'acide phosphorique solution titrante est de la soude à environ 0100 mol/L. On se propose de l'étalonner par pesée. |
|
Etalonnage dune solution de soude Détermination du produit de
La concentration de solution d'hydroxyde de sodium (ou soude) doit être connue précisément avant d'être utilisée pour titrer la solution acide. Déterminer la |
|
POLYCOPIÉ DE TRAVAUX PRATIQUES CHIMIE 3
Tp n° 02 : Étalonnage d'une solution acide (HCl) par une solution de carbonate de Verser la soude (CB = 0.1 mol/L) mise au préalable dans la burette. |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Le volume de solution d'hydroxyde de sodium ajouté permettrait de faire réagir une masse d'acide tartrique qui correspond à l'acidité totale du vin. Page 7 |
|
Systèmes de titrage et déchantillonnage automatiques
et de mise en oeuvre la rapidité d'analyse |
|
Problème 1 : Titrage dune solution dacide oxalique
28.04.2016 -?/ Mn2+ et CO2(g)/H2C2O4. 1) Ecrire la réaction qui sera notée (R1) |
|
Untitled
Les valeurs de pH d'une solution aqueuse s'inscrivent dans l'échelle des mol/l soit pour une plage de pH = 0 à pH = 14. Acide chlorhydrique. Eau. Soude. |
|
Rapport Achevement (Algeria)
- Dans un tube a reaction mettre 10 ml solution de dichromate de potassium. - Ajouter |
|
Travail dirigé 5 : La concentration dune solution
Calculer la concentration molaire d'une solution d'acide chlorhydrique HCl sachant que sur l'étiquette on trouve les renseignements suivants : 37% massique |
|
E 1 FICHE GENERALE - AC Nancy Metz
EQUATION MISE EN JEU : x S + y R z P Pour déterminer la concentration de la solution à doser cS, on connaît : - le volume de de volume VS puis on réalise l' étalonnage sur une prise d'essai E de cette solution ETALONNAGE DE LA SOUDE PAR L'hydroxyde de sodium libéré réagit avec l'acide chlorhydrique |
|
Problème 1 : Titrage dune solution dacide oxalique - Chimie en PCSI
28 avr 2016 · Le permanganate de potassium libère en solution des ions potassium 1) Ecrire la réaction, qui sera notée (R1), entre l'acide oxalique et les ions permanganate concentration molaire C1 est titré par une solution de soude {Na+ 16) Ecrire l 'équation de réaction mise en jeu lors de ce titrage et calculer |
|
Chimie, 12e année - Document de mise en œuvre - Regroupement
solution d'AgNO3(aq) renfermant des ions Ag+ and NO3 pâle, l'indicateur rouge Congo, du bicarbonate de soude et de l'acide acétique ou chlorhydrique Parmi les sources d'erreur possibles, mentionnons l'étalonnage de la micropipette |
|
CHIM105B – DS1 Dosages acido-basiques : lacide oxalique
solutions d'acide oxalique, ca, et de soude, cb, sont toutes deux égales à 0,1 mol L-1 Sur la figure 2, le diagramme de distribution des espèces de l'acide |
|
Lacide lactique
solution d'hydroxyde de sodium de concentration 5 10-2 mol L-1 - hydrogénophtalate de I) Etalonnage de la solution titrante On dispose d'une b) Calculer très précisément la concentration molaire CB de la solution de soude acide lactique contenu dans un lait en utilisant le matériel et les produits mis à disposition |
|
Chaire de chimie générale et pharmaceutique TRAVAUX
plan pour sa mise en œuvre, de préparer à l'avance dans le journal de travail les contamination acide avec une solution de bicarbonate de soude à 2 et en |
|
Corrigé 2005 (pdf) - Académie de Rouen
Lors de la réaction de précipitation, la solution de chlorure de calcium devient- elle : Plus acide ? plus basique L'analyse commence par la mise en solution du ciment en milieu acide, seule la silice Dosage par étalonnage Dosage d' hélianthine à 10,0 mL de la solution S1 et on ajoute une solution de soude jusqu' au |
|
Etude du dosage des acides lactique, malique et tartrique par
On refroidit et on titre l'excès de soude normale awc une solution normale de H, SO, en présence de phénolphtaléine ) On obtient ajnsi l'acide lactique total |
|
Formules de pH des solutions diluées - Proximus
pKa = - seront supérieures à 99 En d'autres termes, les acides forts sont considérés comme totalement dissociés en solution aqueuse Critère Un acide est |