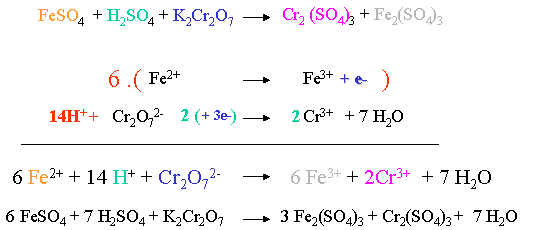oxydoréduction en milieu basique
|
Chapitre 2 : Réactions doxydoréduction
Il s'agit de la méthode à employer lorsque la réaction a lieu en milieu acide Lorsqu'elle a lieu en milieu basique il faut équilibrer cette fois ci avec des |
Comment équilibrer une équation en milieu basique ?
2.
4) Equilibre d'oxydoreduction en milieu basique
Lorsqu'elle a lieu en milieu basique, il faut équilibrer cette fois ci avec des ions hydroxyde HO– à la place des ions H+.
Pour ce faire, le plus simple est de commencer par équilibrer en milieu acide, puis de passer en milieu basique grâce au fait que : H+ + HO– H2O.Comment reconnaître un milieu basique ?
La valeur du pH de la solution est supérieure à 7.
Le produit ménager est donc basique.C'est quoi un milieu basique ?
Un milieu basique est un milieu riche en bases. désigne la constante de dissociation de l'eau).
- 1: Écrire l'oxydant et le réducteur de part et d'autre d'une double-flèche. 2: Équilibrer les atomes autres que l'oxygène et l'hydrogène . 3: Équilibrer les atomes d'oxygène en ajoutant autant de molécules de H2O dans l'autre côté. 4: Équilibrer les atomes d'hydrogène en ajoutant autant des ions H+ de l'autre côté.
|
Chapitre 2 : Réactions doxydoréduction
2.3 Réaction d'oxydoréduction . Equilibre d'oxydoreduction en milieu basique. 25 des couples. Il faut alors ... |
|
Chapitre 4 Oxydo-réduction
Tous les couples oxydant / réducteur ne peuvent cependant pas exister dans un tel milieu… Certains couples n'évoluent en effet |
|
Chapitre 4 Oxydo-réduction
Tous les couples oxydant / réducteur ne peuvent cependant pas exister dans un tel milieu… Certains couples n'évoluent en effet |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
Pour écrire la demi-équation d'un couple oxydant-réducteur en milieu basique il faut : ➢ Écrire la demi –équation du couple en milieu acide donc avec des |
|
Equilibrer une réaction doxydo-réduction
On écrit toujours un couple redox sous la forme Oxydant/Réducteur. Soit (Ox/Red) mais la réaction se faisant en milieu basique on ajoute le nombre d'ions ... |
|
34 - Réactions redox en milieu basique
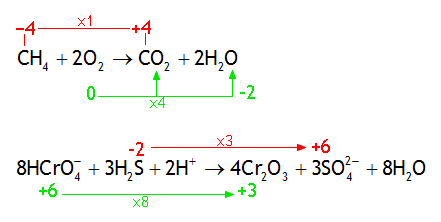
ÉQUATIONS DE RÉACTIONS D'OXYDORÉDUCTION EN SOLUTION AQUEUSE BASIQUE. Les nombres d'oxydation des atomes qui en changent sont indiqués à côté de chaque espèce |
|
تفــاعـلات الأكســدة-اختــزال
Méthode d'équilibre d'une demi équation redox en milieu basique : - Equilibrer la demi-équation en milieu acide. - Ecrire l'autoprotolyse de l'eau avec |
|
La chimie
• une réaction d'oxydoréduction implique le transfert d'électrons d'une substance à • lorsque la réaction se produit dans un milieu basique étape (4) est. |
|
Corrigé DS no 1 : Quantité de matière - Oxydoréduction
7 nov. 2020 chimique - Oxydoréduction. 1ère spécialité Physique-Chimie - LMA ... Exercice 3 - Oxydo-réduction en milieu basique (6 points). En milieu ... |
|
Les réactions doxydoréduction
(8) En milieu basique : NH3 + OCl- = Cl2 + N2H4. NH3. N2H4 couple. OCl-. Cl2 couple no(H) = -3 no(Mn) = -2. N2H4/ NH3 no(Cl) = +1 no(Cl) = 0. OCl-/ Cl2. N2H4/ |
|
Chapitre 2 : Réactions doxydoréduction
2.4 Equilibre d'oxydoreduction en milieu basique . Les réactions d'oxydoréduction sont des réactions chimiques au cours desquelles il y a un échange d' ... |
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
demi-équation d'un couple oxydant-réducteur en milieu basique il faut : ? Écrire la demi –équation du couple en milieu acide donc avec des ions (aq). |
|
Chapitre 4 Oxydo-réduction
Tous les couples oxydant / réducteur ne peuvent cependant pas exister dans un tel milieu… Certains couples n'évoluent en effet |
|
Travail dirigé : Loxydo-réduction
Fe 3+ + Cr 3+ ( milieu acide) b/ MnO4. - + I - ? MnO2 + I2. ( milieu basique) c/ Cu + NO3. -. ? Cu 2+. + NO ( milieu acide). |
|
DS no 1 : Quantité de matière - Oxydoréduction - Lycée dAdultes
7 nov. 2020 Exercice 3 - Oxydo-réduction en milieu basique (6 points). En milieu basique les ions oxonium H. + ne sont pas présents |
|
Corrigé DS no 1 : Quantité de matière - Oxydoréduction
7 nov. 2020 chimique - Oxydoréduction. 1ère spécialité Physique-Chimie ... Exercice 3 - Oxydo-réduction en milieu basique (6 points). En milieu basique ... |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
2) Si on se trouve en milieu basique (et uniquement dans ce cas) ajouter de part et d'autre du signe = des ions hydroxyde HO- (qui sont présents dans la. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Potentiels d'oxydoréduction : Equation de Nernst Elecroneutralité : [BH+] = [OH-] milieu basique on néglige les ions H3O+ provenant de l'eau. |
|
Transformations chimiques en solution aqueuse
Dans une réaction d'oxydoréduction un élément chimique perd (oxydation) ou gagne en milieu basique : forme basique de l'eau : ion hydroxyde OH-. |
|
Etude des risques doxydation de la pyrite dans le milieu basique du
L'habitus des sulfures est aussi un paramètre intéressant à suivre. Les pyrites framboïdales se distinguent de ce que l'on nomme habi-. |
|
Chapitre 2 : Réactions doxydoréduction - Lycée dAdultes
Pour ce faire le plus simple est de commencer par équilibrer en milieu acide puis de passer en milieu basique grâce au fait que : H+ + HO– H2O Exemple : On |
|
Demi-equation-OxRed-basiquepdf
Pour écrire la demi-équation d'un couple oxydant-réducteur en milieu basique il faut : ? Écrire la demi –équation du couple en milieu acide donc avec des |
|
Chapitre 4 Oxydo-réduction
Les réactions d'oxydoréduction en milieu acide ou basique Exemple de réaction se déroulant en milieu acide : Le peroxyde d'hydrogène H2O2(aq) réagit avec |
|
Les réactions doxydo-réduction - Physique - Chimie
Déterminez l'équation d'oxydoréduction qui a lieu dans une solution contenant les ions fer II Fe2+ et les ions permanganate MnO4 - en milieu acide |
|
Les réactions doxydo-réduction - AlloSchool
Méthode d'équilibre d'une demi équation redox en milieu basique : - Equilibrer la demi-équation en milieu acide - Ecrire l'autoprotolyse de l'eau avec |
|
Oxydoréduction - AlloSchool
Afin d'équilibrer la réaction en milieu basique deux ions HO–sont ajoutés aux réactifs et aux produits ; deux ions H+ associés à deux ions HO– forment deux |
|
Oxydo-réduction en solution aqueuse
Une réaction d'oxydoréduction est une réaction d'échange électronique entre l'oxydant d'un couple et le réducteur d'un deuxième couple |
|
Oxydoréduction - cpge paradise
On donne ici les équations équilibrées en milieu acide Les équations en milieu basique s'obtiennent en rajoutant 1 OH– dans chaque membre de l'équation par |
|
Les réactions doxydoréduction et lélectrochimie
en milieu acide D'après les états d'oxydation le Cu est oxydé et le N est réduit • étape (1): écrire l'équation non-équilibrée de la réaction sous forme |
|
Loxydo-réduction
est stabilisé en milieu basique mais une V - Les facteurs influant sur le potentiel d'oxydo- réduction 1 Le pH Par exemple en milieu acide: |
Comment équilibrer une réaction d'oxydoréduction en milieu basique ?
2.4 Equilibre d'oxydoreduction en milieu basique
Lorsqu'elle a lieu en milieu basique, il faut équilibrer cette fois ci avec des ions hydroxyde HO– à la place des ions H+. Pour ce faire, le plus simple est de commencer par équilibrer en milieu acide, puis de passer en milieu basique gr? au fait que : H+ + HO– H2O.Comment équilibrer une équation en milieu basique ?
Pour ajuster les demi-équations en milieu basique (ions hydroxyde majoritaires par rapport aux ions hydrogène H+), on ajoute autant d'ions HO? de part et d'autre de l'équation qu'il y a d'ions H+.- Pour écrire une équation d'oxydo-réduction il faut donc commencer par écrire les deux demi équations puis de les combiner pour former l'équation complète en vérifiant que le nombre d'électrons perdus lors de l'oxydation corresponde au nombre d'électrons gagnés lors de la réduction.
| Chapitre 4 Oxydo-réduction - ac-montpellierfr |
| Chapitre 4 Oxydo-réduction |
| Oxydoréduction - Road To CNC |
| Les réactions d’oxydoréduction |
| Searches related to oxydoréduction en milieu basique filetype:pdf |
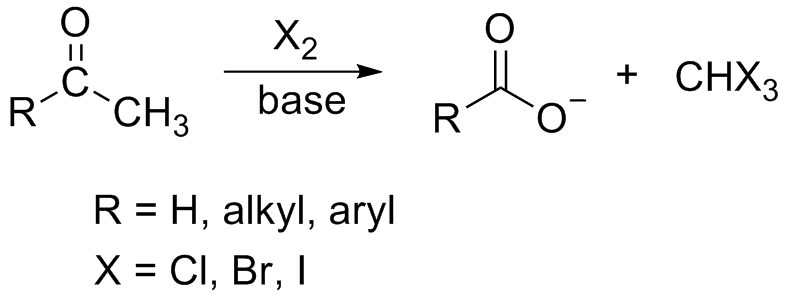
Comment réduire l’oxydation d’aldéhyde?
- R-CHO(aq) + 2 Ag+(aq) + 3 HO–(aq) ?R-COO–(aq) + 2 Ag(s) + 2 H 2 O(l) Lors de cette réaction, l’aldéhyde est de nouveau oxydé en ion aroxylate R-COO–(aq) et les ions argent (I) sont réduits.
Qu'est-ce que la réaction d'oxydoréduction?
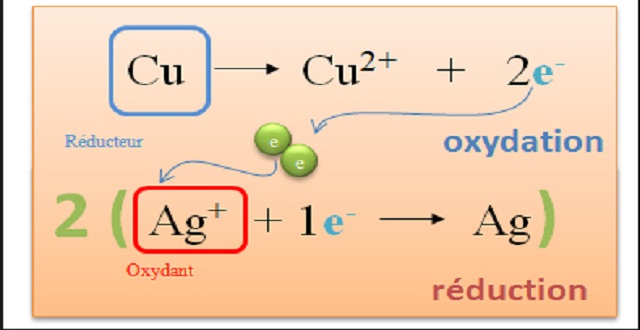
- Une réaction d’oxydoréduction est une réaction au cours de laquelle il y a échange d’électrons. entre le réducteur d’un couple et l’oxydant d’un second couple.
. Au cours de la réaction, le réducteur d’un des couples mis en jeu perd des électrons, alors que l’oxydant de l’autre couple gagne des électrons.
Qu'est-ce que la réaction d'oxydoréduction ?
- Une réaction d’oxydoréduction est une réaction d’échange électronique entre le donneur d’un couple et l’accepteur d’un autre couple.
. Ce transfert électronique peut être décomposé en deux demi-équations ne faisant intervenir qu’un seul couple à chaque fois.
. Traditionnel- lement une réaction d’oxydoréduction prend la forme : a Ox 1+ b Red 2= a Red
Quels sont les différents types d’oxydoréduction ?
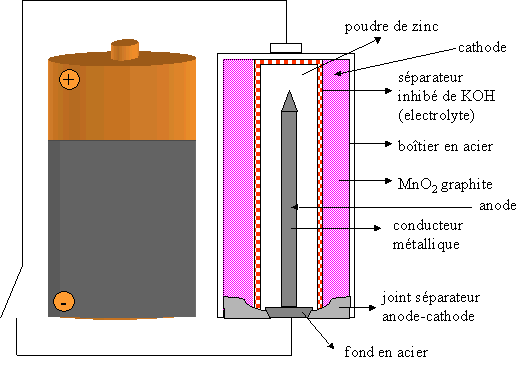
- Oxydoréduction Dr.
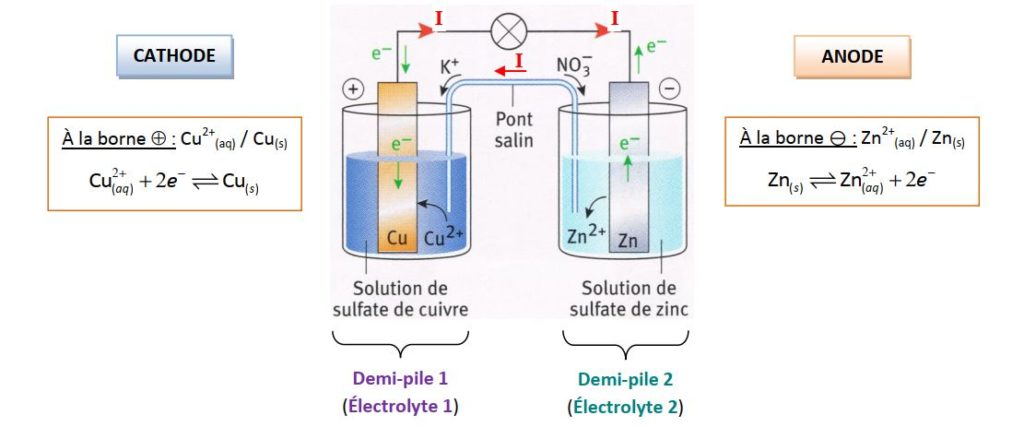
. Ouksel 5 - Lame d’argent plongeant dans une solution contenant des ions Ag+. - Lame de cuivre plongeant dans une solution contenant des ions Cu2+. - Lame de zinc plongeant dans 2+une solution contenant des ions Zn . - Fil de platine 2+plongeant dans une solution contenant des ions Fe3+et Fe .
|
MÉTHODE POUR ÉQUILIBRER LA DEMI-ÉQUATION DUN
Pour écrire la demi-équation d'un couple oxydant-réducteur en milieu basique, il faut : ➢ Écrire la demi –équation du couple en milieu acide donc avec des ions |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
2) Si on se trouve en milieu basique (et uniquement dans ce cas), ajouter de part et d'autre du signe = des ions hydroxyde HO- (qui sont présents dans la |
|
Réactions doxydo-réduction
Jacques Collot - Oxydo- réduction – Page 1 de 29 Réactions d'oxydo- Milieux basiques Equilibrer la réaction : 2 3 Milieu basique Vérifier en utilisant les |
|
Les réactions doxydoréduction - pontonniers-physique
L'eau en tant qu'oxydant : couple H2O/H2 - en milieu neutre ou basique : couple H2O/H2 : 2 H2O + 2 e- = H2 + 2 OH- - en milieu acide : équivalent au couple H |
|
Oxydoréduction Oxydoréduction - Étienne Thibierge
2 mai 2018 · Identifier l'oxydant et le réducteur Écrire ensuite la demi-équation associée, en milieu acide et en milieu basique 4 - Justifier que CrO2– 4 |
|
Chapitre 4 Oxydo-réduction
Tous les couples oxydant / réducteur ne peuvent cependant pas exister dans un tel milieu Certains couples n'évoluent, en effet, qu'en milieu basique Exemple |
|
Réactions doxydoréduction - Lycée dAdultes
Equilibre d'oxydoreduction en milieu basique 25 des couples Il faut alors équilibrer successivement les deux demi équations électroniques des deux couples |
|
35 - Réactions redox en milieu basique - Chimie - PCSI
Chimie organique Exercice 35 Page 1 sur 2 Corrigé exercice 35 ÉQUATIONS DE RÉACTIONS D'OXYDORÉDUCTION EN SOLUTION AQUEUSE BASIQUE |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
Equation chimique en milieu acide : Equation chimique en milieu basique : On compense les ions H+ : Equation chimique : 4 Les couples d'oxydo-réduction de |