facteur de van't hoff formule
|
Freezing Point Depression: Determining CaCl2 Vant Hoff Factor I
In this case the ideal van't Hoff factor equals two. On the other hand calcium chloride |
|
Analyse de la pureté par DSC
paux facteurs d'influence. Validité de l'équation de Van't Hoff présentée par l'équation de Van't Hoff : ... l'impureté M2 |
|
Osmolarite.pdf
facteur de correction : toutes les molécules de soluté ne se La pression osmotique d'une solution est donnée par la loi de van't Hoff. |
|
NOTIONS FONDAMENTALES DE CHROMATOGRAPHIE
2.5 Facteur de sélectivité ou de séparation. 2.6 Courbe de Gauss Equation de van't Hoff: dlnK / dT = ?H° / RT2 permet de calculer l'effet de la ... |
|
Pr. Hindré
Jan 15 2021 Le coefficient d'ionisation de Van't Hoff est donné par la formule : i = 1 + ( – 1). Si = 0 alors la dissociation est nulle et le ... |
|
Reaction chimique - Thermodynamique - Cinétique
Ceci découle directement de la relation de Van't Hoff. Remarque : Les effets de la pression de l'ajout de constituants actifs ou inertes sur un système en |
|
Enthalpie libre évolution et équilibre
L'équilibre atteint toute modification d'un facteur de l'équilibre (pression |
|
Cinétique chimique
LOI DE VAN'T HOFF. 3.3. ORDRE INITIAL ET ORDRE COURANT. II – INFLUENCE DU FACTEUR CINETIQUE TEMPERATURE SUR LA VITESSE DE LA REACTION. 1. LOI D'ARRHENIUS. |
|
THERMOCHIMIE
d)Variation élémentaire d'enthalpie libre au cours de la réaction. Cette formule de VAN'T HOFF peut s'obtenir par exemple directement en partant de la. |
|
Cinétique chimique
LOI DE VAN'T HOFF. 9. 3.3. ORDRE INITIAL ET ORDRE COURANT. 10. II - ETUDE DE QUELQUES REACTIONS D'ORDRE SIMPLE : ETUDE DU FACTEUR CINETIQUE. CONCENTRATION. |
|
Enthalpie libre ; évolution et équilibre - Le Mans University
>Enthalpie libre ; évolution et équilibre - Le Mans University |
|
UE physiologie cellulaire et immunologie
>UE physiologie cellulaire et immunologieefisio online fr/ensenhament11/PCI/osmolarite pdf · Fichier PDF |
|
CINETIQUE CHIMIQUE SPÉ MP
>CINETIQUE CHIMIQUE SPÉ MPhttps://www chireux fr/mp/cours/Polys/cinetique_chimique pdf · Fichier PDF |
Comment calculer le facteur de van t Hoff ?
La quantité de particules réelles produites par le constituant, comprenant les particules non dissociées et les particules résultant de la dissociation, vaut : Le facteur de van 't Hoff correspond au ratio de la quantité de particules réelles issues du soluté à la quantité de soluté apparente : On note la fraction de soluté dissocié :
Qu'est-ce que le coefficient de t Hoff van ?
Le coefficient de « t Hoff van a été nommé d'après chimique néerlandais Jacobus Henricus van « t Hoff. Il a montré que, comme le La loi de Boyle de gaz idéal, il existe une relation de proportionnalité entre pression osmotique (?) concentration molaire (M) et température (T) d'un solution. Ce rapport est intitulé "équation van « t Hoff».
Qu'est-ce que la loi de van t Hoff ?
La loi de van 't Hoff — à ne pas confondre avec l'équation de van 't Hoff en thermodynamique — relie le mécanisme chimique à la cinétique d'une réaction : Pour une étape élémentaire, les ordres partiels sont égaux aux nombres stœchiométriques. Attention
|
Les solutions
d'ébullition du solvant pur – on peut utiliser la formule suivante : téb 5téb sln 2 t° éb) ; • i est le coefficient de Van't Hoff ; • m est la molalité de la solution en |
|
Programme de Physique - Concours Agro Veto
Il signalera l'influence du facteur exponentiel de Boltzmann, mais aucune autre notion quantitative formule n'est pas exigible Influence de la température sur K°, loi de Van't Hoff - Quotient de réaction Qr et calcul de sa valeur pour un état |
|
Equilibre chimique
23 oct 2009 · Quand un système à l'équilibre est soumis é divers facteurs influençant cet Quelle est la relation avec le principe de Le Châtelier et de Van't Hoff ? de déterminer la constante d'équilibre de la solution, d'après la formule : |
|
Théorie et pratique des mesures de la pression osmotique - Agritrop
à une série de formules qui en sont l'aboutissement et qui permettent d'envisager des applications Le coefficient de Van 'T Hoff, rapport du nombre total de |
|
THERMOCHIMIE
5)Évolution d'une même espèce chimique sous deux phases à P et T constants Cette formule de VAN'T HOFF peut s'obtenir par exemple directement en partant de la de moles de gaz est constant, la pression n'est pas facteur d' équilibre |
|
Les électrolytes
➢ʋ devrait être près de 2 pour NaCl en solution (pour une dissociation totale) Page 26 COEFFICIENT DE VAN'T HOFF - ÉQUATIONS ∆ |
|
EQUILIBRES CHIMIQUES CINETIQUE CHIMIE EN SOLUTION
chimiques qui conduisent directement à l'enthalpie libre à l'aide de la formule ci- dessus on obtient finalement (loi de Van't Hoff) : dlnK Le facteur 55,5 n'a |
|
Reaction chimique - Thermodynamique - Cinétique
Thermodynamique chimique 18/18 VI Variation de la constante d'équilibre et évolution de l'équilibre avec la température 1 Relation de Van't Hoff Compte |



















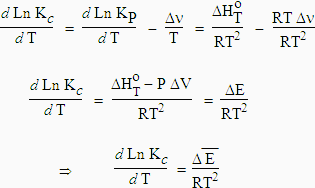

















![Chimie Des Solutions Mpsi - [PDF Document] Chimie Des Solutions Mpsi - [PDF Document]](https://demo.vdocuments.mx/img/378x509/reader024/reader/2021010212/548ed3d2b479590d2b8b4eac/r-1.jpg)
![Chimie Des Solutions Mpsi - [PDF Document] Chimie Des Solutions Mpsi - [PDF Document]](https://upload.wikimedia.org/wikipedia/commons/thumb/3/34/Mu%28solvant%29-f%28T%29.png/350px-Mu%28solvant%29-f%28T%29.png)