combien de moles d eau dans un litre
|
1 Matiere
molécules d'eau en déduire la masse d'une mole de molécules d'eau 2 Combien de molécules d'eau trouve-t-on dans ce litre ? 3 Sachant que 25 mol de |
|
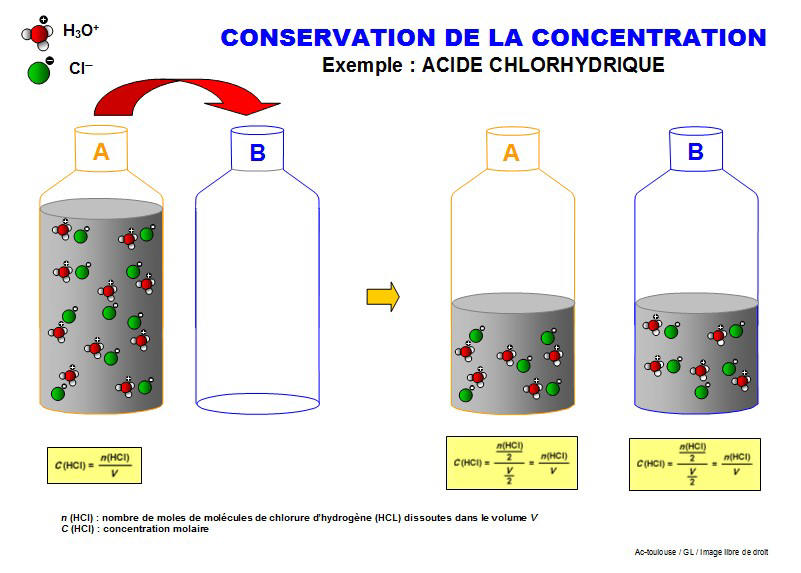
Mole – Masse molaire – Volume molaire
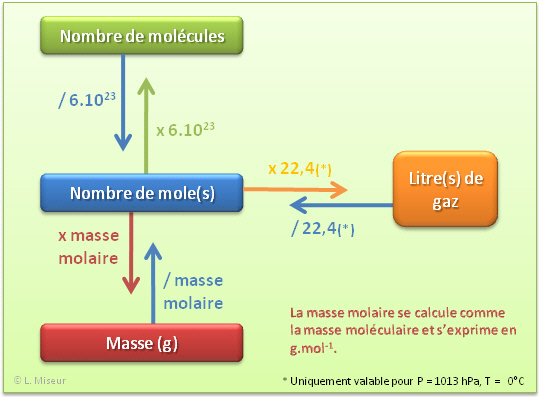
1 mole d'eau (c'est-à-dire environ 6 1023 molécules d'eau ce nombre est le nombre d'Avogadro noté N) pèse 18 g et occupe à l'état liquide un volume de |
Comment calculer les mol par litre ?
Unités.
Dans le Système international, la concentration molaire s'exprime en moles par mètre cube (mol/m3 ou mol⋅m−3), mais on utilise plus couramment les moles par litre (mol/l ou mol⋅l−1) : 1 mol/l = 1 000 mol/m.Comment calculer le nombre de moles de l'eau ?
1 mole d'eau (c'est-à-dire environ 6.1023 molécules d'eau, ce nombre est le nombre d'Avogadro, noté N) pèse 18 g, et occupe, à l'état liquide, un volume de 18cm3.
Dans un volune "V" (en cm3) d'eau, il y a donc V/18 * N molécules d'eau.Quelle est la masse d'une mol d'eau ?
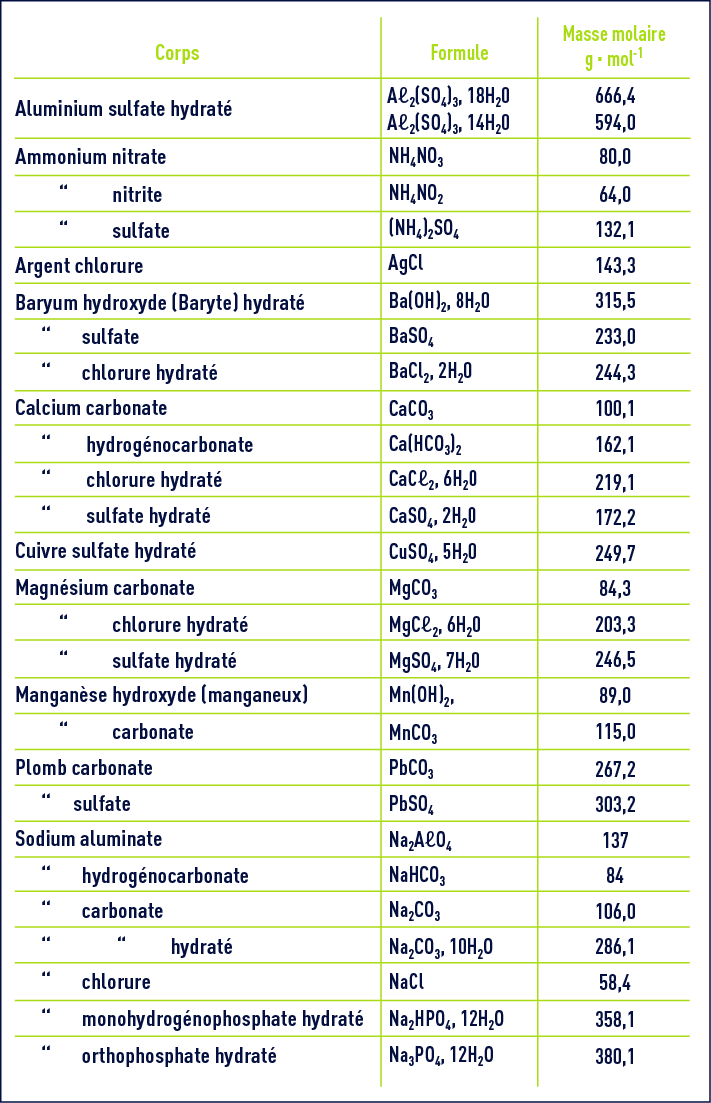
La masse molaire moléculaire est égale à la somme des masses molaires atomiques des éléments chimiques constituant la molécule.
L'unité est toujours le gramme par mole, notée g. mol–1.
Ainsi, la masse molaire de la molécule d'eau H2O est : M(H2O) = 2 x M(H) + M(O) = 2 x 1,00 + 16,0 = 18,0 g.- Tableau de conversion de la glycémie (mmol/L en g/L)
Afin de passer d'une unité de mesure de la glycémie à une autre, voici les facteurs de conversion : g/L x 5,5 = mmol/L. mmol/L x 0,18 = g/L.
|
Td corriges biochmv 2014-2015.pdf
EXERCICE 5: Effet tampon. a) On ajoute 10-3 mole de HCl (acide fort) dans un volume final de 1 L d'eau. Quelle est. |
|
1) Calculez le nombre dentités (N = nbr. de molécules atomes ou
Concentration molaire : combien y a-t-il de moles dans un litre c = n. V. Exercices a) Nous ajoutons 25 g de NaCl (sel de cuisine) dans 5 litres d'eau. |
|
Calculer une quantité de matière
C la concentration |
|
Chapitre 1 La quantité de matière la concentration molaire et le
L'unité est toujours le gramme par mole notée g.mol–1. Ainsi |
|
Chapitre 1 - LATOME ET LES ÉLÉMENTS
Réponse : La masse molaire de l'eau est de 1802 g/mol. b) Combien y a-t-il de moles d'eau (H. 2. O) |
|
Les solutions
naturelle l'eau est le solvant de base pour réaliser des réactions chimiques. L-1 nombre de moles d'ions monovalents équivalents dissous dans un litre ... |
|
Les équilibres- exercices supplémentaire avec correction -2017
si à l'équilibre les concentrations sont les suivantes : Si à t=0 |
|
N 602×1023
Ic l'atome d'aluminium contient 27 nucléons donc sa masse est de 451×10?26 kg . 1 Combien y a-t-il de molécules d'eau dans une goutte d'eau ? |
|
Travail dirigé 5 : La concentration dune solution
17. Calculer la concentration molaire de la solution obtenue en mélangeant 200 mL d'eau à 50. mL de NaOH 5 mol.L-1. Quel est le facteur de dilution ? |
|
Chapitre 1 La quantité de matière la concentration molaire et le
L'unité est toujours le gramme par mole notée g mol–1 Ainsi la masse molaire de la molécule d'eau H2O est : M(H2O) = 2 x M(H) + M(O) = 2 x 100 + 160 |
|
Calculer une quantité de matière
C la concentration s'exprime en moles par litre (mol L–1) ; la masse volumique de l'eau (1 kg L–1) Ainsi si la densité d'un liquide est égale |
|
IIILeau
Calculons la concentration molaire de l'eau (considérée comme soluté! ) Or dans un litre d'eau des 5536 moles « initialements présentes » 2 10 |
|
QUANTITÉ DE MATIÈRE
Une mole contient 602 1023 entités élémentaires (= atomes ions molécules ) Une mole d'atomes d'hydrogène contient 602 1023 atomes d'hydrogène |
|
La Mole et la Concentration Molaire Superprof
Avis 43 |
|
A) Donner la définition de la molarité dune solution b) Calculer la
Une solution qui contient une mole par litre est une solution molaire La molalité est la concentration exprimée en moles par kg d'eau Une solution qui |
|
Concentration molaire - Wikipédia
Par exemple une mole d'eau liquide à 25 °C occupe un volume de 0018 l donc la concentration (molaire) de l'eau dans l'eau pure vaut 556 mol/l |
|
Chimie quantitative – mole masse molaire volume molaire
L/mol Exercice 2 Quel est le nombre d'atomes de fer dans 28 g de fer ? Combien de molécules d'eau sont produites quand 12 molécules d'éthane |
Quel est le nombre de mol de l'eau ?
1 mole d'eau (c'est-à-dire environ 6.1023 molécules d'eau, ce nombre est le nombre d'Avogadro, noté N) pèse 18 g, et occupe, à l'état liquide, un volume de 18cm3. Dans un volune "V" (en cm3) d'eau, il y a donc V/18 * N molécules d'eau.Comment trouver des mol par litre ?
L'équation pour la concentration molaire est �� = �� �� , où �� est la quantité de matière du soluté en moles, �� est la concentration molaire exprimée typiquement en moles par litre et �� est le volume de la solution, typiquement exprimé en litres.Comment calculer la mole de l'eau ?
mol–1. Ainsi, la masse molaire de la molécule d'eau H2O est : M(H2O) = 2 x M(H) + M(O) = 2 x 1,00 + 16,0 = 18,0 g. mol–1.- Il suffit d'appliquer la relation n=m/M pour déterminer le nombre de mole.
Comment calculer des moles par litre ?
Comment calculer la mole de l'eau ?
. La masse d'une mole d'eau est donc la masse molaire de l'oxygène et 2 fois la masse molaire de l'hydrogène soit : M(H2O) = 2M(H) + M(O) soit M(H2O) = 2 × 1,0 + 16,0 = 18 g·mol-1.
Comment calculer le nombre de moles dans un liquide ?
Comment calculer le nombre de moles ?
. Ensuite, il est possible de déterminer le nombre de moles.
|
Quantités de matière et concentration molaire
utilisent les quantités de matière exprimée en mol et surtout pas en gramme ➢ Une mole est un Pour la molécule d'eau de formule H2O : M(H) = 1g mol-1 avec n en mole (mol ) , V en litre ( L ) et C en mole par litre ( mol L-1 ) Applications |
|
Chapitre 1 : Pourquoi et comment mesurer des - Physagreg
Pour connaître la composition d'une eau Le nombre d'Avogadro définie le nombre d'entité dans une mole : 6 023*10 23 mol -1 Sa concentration molaire est la quantité de matière de cette espèce dans un litre de solution On peut donc |
|
Molarité, molalité - e-fisio
moles de molécules par litre b) Calculer la molarité d'une solution aqueuse contenant 585 mg de NaCl par litre d'eau (Na : PM = 23 ; Cl : PM = 35,45) réponse |
|
Quelques rappels sur les calculs de quantités et de - e-fisio
unité : osmole litre-1 ; abréviation : osm L-1 osmolalité : concentration en particules solubles exprimée en nombre de moles de particules par masse de solvant ( |
|
Exercice 4 : Correction :
On calcule la quantité d'ions H3O+ contenus dans un litre d'eau Pour avoir le nombre de moles d'eau nH2 0 contenues dans une masse mH2 0 d'eau, |
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
On introduit 0,55g de sulfate de zinc (ZnSO4) et on ajoute de l'eau jusqu'au Une solution dont 5 mL contiennent nA mol d'une substance dissoute A est 10 suivantes : verser le contenu du berlingot dans une bouteille d'un litre et de compléter 2/ Variation du nombre de moles de soluté et de la concentration en soluté |
|
CONCENTRATION MOLAIRE ET SOLUTIONS AQUEUSES ⇒ ⇒
La concentration molaire est la quantité de matière de soluté dans un litre de solution On a donc : C = 8,00 10 -2 mol L -1 L'ammoniac dans l'eau 1 Quantité |
|
Convertir les données suivantes dans lunité demandée
b) V2 = 2,0 L de solution aqueuse de glucose contenant n2 = 1,5 mole de est C16H10N2O2 : on en dissout n = 3,5 mol dans un volume d'eau suffisant pour |


















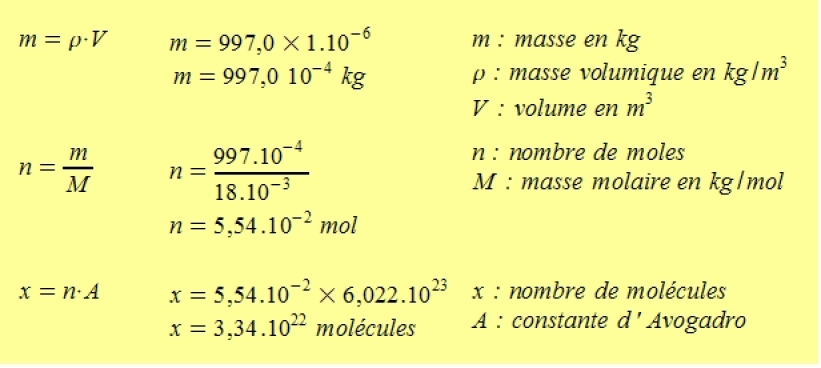







![Corrigé [PDF - 277 Ko] - Concours Geipi Polytech Corrigé [PDF - 277 Ko] - Concours Geipi Polytech](https://upload.wikimedia.org/wikipedia/commons/thumb/e/e9/Water_molecule_dimensions.svg/langfr-200px-Water_molecule_dimensions.svg.png)