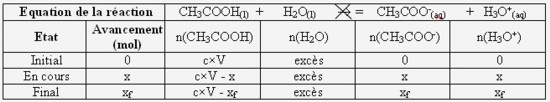reaction totale ou limitée
|
Chapitre 2
Lors d'une transformation chimique on dit que la réaction est totale si elle s'arrête uniquement lorsque l'un des réactifs (ou plusieurs) a (ont) été |
|
Chimie – Partie B – Chapitre 3 : Transformations limitées
L'avancement maximal xmax d'une transformation représente l'avancement correspondant à une transformation totale c'est-à-dire une transformation ou le réactif |
|
Cinétique chimique : introduction
On peut établir un tableau d'avancement : A l'instant final si on a n0 ‐ ξfinal = 0 alors la réaction est totale et on atteint l'avancement maximal |
|
La réaction chimique
REACTION TOTALE : Lors d'une réaction totale il y a disparition du réactif limitant l'avancement final est égal à l'avancement maximal Les autres |
|
Reaction chimique
On dit qu'une réaction est Totale ou Quantitative quand cette réaction n'est possible que dans un seul sens En revanche il ne se passe aucune réaction si on |
|
Réactions chimiques totales et limitées Equilibre chimique
2) Définition d'une réaction chimique totale V) REACTIONS CHIMIQUES LIMITEES VI) TAUX D'AVANCEMENT FINAL D'UNE REACTION CHIMIQUE VII) EXEMPLE Mise en |
|
Réactions limitées
7 Quand la réaction est totale ? Transformation totale : une transformation chimique est totale si au moins l'un des réactifs a été entièrement consommé |
|
Transformation et reaction chimique
Pour déterminer si une transformation est totale ou limitée il faut calculer le taux d'avancement final Dans ce programme on ne parle plus de transformation |
|
TRANSFORMATION TOTALE OU LIMITE
Autrement la réaction est limitée Lorsque une transformation n'est pas totale la réaction associée peut s'effectuer dans les deux sens une telle |
|
Transformations chimiques seffectuant dans les deux sens
Transformation non totale ou limitée est une transformation dont leur évolution s'arrête sans la disparition totale de tout réactif du système chimique |
Comment savoir si une réaction est totale ou limitée ?
Une réaction est totale si à la fin de la réaction au moins un des deux réactifs est complètement consommé : il s'agit du réactif limitant.
Une réaction est non totale si tous les réactifs et les produits sont présents à la fin de la réaction.C'est quoi une réaction limitée ?
Qu'est-ce qu'une réaction limitée ? Une réaction limitée se termine lorsqu'un des réactifs est épuisé.
C'est quoi une transformation totale ?
4Définitions Transformation totale : une transformation chimique est totale si au moins l'un des réactifs a été entièrement consommé.
- , ce qui revient à dire qu'à l'équilibre chimique, les produits sont en concentrations importantes devant celles des réactifs : Si ce bandeau n'est plus pertinent, retirez-le.
|
La Réaction chimique.
II - Réaction totale ou limitée (rappel du premier semestre). Quand une réaction est totale : le réactif qui disparaît complètement est appelé réactif |
|
Reaction chimique - Thermodynamique - Cinétique
II - Réaction totale ou limitée (rappel du premier semestre). Quand une réaction est totale : le réactif qui disparaît complètement est appelé réactif |
|
Partie B – Chapitre 3 : Transformations limitées
Pourquoi une transformation chimique pourrait ne pas être totale ? Nous avons vu dans les précédents Chapitre 3 : Transformations limitées : réactions. |
|
Mesure de pH. Réaction totale ? ou limitée o
Réaction totale ? ou limitée o. I. Mesure de pH et incertitude : Le professeur va vous montrer : Comment étalonner le pH-mètre ? |
|
TRANSFORMATION ET REACTION CHIMIQUE A.Transformation ou
la transformation est totale ou limitée. ? = xf / xmax. Le taux d'avancement final dépend de la constante d'équilibre associée à la réaction et de l'état |
|
ACIDE FAIBLE ? FORT? cest à dire réaction avec leau limitée
On constate donc que xf < xmax : La réaction entre l'acide et l'eau n'est pas totale elle est limitée. Elle mène à un équilibre chimique. |
|
Transformations chimiques seffectuant dans les deux sens
totalement et on dit que la réaction n'est pas totale ou limitée. 2-2– Définition : Transformation non totale ou limitée est une transformation dont leur |
|
Étude de lévolution dun système chimique
Si une réaction est non totale c'est à dire limitée à l'état final |
|
Chapitre 3 : Transformations totales ou limitées
Montrer que le taux d'avancement final de la transformation ne dépend pas du volume V1. 3.2. Calculer sa valeur. La réaction est-elle totale ? Exercice 2 : |
|
Exercice 1 : Étude de différentes formes daspirine (5 points) 1
La réaction de l'aspirine avec l'eau n'est pas une réaction totale mais une réaction limitée car xf < xmax. On peut donc affirmer que l'aspirine est un |
|
Reaction chimique - Thermodynamique - Cinétique
Quand une réaction totale est faite dans les proportions stœchiométriques tous les réactifs disparaissent à l’issue de la réaction Exemple : A3B 2C Dans l’état initial nA= 0 3 mol nB= 0 8 mol et nC= 0 Calculer sachant que la réaction est totale |
|
Reaction chimique - Thermodynamique - Cinétique
4 Réaction totale ou limitée Il y a existence d’un réactif limitant dont la disparition provoque l’arrêt de la réaction Pour ce réactif limitant n f = 0 mol A l’état ?nal ? f = ? max On peut remplacer le signe « = » de l’équation de réaction par une simple ?èche « ? » Réaction totale / quantitative |
|
RÉACTIONS ACIDO-BASIQUES
a) Réaction totale ou limitée Exemple de réaction totale : +HCl (g) + H 2 O (l) Cl - (aq) + H 3 O (aq) Avancement maximal théorique : - x max = C V = 25 10 4 mol Avancement final expérimental +: x f-= [H 3 O ] V = 10-pH V = 10 202 x 25 10-3 = 239 10-4 mol Exemple de réaction limitée : +CH 3 COOH (?) + H 2 O (?) CH 3 COO - (aq |
|
Chapitre 6 : Etat final d’un système chimique - WordPresscom
dit alors que la réaction est non-totale ou limitée Dans ce cas les réactifs et les produits coexistent à l’état final Cet état est alors appelé état d’équilibre chimique Réaction totale Réaction non-totale Une réaction non-totale est modélisée par deux réactions s’effectuant dans des sens opposés : |
Comment savoir si une réaction est totale ou limitée ?
II - Réaction totale ou limitée (rappel du premier semestre) Quand une réaction est totale : le réactif qui disparaît complètement est appelé réactif limitant. Quand une réaction totale est faite dans les proportions stœchiométriques, tous les réactifs disparaissent à l’issue de la réaction.
Comment calculer le réactif limitant ?
Quand une réaction totale est faite dans les proportions stœchiométriques, tous les réactifs disparaissent à l’issue de la réaction. Exemple : A3B 2C? ? Dans l’état initial, nA= 0.3 mol, nB= 0.8 mol et nC= 0 Calculer ? sachant que la réaction est totale. Quel est le réactif limitant ? A + 3B ?2C t0= 0 0.3 0.8 0
Comment calculer l’état final d’une réaction chimique ?
L’état final est donc : nA= 0.03 mol, nB= 0 et nC= 0.54 mol. Remarque : si on écrit l’équation-bilan :1/2 3/ C A ? 2 B?, on obtiendra le même résultat final. Université du Maine - Faculté des Sciences La réaction chimique 2/2 III - Les différents types de réaction
Comment calculer l’avancement d’une réaction ?
Une réaction peut être réalisée dans les conditions stœchiométriques ou avec un excès de l’un des réactifs. Le calcul du rendement ou taux d’avancement? d’une réaction se fait à partir du nombre de mole du réactif limitant(réactif qui disparaît totalement). Pour une réaction quelconque : On définit l’avancement de la réaction : kok i oi o kk o
Quand on dit qu'une réaction est totale ?
. Quand une réaction totale est faite dans les proportions stœchiométriques, tous les réactifs disparaissent à l'issue de la réaction.
Pourquoi la réaction est totale ?
. L'avancement à l'état final est noté xf et s'exprime en mol.
. Définition de la réaction totale : l'un des réactifs est totalement consommé.
Comment savoir si une réaction est totale avec le pH ?
. On considère une solution d'acide chlorhydrique de concentration c = 1.0*10-2 mol/L. On mesure le pH d'un volume V de solution, on obtient alors pH = 2.0.
Pourquoi une réaction n'est pas totale ?
. Autrement, la réaction est limitée. Lorsque une transformation n'est pas totale, la réaction associée peut s'effectuer dans les deux sens, une telle réaction est dite réversible.
|
Page 1 Déterminer un réactif limitant et un avancement maximum
On fait réagir 0,08 mol de d'aluminium avec 0,09mol de soufre Il se forme du sulfure d'aluminium selon la réaction dont l'équation bilan est 2 Al + 3 S = Al2S3 |
|
Hydroxyde de sodium et solutions aqueuses - INRS
Les réactions de l'hydroxyde de sodium avec de nombreux composés des souris ont été exposées à de la soude diluée à 50 , au maximum 2 heures, avec |
|
Definition of reaction thresholds and tolerance limits for testing the
16 fév 2018 · In its recommendation from 2010, 'Physical-technical quality assurance in radiotherapy - proposals for the testing of the total treatment system', |
|
Limite de linéarité Importance de la dilution - CSCQ
Chaque méthode possède une limite de détection et une limite de quantification connues et Inférieur à la limite de détection ou " |
|
ANALYTICAL DETECTION LIMIT GUIDANCE - Wisconsin DNR
Laboratory Guide for Determining Method Detection Limits Wisconsin which a plot of the concentration of an analyte versus the response of that particular analyte remains A justifiable reporting limit for total suspended solids (and |
|
Effects of Transport Limitations on Rates of Solid-Catalyzed Reactions
6 mar 1999 · (constant total concentration) can be obtained from simplifying the Stefan- Maxwell mass-transfer limitations on the observed reaction rate |
|
Chapter 14 Chemical Kinetics
Determine the rate law and rate constant for a reaction from a series of experiments given the measured rates x+y = overall reaction order or (total) order of the reaction the rate-determining step (rds) or rate-limiting step Elementary Step |