Composés ioniques, equations de dissolution, Masse molaire Terminale Chimie
|
Dissolution des composés ioniques dans leau
1- Équation de dissolution du chlorure de sodium (NaCl) constitué d'ions chlorure (Cl–) et d'ions sodium (Na+) : NaCl(s) |
|
Fiche 4 : Les composés ioniques
Pour respecter l'électroneutralité ces solides ioniques sont constitués d'ions : cations et anions Exemple : Quel solide ionique pouvons-nous former avec l' |
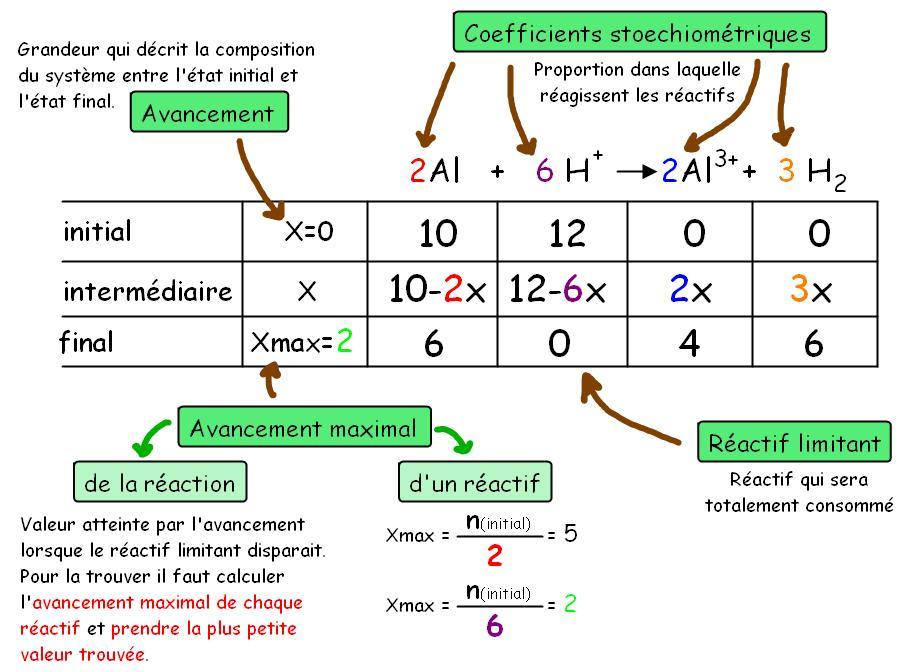
Comment ecrire l équation de dissolution d'un solide ionique ?
Écrire l'équation de dissolution
On écrit l'équation de dissolution en dessinant une flèche orientée vers la droite et en indiquant la formule du solide ionique à sa gauche et les formules des ions, précédées de leurs coefficients stœchiométriques (égaux à leurs indices dans la formule du solide), à droite.Quel est l'équation de la dissolution ?
L'équation de dissolution dans l'eau est : FeCl3, 6 H2O (s)→ Fe3+ (aq) + 3 Cl– (aq)+ 6 H2O (l) D'après l'équation de dissolution : n(Fe3+(aq)) = n(FeCl3, 6 H2O).
En divisant par V : n(Fe3+(aq)) / V = n(FeCl3, 6 H2O) / V. [Fe3+] = c = 3,50 × 10–2 mol.
L–1.Comment trouver la formule d'un composé ionique ?
Pour trouver la formule ionique d'un composé, identifiez d'abord le cation et notez son symbole et sa charge.
Ensuite, identifiez l'anion et notez son symbole et sa charge.
Enfin, combinez les deux ions pour former un composé électriquement neutre.- Cela forme le solide ionique : CaCl2(s) nommé chlorure de calcium (sel utilisé pour le salage des routes en hiver).
|
Chapitre 5 de la structure à la cohésion solubilité et miscibilité des
1e Spécialité Physique Chimie. CHAPITRE 5 2 Dissolution des solides ioniques. Exercice 1. Exercice 2 ... Connaissant la masse molaire moléculaire. |
|
EXERCICES
1e Spécialité Physique Chimie. CHAPITRE 1. DÉTERMINATION DE LA miques ou composés ioniques suivants : ... Calculer la masse molaire de l'eau de deux. |
|
Exercices de physique-chimie Première Spécialité
Calculer la masse molaire des esp`eces chimiques ou composés ioniques suivants : Écrire l'équation de la réaction de dissolution dans l'eau du sulfate ... |
| Correction exercices Précis de Physique-Chimie chapitre1 à 4 |
|
La dissolution du composé solide FeCl3(s) dans leau donne
Donner l'équation de dissolution du chlorure de fer III solide dans l'eau : 3 n0(soluté) la quantité de matière initiale du composé ionique. |
|
Accompagnement personnalisé – Physique-chimie Concentration
2- Calculer les concentrations molaires des espèces ioniques présentes dans 2-Écrire l'équation de la réaction de dissolution du chlorure de fer (III) ... |
|
Programme de physique-chimie de première générale
Les notions de masse molaire volume molaire et concentration en quantité de matière (en composé ionique dans l'eau par une équation de réaction |
|
COURS DE CHIMIE Avec EXERCICES
5- Masse atomique et masse molaire . 2- Précipitation et non précipitation d'un composé ionique peu soluble............................ 171. |
|
Solution Des Exercices
L'équation est : N2 (g) + 3H2 (g) 2NH. ?. 3 (g). 2. Quantité de matière de diazote : La quantité de matière mis en jeu sachant que la masse molaire de |
|
Rappel : les formules de chimie
La masse molaire atomique MC =12 g.mol-1 : une mole d'atomes de carbone pèse 12 g. La masse molaire moléculaire s'obtient en ajoutant les masses molaires |
Comment ecrire l équation de la dissolution ?
Quelle est la formule d'un composé ionique ?
. Exemple : le chlorure de baryum est composé d'ions chlorure Cl- et d'ions baryum Ba2+.
. La charge apportée par un ion baryum (1 x +2) est compensée par la charge apportée par 2 ions chlorure (2 x -1).
. La formule est : BaCl2.
Quelles sont les 3 étapes clés au cours de la dissolution d'un composé ionique ?
Qu'est-ce que l équation de dissolution ?
|
EXERCICES - Physicus
1e Spécialité Physique Chimie CHAPITRE 1 COMPOSITION D'UN 1 MASSES MOLAIRES ET QUANTITÉS DE MATIÈRE Exercice Calculer la masse molaire des espèces chi- miques ou composés ioniques suivants : 1 fabriquée par dissolution de 10 g de bicar- Dans cette équation, on reconnaît la défini- |
|
PHYSIQUE-CHIMIE - TEL archives ouvertes
classes de Terminale D des collèges et lycées en République du Bénin Produit ionique ; pH d'une solution aqueuse pendule élastique ; équation différentielle; fréquence propre ; Composition du noyau : nucléons densité d, contenant en masse p de produit de masse molaire M Le volume V0 à prélever est tel |
|
Rappel : les formules de chimie
La masse molaire atomique MC =12 g mol-1 : une mole d'atomes de carbone pèse 12 g La masse molaire moléculaire s'obtient en ajoutant les masses molaires Ecrire l'équation de dissolution et déterminer les concentrations des espèces lorsque le soluté solide ionique se transforme en espèces séparées ioniques ? |
|
Cours et exercices de chimie des solutions - Elearning-ESGEE
Cours et exercices de chimie des La concentration massique ou titre pondérale tP d'une solution est la masse d'un Conductivité molaire ionique limite : l'équation (1) ne reflète pas une réaction chimique réelle ; on l'appelle parfois la demi- Calculer le pH de 500 mL d'une solution aqueuse préparée par dissolution |
|
EQUILIBRES CHIMIQUES CINETIQUE CHIMIE EN SOLUTION
1) Relations entre grandeurs molaires standards de réaction 25 2) La dissolution est un phénomène limité 58 Pour ce faire, on introduit des grandeurs d'état, liées par des équations d'état composition du système est encore donnée par la loi d'action de masse dissolution d'un composé ionique dans l'eau) |
|
Exercices de révisions : Physique-chimie
3 En déduire l'équation de la réaction étudiée (réaction de dismuation) Un élève a préparé cette solution par dissolution du solide dans 100,0 mL d'eau 5) Déterminer la composition, en quantité de matière, du système (c'est à dire toutes les Masse molaire atomique du zinc et du cuivre : M(Zn) = 65,4 g mol-1 |
|
Cours de Chimie Structure de la matière - USTO
Eq II 3 de même la masse molaire sera : M = Σ (xi Mi) (g/mole) Eq II 4 La masse atomique tiendra compte de sa composition, elle est donnée par l' équation |
|
Télécharger ce fichier pdf - Labolycée
À partir de l'exploitation des courbes données ci-dessous déterminer la concentration molaire d'acide citrique de la solution titrée Titrage pH-métrique de la |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
Potentiels d'oxydoréduction : Equation de Nernst La concentration molaire d' une espèce chimique en solution CA est la Calculer la masse de soude NaOH nécessaire pour préparer 50 mL d'une le volume de gaz à dissoudre, V le volume de la solution, Vm le volume molaire des La composition du système est |