abondance isotopique calcul
|
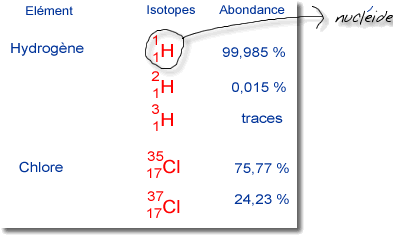
Abondance isotopique et masse Atomique relative
L'abondance isotopique est le pourcentage ( proportion ) de la masse d'un isotope dans la masse atomique d'un élément Page 4 Abondance isotopique et masse |
|
Chapitre 5 La mole
2 : Calcule l'abondance relative de chaque isotope du bore selon les infos pdf Page 11 Ch5 11 2013 Conversion nombre de moles ⇒masse en g masse = nombre |
|
Chimie 30S Devoir : Masse atomique moyenne 1 Les deux isotopes
Sachant que la masse atomique moyenne de cet élément est de 159994u calcule l'abondance relative de chacun des deux autres isotopes en pourcentage 15x + 16(1 |
|
Exercice N°1 M(X)= ∑ ∗ K)]/100 K) + X3*M ( 39102= 389637
2- Calculer l'énergie de liaison El de l'isotope 39K en joule puis en Mev/noyau Solution : 1-Calcul les abondances naturelles des isotopes 39K et 41K : On |
|
EXERCICES SUR LES CONSTITUANTS DE LA MATIERE (Série N°1)
1) Quel est l'isotope du silicium le plus abondant ? 2) Calculer l'abondance naturelle des deux autres isotopes Page 2 Exercice N°4 1) Le noyau de l'atome |
|
Fiche de synthèse n° 2a Isotopes et masse molaire
Calcul de la masse molaire moyenne La masse molaire d'un élément chimique doit en réalité tenir compte des proportions des différents isotopes rencontrés |
|
TD N° 01 DE CHIMIE
2 Calculer l'abondance naturelle des deux autres isotopes Exercice 4 Les masses du proton du neutron et de l'électron sont respectivement |
|
TD N°01 Structure de latome
Indiquer la composition des deux isotopes Sachant que la masse molaire du mélange isotopique naturel est de 63540 calculer l'abondance des deux isotopes |
|
UE
1) Donnez la composition du noyau de l'isotope 123Sb 2) Calculer l'abondance naturelle des deux isotopes de l'antimoine Exercice 4 Le bore (B) a une masse |
Comment calculer l'abondance de l'isotope ?
L'abondance relative de chaque isotope peut être déterminée par spectrométrie de masse.
Dans un spectromètre de masse un faisceau d'électrons de haute énergie est utilisé pour vaporiser et ioniser les atomes et les molécules.Comment calculer l'abondance ?
l'abondance relative est la quantité relative au nombre d'individus d'une espèce donnée par unité de surface ou de volume par rapport au nombre total d'individus de toutes les espèces confondues.
L'abondance relative est calculée selon la formule : Ar = Aa/N×100, N étant le nombre total d'individus.Comment calculer l'abondance isotopique du carbone ?
La mesure de l'abondance isotopique du carbone se fait en spectrométrie de masse, sur des instru- ments dits à source gazeuse, dans lesquels l'élé- ment étudié est préalablement converti sous forme d'un gaz, le plus chimiquement inerte possible.
- L'abondance isotopique d'un isotope est la fraction molaire de cet isotope dans le mélange exprimée en %.
La somme des abondances isotopiques est égale à 100.
|
1. Déterminer la masse atomique moyenne du carbone sachant quil
m.a.m. = (m 12C x % abondance) + (m 13C x % abondance) Isotope. Masse atomique. (u). % abondance ... Calculer la masse atomique moyenne du. |
|
Chapitre 5 La mole
Par exemple le magnésium a 3 isotopes naturels |
|
7 abondances naturelles des isotopes
Afin d'aider le lecteur à apprécier les valeurs d'abondance naturelle telles pour le calcul de 13?g/b as 13?g/b ? 1 avec 13?g/b = 0.0111421/0.0112372 ... |
|
LA METHODE ISOTOPIQUE
ABONDANCE ISOTOPIQUE. (Pour les détails voir volume I). L'hydrogène et l'oxygène comportent un certain nombre d'isotopes |
|
TP BT06 MS_LCESI_2012 QTOF
Abondance isotopique = pourcentage des isotopes d'un élément dans la nature Calcul de l'abondance relative des satellites isotopiques M+1 M+2 pour. |
|
1. Lazote possède 2 isotopes. La masse de lazote 14 équivaut à 14
détermine le % abondance de chacun des isotopes. Isotope abondance 15N = 100 – X = 100 - 9964 = 0 |
|
Chimie 30S Devoir : Masse atomique moyenne 1. Les deux isotopes
2. À l'état naturel le silicium se compose de trois isotopes. Voici ces isotopes suivis de leur abondance relative et de leur masse atomique : le Si. |
|
Module 2- Quantités chimiques
chaque isotope présent dans un élément porte le nom d'abondance relative Afin de calculer la masse atomique moyenne d'un élément il faut. |
|
T.D. N° 01 DE CHIMIE
Quel est l'isotope du silicium le plus abondant ? 2. Calculer l'abondance naturelle des deux autres isotopes. Exercice 4. Les masses du proton du neutron et de |
|
UE - Éléments Chimiques TD1 : Latome
2) Calculer l'abondance naturelle des deux isotopes de l'antimoine. Exercice 4. Le bore (B) a une masse atomique moyenne de 10811 u et un numéro atomique Z |
|
Isotopes et spectrométrie de masse (leçon) Khan Academy
LA METHODE ISOTOPIQUE 2 1 ABONDANCE ISOTOPIQUE (Pour les détails voir volume I) L’hydrogène et l’oxygène comportent un certain nombre d’isotopes dont les variations dans les eaux naturelles servent de support à l’utilisation des techniques isotopiques en Hydrologie |
|
4 VARIATIONS DES ABONDANCES PAR LES PROCESSUS NATURELS - IAEA
Les valeurs de ? déterminées par les laboratoires isotopiques peuvent alors être transformées en valeurs R en appliquant (réécriture de l’équation 4 2): R = Rr(1 + ?) (4 3) ou les valeurs Rrsont les rapports isotopiques des matériaux de référence internationaux qui seront définis plus loin dans le Chapitre 7 |
|
Spectrométrie de masse –Introduction
• Abondance isotopique = pourcentage des isotopes d’un élément dans la nature • Masse moyenne pondérée (MM) = Masse atomique apparaissant sur le tableau périodique et qui tient compte des isotopes et de leur abondance Exemple : nbre de nbre de protons : nucléons : nbre nbre de nbre masse abondance abondance |
Qu'est-ce que l' abondance relative d'un isotope ?
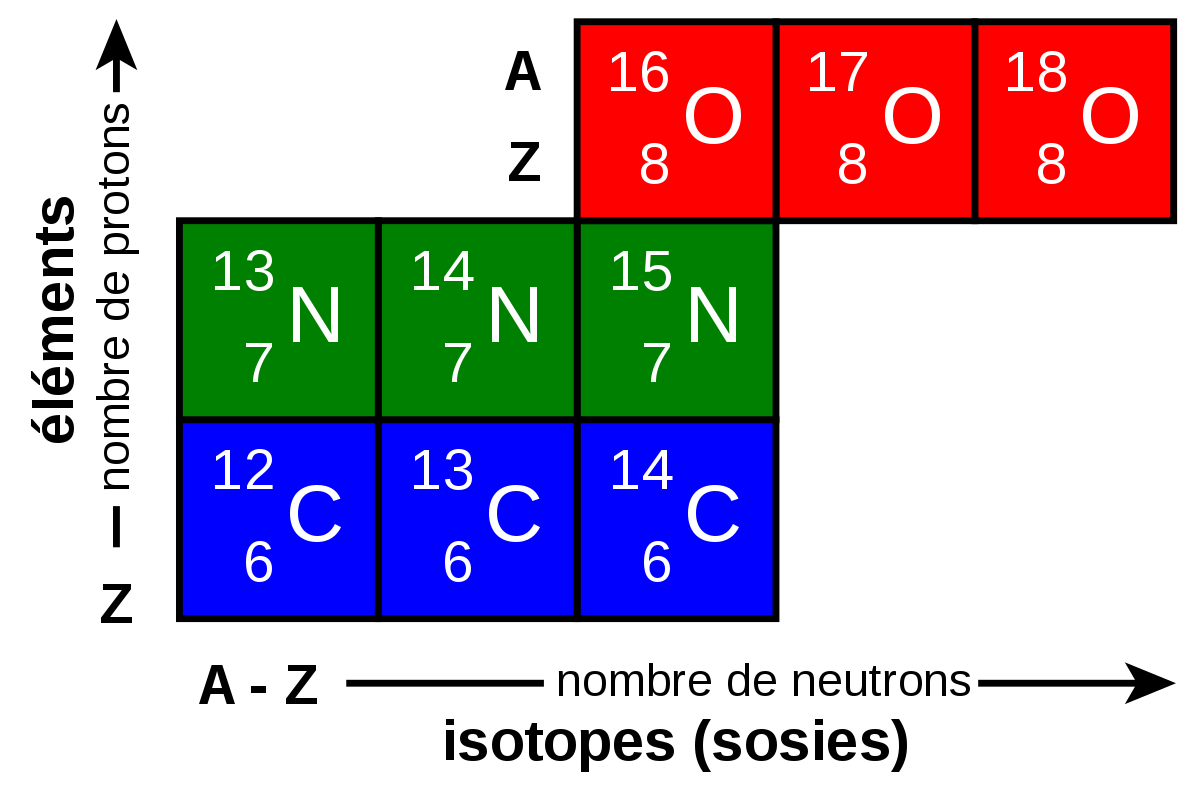
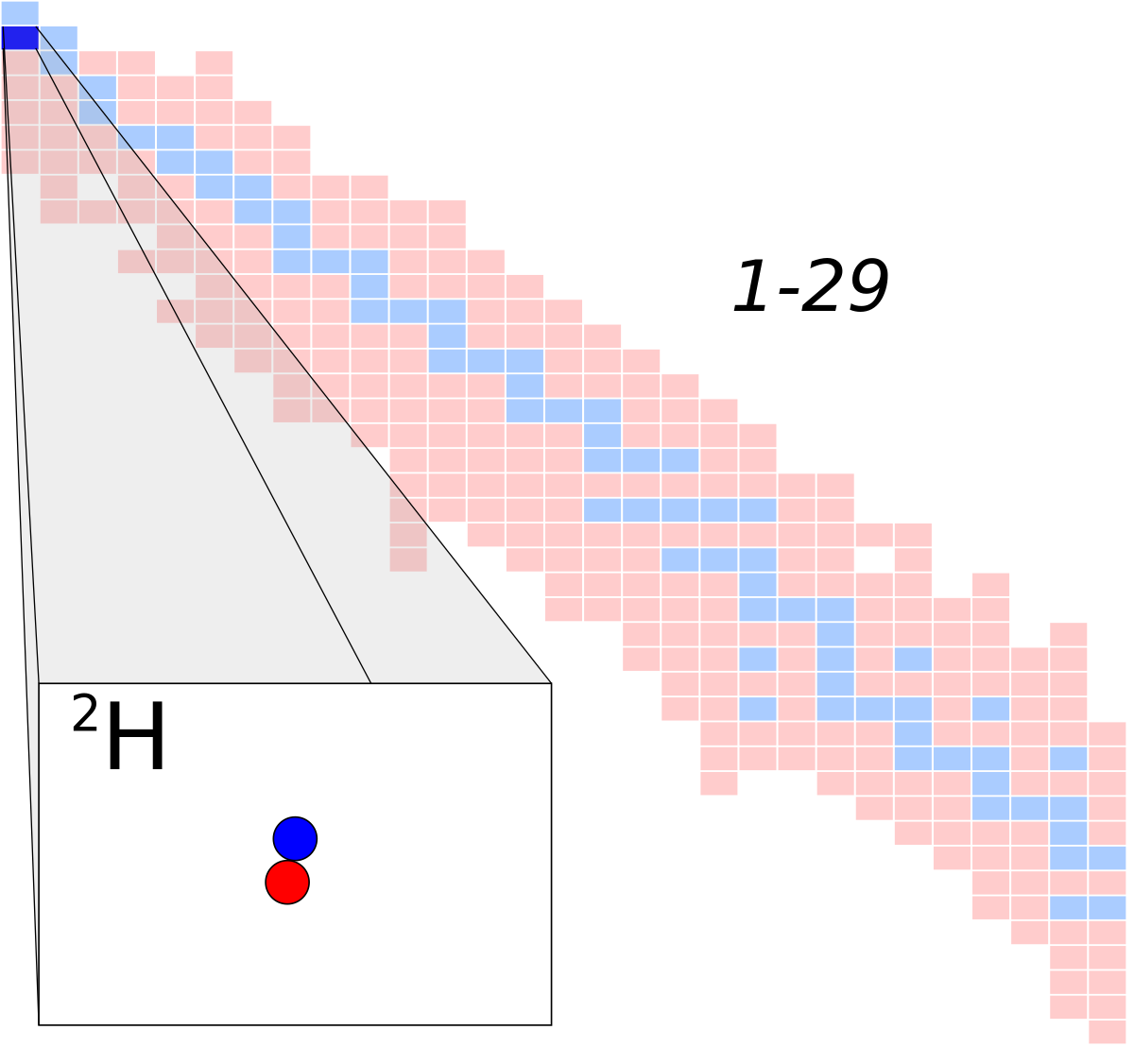
Les atomes qui possèdent un même nombre de protons et d'électrons mais un nombre différent de neutrons sont appelés isotopes. Les isotopes possèdent des masses atomiques différentes. L' abondance relative d'un isotope correspond à la proportion sur Terre d'un même élément de masse atomique spécifique.
Comment calculer l'abondance d'un isotope ?
L'abondance relative de chaque isotope peut être déterminée à partir de la hauteur, ou intensité, du pic de rapport masse sur charge correspondant. Sur la simulation du spectre de masse, on suppose que chaque ion identifié par un pic est porteur d'une charge 1+ 1+, permettant ainsi de calculer la masse atomique de chaque isotope.
Comment détecter les isotopes ?
Isotopes et masse atomique. Comment les isotopes peuvent être détectés à l’aide de la spectrométrie de masse. Les atomes qui possèdent un même nombre de protons et d'électrons mais un nombre différent de neutrons sont appelés isotopes. Les isotopes possèdent des masses atomiques différentes.
Comment définir un isotope en particulier ?
De la même façon que le numéro atomique définit l'élément, le nombre de masse définit l'isotope spécifique de cet élément en particulier. De fait, la façon la plus simple de définir un isotope en particulier est d'utiliser la notation "nom de l'élément - nombre de masse".
Quel est la formule de l'abondance ?
. L'abondance relative est calculée selon la formule : Ar = Aa/N?0, N étant le nombre total d'individus.
Qu'est-ce que l'abondance isotopique ?
. La somme des abondances isotopiques est égale à 100.
. La composition isotopique d'un élément est constituée des valeurs des abondances isotopiques des isotopes qui le composent.
Comment savoir quel est l'isotope le plus abondant ?
|
TD N° 01 DE CHIMIE
Quel est l'isotope du silicium le plus abondant ? 2 Calculer l'abondance naturelle des deux autres isotopes Exercice 4 Les masses du proton, du neutron et de |
|
1 Déterminer la masse atomique moyenne du carbone - Pages
13u 1,108 Isotope Masse atomique (u) abondance 12C 12u 98,892 13C 13u 1,108 Calculer la masse atomique moyenne du néon m a m = ? |
|
UE - Éléments Chimiques TD1 : Latome - Université de Strasbourg
2) Calculer l'abondance naturelle des deux isotopes de l'antimoine Exercice 4 Le bore (B) a une masse atomique moyenne de 10,811 u et un numéro atomique |
|
PDF :1 - BIENVENUE SUR LA PAGE DE THIERRY BRIERE
3) Evaluer approximativement l'abondance naturelle de chacun des isotopes Le calcul indirect en partant de la masse en kg multipliée par N pour passer à la |
|
Chapitre 5 La mole - DSFM
Par exemple, le magnésium a 3 isotopes naturels, l'abondance relative de chaque isotope est : 24Mg = 79 ; 25Mg = 10 ; 26Mg = 11 Sa masse atomique |
|
Chimie 521 – Masse atomique
Les atomes de chaque isotope ont des masses l'abondance en pourcentage et la masse d'un atome calculer la masse atomique de l'élément « soupe » : |
|
I Masse dun atome
La stœchiométrie est un calcul qui permet d'analyser les quantités de réactifs isotopes des masse isotopes des relative abondance × ∑ Masse atomique |
|
FICHE 2 - 2ATP
Masse molaire atomique, abondance isotopique, masse atomique relative : molaire atomique : connaître la proportion de chacun des isotopes pour calculer la |
|
Td2_-1pdf - Département de Géologie
2 Calculer la masse atomique de l'azote naturel sachant que : 14N a une masse de 14,007515u m a et une abondance isotopique de 99,635 'N a une |