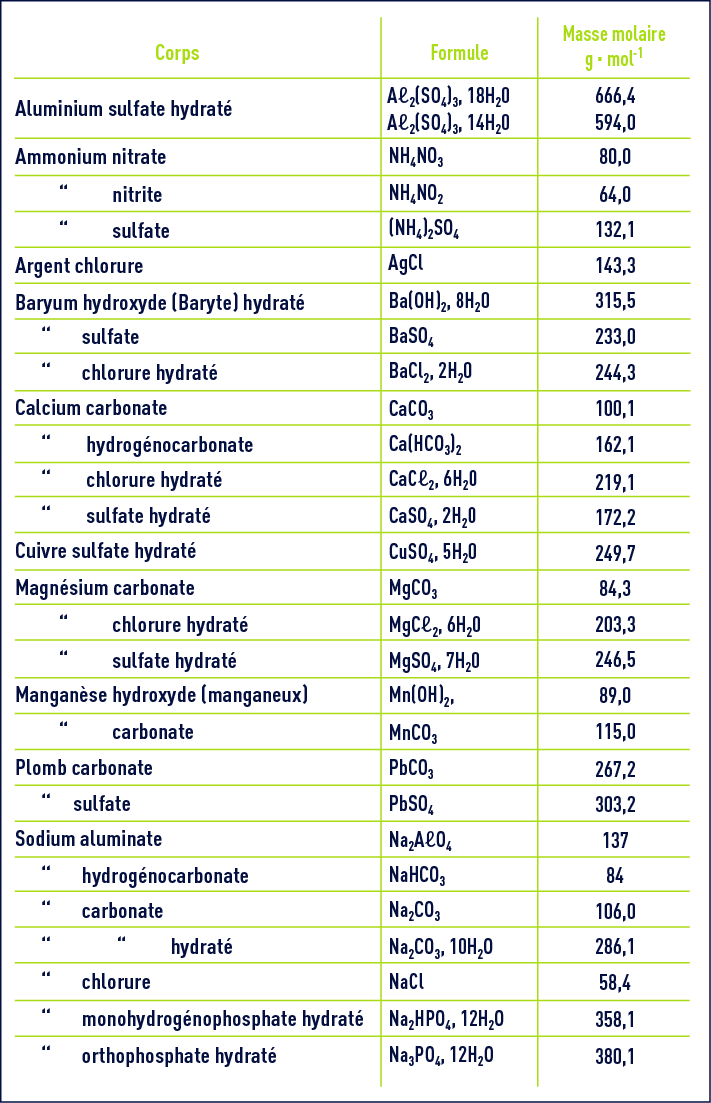
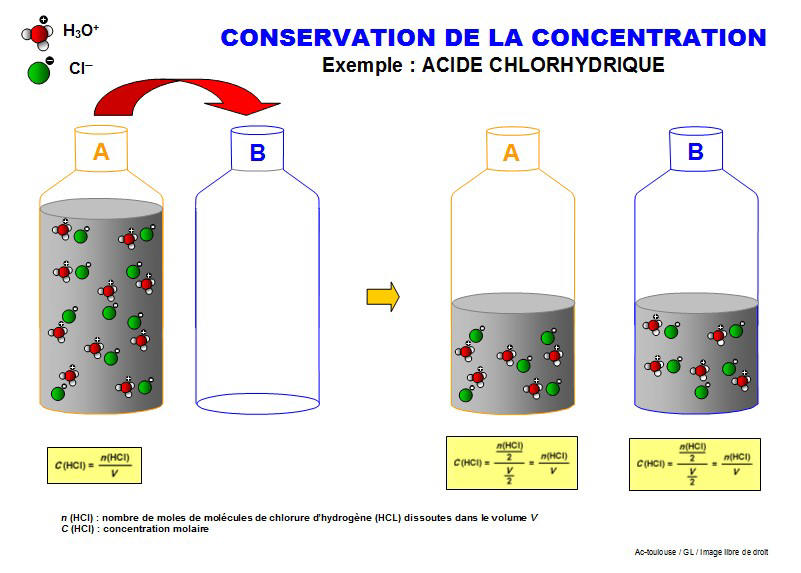
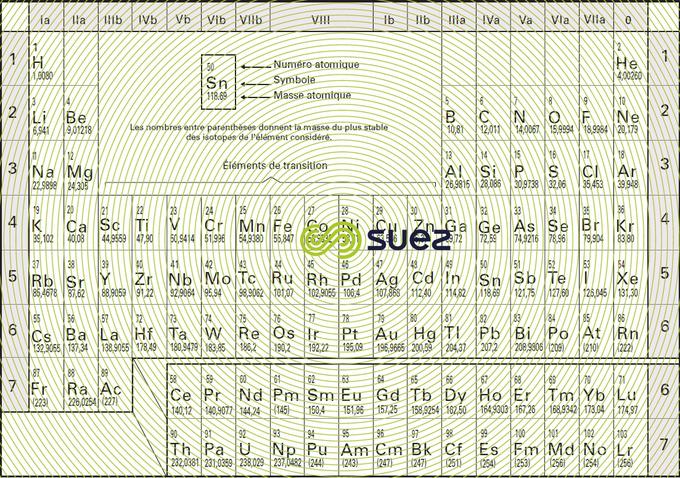
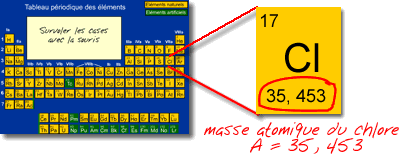
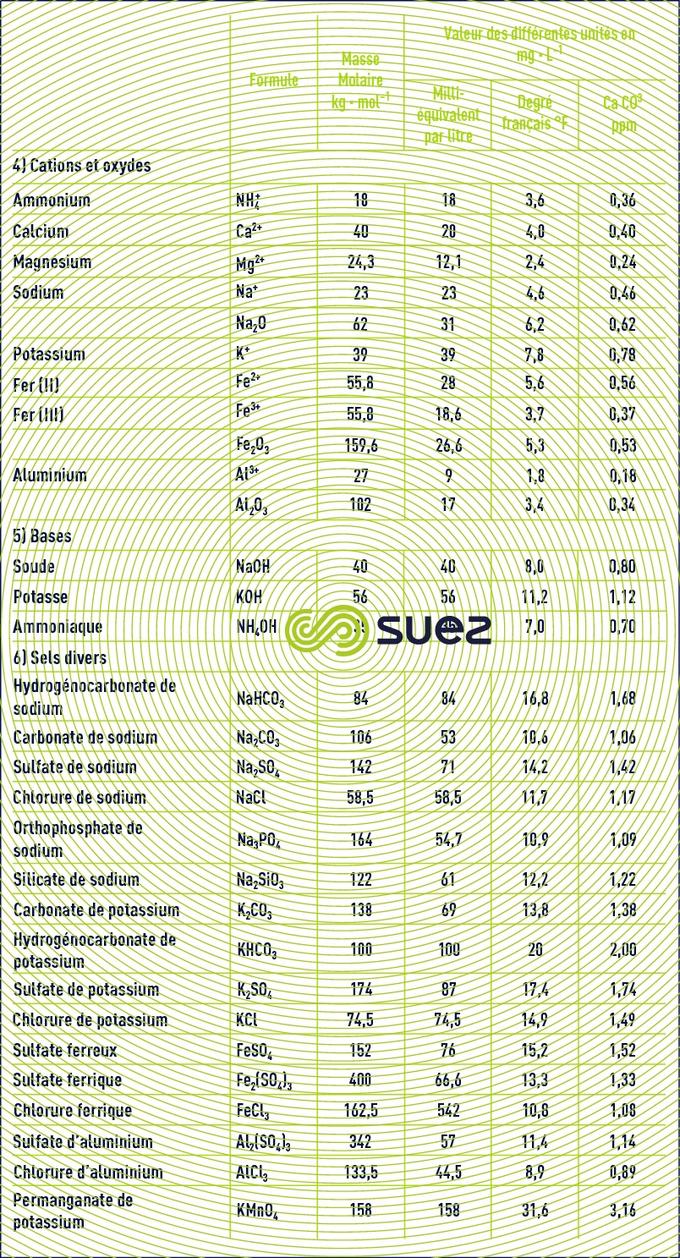
composition isotopique molaire et massique du chlore
|
Chimie Générale (Chimie 1)
23 déc 2020 · Composition massique 3 Les solutions 3 1 Définition 3 2 On peut citer comme exemples les isotopes de l'oxygène et du chlore : ; 8 16 |
|
Détermination précise de la composition isotopique
La composition isotopique et élémentaire d'échantillons nucléaires a été déterminée par couplage de l'électrophorèse capillaire (CE) à la spectrométrie de masse |
|
Fiche de synthèse n° 2a Isotopes et masse molaire
Composition isotopique de l'élément chlore : Isotope du chlore 35Cl 37Cl Proportions ( ) 758 242 La masse molaire de l'élément chlore vaut donc : |
|
Structure de la matière 1 Utilisation de la masse molaire 2 Quantité
3 Le chlore naturel La masse molaire du chlore vaut M(Cl) = 35453 g mol −1 Sachant que le chlore est un mé- lange des isotopes M(35Cl) et M(37Cl) dont |
|
Utilisation des isotopes stables du chlore pour le traçage des
7 mai 2018 · COMPOSITION ISOTOPIQUE DU CHLORE Figure 65 : Coefficients d'atténuation massique de différents solides et solutions salines |
|
¢¡¤£¦¥¨§©£¦¥ ¥ !¡¤$#©¥% ¥&) (10©032¤¡¤£45&!¡¤67§3 8
Le chlore naturel est un mélange de deux isotopes 35Cl et 37Cl dont les E n conséquence la masse molaire de l'élémént chlore est de 35 5 g mol |
Quelle est la masse molaire du chlore ?
Dans le tableau périodique figure alors une masse molaire moyenne calculée à partir de la composition isotopique de l'élément chimique considéré.
La masse molaire de l'élément chlore vaut donc : MCl = 35 × 75,8/100 + 37 × 24,2/100 = 35,5 g·mol–1.Comment déterminer la composition isotopique d'un élément ?
L'élément chlore (Z=17) possède 2 isotopes : le chlore 35 ayant 18 neutrons et le chlore 37 ayant 20 neutrons.
Quels sont les isotopes du chlore ?
La composition isotopique d'un échantillon indique les proportions des divers isotopes d'un élément chimique particulier (ou de plusieurs éléments) dans cet échantillon.
|
Fiche de synthèse n° 2.a Isotopes et masse molaire
De la composition du noyau à la définition d'isotopes La masse molaire de l'élément chlore vaut donc : MCl = 35 × 758/100 + 37 × 24 |
|
I ATOMISTIQUE
la masse molaire des isotopes avec le nombre de masse de ces derniers). Ecrire la structure électronique de l'atome de chlore dans son état énergétique ... |
|
Détermination de la composition isotopique du soufre pour létude
01-Feb-2017 bio-corrosion et l'utilisation de la composition isotopiques du ... Le soufre 32 et le dioxygène 16 ont une masse molaire très proche :. |
|
Détermination de la composition isotopique du soufre pour létude
29-May-2017 bio-corrosion et l'utilisation de la composition isotopiques du ... Le soufre 32 et le dioxygène 16 ont une masse molaire très proche :. |
|
Chimie générale et organique Séries de Travaux Dirigés et Solutions
La masse molaire atomique du carbone est 12011 g/mole. 1. Donner la composition du noyau de chacun des isotopes. 2. Calculer la proportion massique des |
|
Atomistique Corrigé
1) Préciser la composition d'un noyau de l'isotope le plus abondant de l'antimoine 2) Déterminer la masse molaire de l'élément antimoine. |
|
Utilisation des isotopes stables du chlore pour le traçage des
07-May-2018 poreux - impact sur la composition isotopique du chlore . ... (m.s-2) la masse volumique du fluide (kg.m-3) et la hauteur (m). |
|
Biologie cellulaire. Exercices et méthodes
fractions massique et molaire. Fondements et prérequis en chimie 1. MOTS-CLÉS. En chimie la théorie et les applications sont entrelacées à la manière des |
|
Cours de Chimie Structure de la matière
La masse molaire atomique: est la masse d'une mole d'atomes. Chlorure de Sodium de 90ml. 1-Quel est le pourcentage massique en NaCl de cette solution. |
|
Module 2- Quantités chimiques
Masse atomique : MOYENNE des masses des isotopes d'une sorte d'élément b) Quel est le % massique du chlore dans ce composé? m Cl = 105g. |
|
Fiche de synthèse n° 2a Isotopes et masse molaire
Dans le tableau périodique figure alors une masse molaire moyenne calculée à partir de la composition isotopique de l’élément himique onsidéré Exemple: Composition isotopique de l’élément hlore : Isotope du chlore 35Cl S37Cl Proportions ( ) 758 242 N La masse molaire de l’élément chlore vaut donc : M Cl |
Comment calculer la masse molaire d’un chlore?
calculée à partir de la composition isotopique de l’élément chimique considéré. Exemple : Composition isotopique de l’élément chlore :Isotope du chlore Proportions (%) 35Cl 75,8 % 37Cl 24,2 % La masse molaire de l’élément chlore vaut donc : MCl = 35 × 75,8/100 + 37 × 24,2/100 = 35,5 g·mol–1.
Quels sont les isotopes du chlore ?
Seuls deux isotopes sont stables, 35 Cl et 37 Cl, et représentent la quasi-totalité du chlore naturellement présent (respectivement 75,77 et 24,23 %), le reste étant le chlore 36, un radioisotope cosmogénique présent à l'état de trace. La masse atomique standard du chlore est de 35,453 (2) u . Dichlore gazeux. Dichlore liquide.
Quel est le radioisotope du chlore ?
Parmi eux, les deux principaux sont les isotopes stables 35Cl (75,77 %) et 37Cl (24,23 %), présents en proportion relative 37,885:12,115, respectivement, permettant d'attribuer au chlore une masse atomiquestandard de 35,453(2) u Le radioisotope du chlore à la plus longue durée de vie est 36Cl avec une demi-viede 301 000 années.
Quelle est la forme du chlore ?
Le chlore, à l'état de corps simple, se présente sous la forme de la molécule de dichlore Cl 2, qui est un gaz jaune-vert 2,5 fois plus dense que l' air, aux conditions normales de température et de pression. Ce gaz a une odeur suffocante très désagréable et est extrêmement toxique .
Quel est la masse molaire moléculaire du chlore ?
Quelles sont les isotopes du chlore ?
. On peut donc en déduire son nombre de neutrons : A – Z = 7 – 3 = 4.
. Deux isotopes d'un élément chimique poss?nt le même numéro atomique Z mais des nombres de masse A différents.
Comment calculer la composition isotopique d'un élément ?
. Exemples : Masse molaire du chlore : MCl= 35,453 g. mol.
|
Physique EXERCICES - PhyCats - plaforg
La masse molaire atomique du chlore vaut M(Cl) = 35,453 g·mol–1 Considérons l'isotope 34 du soufre (Z = 16), qui constitue 4,2 du soufre naturel Application numérique : M(Cu) = 63,54 g·mol–1 ; masse volumique du cuivre ρ = 8900 kg m–3 ; NA = 6,022 1023 mol–1 Composition initiale de l'air : 4/5 N2 , 1/5 O2 |
|
Module 2- Quantités chimiques - Pages
chaque isotope présent dans un élément porte le nom d'abondance relative d'un isotope b) Quel est le massique du chlore dans ce composé? m Cl = 105g |
|
Cours de Chimie Structure de la matière - USTO
La masse molaire atomique: est la masse d'une mole d'atomes Exemple 1- Quel est le pourcentage massique en NaCl de cette solution 2- Quelle Exemple : Représentation symbolique des trois isotopes de l'hydrogène Quel est le nombre de protons, de neutrons et d'électrons qui participent à la composition des |
|
¢¡¤£¦¥¨§©£¦¥ ¥ ¡¤$#©¥% ¥&) (10©032¤¡¤£45&¡¤67§3 8
1 1 Gaz parfaits et densité massique E n conséquence , la masse molaire de l' élémént chlore est de 35 ,5 g mol −1 compositions isotopiques possibles |
|
Méthodes isotopiques didentification de lorigine des - RECORD
4 4 Autres systèmes isotopiques (inclus la problématique du chlore) compositions isotopiques en carbone restent stables dans des contrôles stériles un élément trace métallique lourd, volatil et hautement incompatible de masse molaire |
|
Concentration en bore - Ce document est le fruit dun long travail
2 2) Les analyses de compositions isotopiques en bore 39 2 2 1) La microsonde Fig 4 8 : Variation du rapport Na/Cl en fonction de la teneur en chlore Une isotopique, dans lesquelles f représente la fraction molaire de B(OH)3, il vient: |
|
ETUDE DU MONOFLUORURE DE CHLORE : - International
Division d'Etudes de Séparation Isotopique et de Chimie Physique Département électronique résolu, le monofluorure de chlore, C1F, est le seul Masse volumique (liq ) notamment pour la détermination des compositions isotopiques |
|
Caractérisation isotopique et géochimique des - InfoTerre - BRGM
Illustration 11 : Composition isotopique des sulfates δ34S et δ18O de l'eau de mer au que sur l'état volumique des nappes ou des masses d'eau bicarbonate, sodium chlorine and sodium sulphate waters can be observed in several |