nombre d'oxydation mno4-
|
Chapitre 3 :Oxydoréduction
Exemple : MnO4 - (permanganate) n o(Mn) + 4 n o(O) = -I n o(O) = -II Donc Oxydation ⇔ augmentation du nombre d'oxydation Réduction ⇔ diminution du |
|
Cours-Réaction-redoxpdf
o Le nombre d'oxydation (appelé aussi degré d'oxydation) est un nombre qui E = E0 (MnO4- / Mn2+) E = E ERH = 0000 v + - MnO 4 - ( 1 M ) Mn2+ (1 M ) |
|
LE NOMBRE DOXYDATION
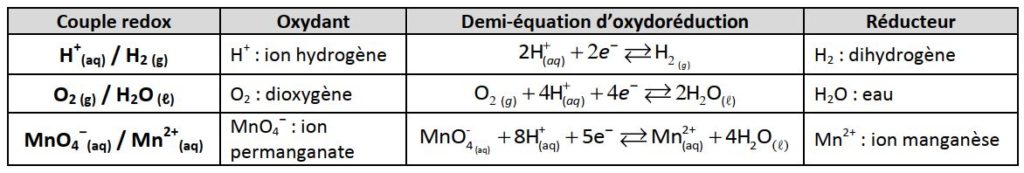
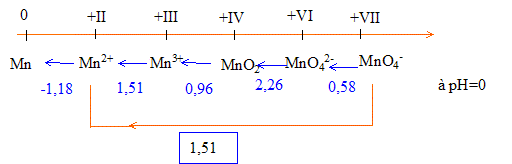
de cuire) Exemple : MnO4 - + 8 H+ + 5 e- = Mn2+ + 4 H2O Le nombre d'oxydation du manganèse Mn passe de +VII (dans l'ion MnO4-) à +II (dans l'ion Mn2+) |
|
LES DOSAGES OXYDO-REDUCTIMETRIQUES (REDOX)
➢ La demi-réaction d'oxydation par le MnO4 - est la suivante MnO4 - + 8H+ + 5 e- Mn2+ + 4H2O ➢ Le potentiel standard du couple MnO4 -/ Mn2+ à pH =0 est |
|
Les réactions doxydoréduction
MnO4 - + 8 H+ + 5 e- = Mn2+ + 4 H2O Le nombre d'oxydation du manganèse Mn passe de +VII (dans l'ion MnO4-) à +II (dans l'ion Mn2+) Page 5 Isabelle Prigent |
|
§ 8 (suite) Equation de Nernst
La corrosion du fer est en réalité due à l'oxygène O2 dont le potentiel d'oxydation à pH 7 E = + 0 81 V / SHE est beaucoup plus élevé L'eau joue toutefois |
Quel est le nombre d'oxydation de MnO4 ?
Dans l'anion permanganate (MnO4-), l'atome de manganèse est lié à quatre atomes d'oxygène par trois doubles liaisons et une simple liaison.
L'état d'oxydation du manganèse dans ce sel est de +7.Comment calculer le nombre d'oxydation ?
Le nombre d'oxydation de chaque atome est alors égal à la différence entre le nombre d'électrons de valence à l'état atomique fondamental et le nombre d'électrons qui lui a été attribué à la suite de cette nouvelle répartition.
Quels sont les nombres d'oxydation ?
Le peroxyde d'hydrogène a la formule chimique H2O2.
L'hydrogène a un nombre d'oxydation de plus un.
Comme son nom l'indique, ce composé est un peroxyde, et l'oxygène aura donc un nombre d'oxydation de moins un.
|
Rappel de 1ère année sur les nombres doxydation
Le nombre d'oxydation d'un élément chimique dans un édifice mono ou polyatomique MnO4. - + 5e- + 8H+ ? Mn2+ + 4 H2O. (1) Equilibre rédox. |
|
Étude dune réaction : titrage des ions fer II par les ions permanganate
Solution de permanganate de potassium. K+(aq) + MnO4. -(aq). Concentration [MnO4. -]. Volume équivalent Véq à déterminer ? Solution acidifiée de sel de Mohr. |
|
Chapitre 4 Oxydo-réduction
pour avoir le même nombre d'atomes d'oxygène de part et d'autre de la double à l'oxydation des ions cyanure CN–(aq) par les ions permanganate MnO4. |
|
Les réactions doxydoréduction
Evolution du nombre d'oxydation dans les réactions Prenons les exemples des couples Cu2+/Cu I2/I- |
|
Problème 1 : Titrage dune solution dacide oxalique
28 apr 2016 La réaction entre l'acide oxalique et les ions permanganate fait l'objet ... en milieu acide sachant que les ions MnO4 ... Degré d'oxydation. |
|
Oxydo-réduction et pile : commentaires scientifiques décrivant les
L'oxydation d'un réactif correspond à une réaction au cours de laquelle des MnO4. -. + 5 e. -. + 8 H. + ? Mn2+. On pondère la matière càd le nombre. |
|
Devoir Surveillé n° 6 Option PSI
24 mag 2018 4) Déduire de la question 1) le nombre d'oxydation maximal de l'élément cérium. ... Mn(OH)2(s) ainsi que les ions en solution Mn2+ et MnO4. |
|
I i i i
CH3-CH2-CH=CH2 + MnO4- ? Mn(IV) + diverse Oxidations- produkte. 3 Voraussetzungen d'oxydation. 3 Conditions ... Nombre de coups de pompe (n). |
|
Exercice 1 : léthylotest comment ça marche ?
1) Quel est le nom des ions MnO4. - ? 1 Pt MnO4. - est l'ion permanganate. KMnO4 est le permanganate de potassium. 2) Quel est le nombre d'oxydation du |
|
Exercice 1 : léthylotest comment ça marche ?
1) Quel est le nom des ions MnO4. - ? 1 Pt MnO4. - est l'ion permanganate. KMnO4 est le permanganate de potassium. 2) Quel est le nombre d'oxydation du |
|
Chapitre 3 : Oxydation et Réduction – Exercices ? Corrigé
Le nombre d’oxydation du zinc dans Zn est 0 Le nombre d’oxydation du zinc dans Zn2+ est +II Le nombre d’oxydation de l’atome de zinc a augmenté de 0 à +II donc le zinc subit l’oxydation b Zn Zn2+ + 2e-c Le nombre d’oxydation de l’hydrogène diminue Il passe de +I a 0 |
|
Chapitre 3 : Oxydation et Réduction – Exercices
Le nombre d'oxydation (n o ) ou degré d'oxydation est le nombre de charges électriques réelles ou fictives que porte un élément au sein d'une espèce chimique (molécule ou ion) Il est désigné par un chiffre romain (+I -II +IV ) |
Comment calculer le nombre d’oxydation ?
Le nombre d’oxydation de l’oxygène dans un composé est ? 2. Le nombre d’oxydation de l’hydrogène dans un composé est + 1. Le nombre d’oxydation d’un halogène dans un composé est ? 1. En gardant ces règles à l’esprit, on peut déterminer les nombres d’oxydation des atomes dans divers composés.
Comment calculer le nombre d'oxydation ?
Les chimistes utilisent les règles suivantes pour déterminer un nombre d'oxydation : Règle 1.~ 1. Le nombre d'oxydation d'un atome dans un corps simple élémentaire ou moléculaire est nul. Règle 2.~ 2. Dans le cas d'ions monoatomiques (constitués d'un seul type d'atome), le nombre d'oxydation de l'atome est égal à la charge de l'ion. Règle 3.~ 3.
Quel est le nombre d’oxydation d’un métal alcalin ?
Le nombre d’oxydation d’un métal alcalin (groupe 1) dans un composé est + 1. Le nombre d’oxydation d’un métal alcalino-terreux (groupe 2) dans un composé est + 2. Le nombre d’oxydation de l’oxygène dans un composé est ? 2. Le nombre d’oxydation de l’hydrogène dans un composé est + 1.
Quels sont les règles régissant les nombres d’oxydation de divers éléments sous différentes formes ?
Il existe de nombreuses règles régissant les nombres d’oxydation de divers éléments sous différentes formes. Voici trois règles que nous avons abordées jusqu’à présent : Le nombre d’oxydation d’un atome ou d’une molécule sous sa forme élémentaire est zéro. Le nombre d’oxydation d’un métal alcalino-terreux dans un composé est + 2.
Quel est le nombre d'oxydation de MnO4 ?
. Les atomes de manganèse y sont au degré d'oxydation +VII, si bien que son nom selon l'IUPAC est manganate (VII) de potassium.
Comment déterminer le nombre d'oxydation ?
|
Rappel de 1ère année sur les nombres doxydation
Le nombre d'oxydation d'un élément chimique dans un édifice mono ou MnO4 - + 5e- + 8H+ ⇔ Mn2+ + 4 H2O (1) Equilibre rédox (2) Equilibre des charges |
|
Nombre doxydation - Zeste de Savoir
15 jan 2019 · Un nombre d'oxydation s'affecte à un élément chimique seulement Nous ne pouvons pas Couple n°1 KMnO4/MnO2 Alors, dans le cas de |
|
Télécharger le support de cours en Pdf - Oxydo-réduction et pile
électrons est appelée oxydant nombre d'électrons transférés pour cet atome électrons Le permanganate est donc un oxydant MnO4 - → Mn2+ MnO4 |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
doit céder autant d'électrons qu'il n'y en a de capter par l'oxydant) trouvées de part et d'autre de la flèche en ne les faisant apparaître que du côté où il y en a le plus grand nombre ex : couple du permanganate en milieu acide MnO4 |
|
Devoir Surveillé n° 6 Option PSI
24 mai 2018 · 4) Déduire de la question 1) le nombre d'oxydation maximal de l'élément cérium Mn(OH)2(s) ainsi que les ions en solution Mn2+ et MnO4 - |
|
Oxydoréduction : pile et titrage
13 avr 2017 · 2) Écrire la demi-équation électronique relative au couple MnO4 -/Mn2+ 0,5 Pt A l'anode, il y a oxydation du dihydrogène : H2(g) = 2H+ + 2e- 7) Quel est le nombre minimal de cellules, d'une surface efficace de 250 cm2, |
|
Titrage des ions fer II par les ions permanganate
Solution de permanganate de potassium K+(aq) + MnO4 -(aq) Concentration [ MnO4 -] Volume équivalent Véq à déterminer ? Solution acidifiée de sel de Mohr |
|
Chapitre 4 Oxydo-réduction
Couple oxydant / réducteur et demi-équation électronique et l'ion manganèse ( II) Mn2+ forment un couple oxydant / réducteur noté MnO4 Le nombre d' électrons libérés, lors du passage de l'aluminium Al(s) aux ions Al3+(aq), doit être |
|
Cl
Que vaut le nombre d'oxydation des éléments dans les composés suivants ? Fe : 0 S8 : 0 multiplier les 5 CO2 par 2 donnant 10 CO2, ainsi que le MnO4 |
|
Oxydoreduction - Lycée Ismael Dauphin
MnO4 - (aq) / MnO2(s) (en milieu acide) Exercice 5 : Ecrire les couples oxydant / réducteur relatifs aux demi-équations d'oxydoréduction suivantes: H2(g) |