comment calculer le ph d'une solution
|
Calculs de pH
Nous allons dans ce chapitre voir comment il est possible de calculer à priori le pH d'une solution aqueuse Le calcul exact du pH est toujours possible mais il |
|
PH dune solution aqueuse
Calculer le pH des solutions d'HCl dont les concentrations sont les suivantes : - c = 02 mol /L : |
|
PH DES SOLUTIONS AQUEUSES I Généralités
Équations de pH des solutions simples 1 DÉMARCHE UTILISÉE POUR CALCULER LE pH : ✓ Établir les réactions de dissociation ✓ Ecrire l'équilibre de l'eau |
|
PH des solutions aqueuses simples (Aspect quantitatif)
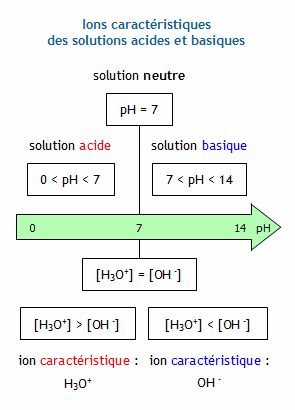
Le pH d'une solution aqueuse est : Acide : [H3O+]> [OH-] : pH< ½ pKe Neutre : [H3O+]= [OH-] : pH = ½pKe Basique : [H3O+] < [OH-] : pH |
|
PH DES SOLUTIONS AQUEUSES
2- Calcul du pH : On considère un mélange d'acide faible HA de concentration CA et de base conjuguée de concentration CB HA + H2O A - + H3O + (ionisation |
|
VIEtude sommaire des mélanges
Calculer les pH des solutions aqueuses suivantes: a) solution 0050 M en CH3COOH et 0050 M en CH3COONa b) solution 0150 M en HCOOH et 0250 M en HCOONa c |
Comment calculer le pH d'une solution exemple ?
Le pH d'une solution est lié à la concentration en quantité de matière d'ions oxonium.
Les relations entre le pH et la concentration en quantité de matière d'ions oxonium sont pH = –log[H3O+] et [H3O+] = 10–pH.Quelle est la formule pour calculer le pH d'une solution ?
Pour calculer le pH d'une solution d'acide fort, on peut utiliser la relation "pH = -log[H₃O⁺]" en considérant que la conversion de l'acide est totale.
Pour une solution basique de concentration en ions hydroxyde donnée, on peut calculer le pH en utilisant le pOH ("pOH = -log[OH⁻]") et la relation "pH = 14 - pOH".Comment calculer le pH après dilution ?
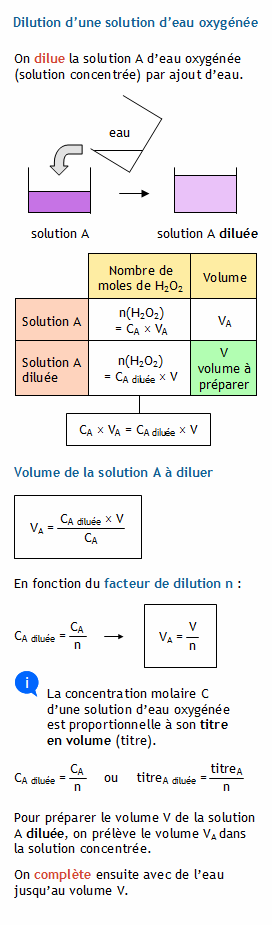
Quand on dilue cet acide 10 fois, son pH devient : pH' = – logC', avec C' = C/10 pH' = – log C/10 = – log C + log10 = – log C + 1 = pH + 1.
Quand on dilue 10 fois un acide fort, son pH augmente d'une unité ».- Calculer le pH d' une solution aqueuse d' hydroxyde de sodium de concentration C égale à 0,1 mol.
L-1.
On applique la formule précédente : pH = 14 + log10-1.
- Pour un acide fort : pH = - log C.
- Pour une base forte: pH = 14 + log C. Ces formules sont valables pour les concentrations supérieures à 10-7 mol/L.
- Pour un acide faible : pH = 1/2 pKa - 1/2log C.
- Pour une base faible : pH = 7 + 1/2 pKa + 1/2log C. ...
- pH = 1/2( pKa
Quelle est la formule du pH ?
Comment calculer le pH d'une solution à partir d'une concentration ?
. Si on nous demande de calculer la concentration en quantité de matière d'ions oxonium, il faut utiliser la relation [H3O+] = 10–pH.
Comment calculer le pH d'une solution diluée ?
Comment calculer le pH initial ?
. Le nouveau pH sera : pH = pKa – log ( 1.1 / 0.9 ) = 4.75 – 0.09 = 4.66 Le pH n'aura varié que de 0.09 unité.
|
Chimie
B Calcul de la concentration à partir des grandeurs physiques de la solution expliquons comment planifier la préparation des solutions, en illustrant |
|
Préparation dune solution connaissant la densité de la solution m`ere
On veut préparer un volume Vf de solution de concentration Cf `a partir d'une solution commerciale de concentration Ci Il faut donc calculer le volume Vi de |
|
Chapitre 11 : Solution et concentration - Physagreg
On veut obtenir une solution fille de volume 100 mL et de concentration 0 10 mol/ L a On calcule tout d'abord, le volume de solution mère que l'on doit prélever : D |
|
Densité dun solide - Préparation dune solution - Dilution ENONCE
3- Dilution A partir d'une solution commerciale d'acide nitrique de densité d = 1, 33 et de pourcentage en a- Calculer la concentration de la solution "mère" (c) |
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
7 Calculer la concentration molaire d'une solution dont un volume de 50 mL contient 0,01 mol de substance dissoute (R : 0,2 mol/L) 8 Comment préparer 100 |
|
Quelques définitions Calculs à réaliser
Il indique la masse de l'espèce chimique dont on veut faire la solution ( soluté ) dans 100 g de liquide Exemple : Pour l'acide chlorhydrique, l'étiquette indique d = |
|
Calcul de la concentration massique dune solution - pontonniers
Calculer la concentration massique en soluté des solutions suivantes : Soluté Volume Calculer le pourcentage massique en éosine de la solution obtenue b |
|
Annales exercices_1
18 oct 2014 · Solution aqueuse d'acide chlorhydrique à 37 en masse (37g de HCl pour 3) Calculer le pH de la solution tampon et justifier le fait que cette |