ph ? l'équivalence dosage acide faible base forte
|
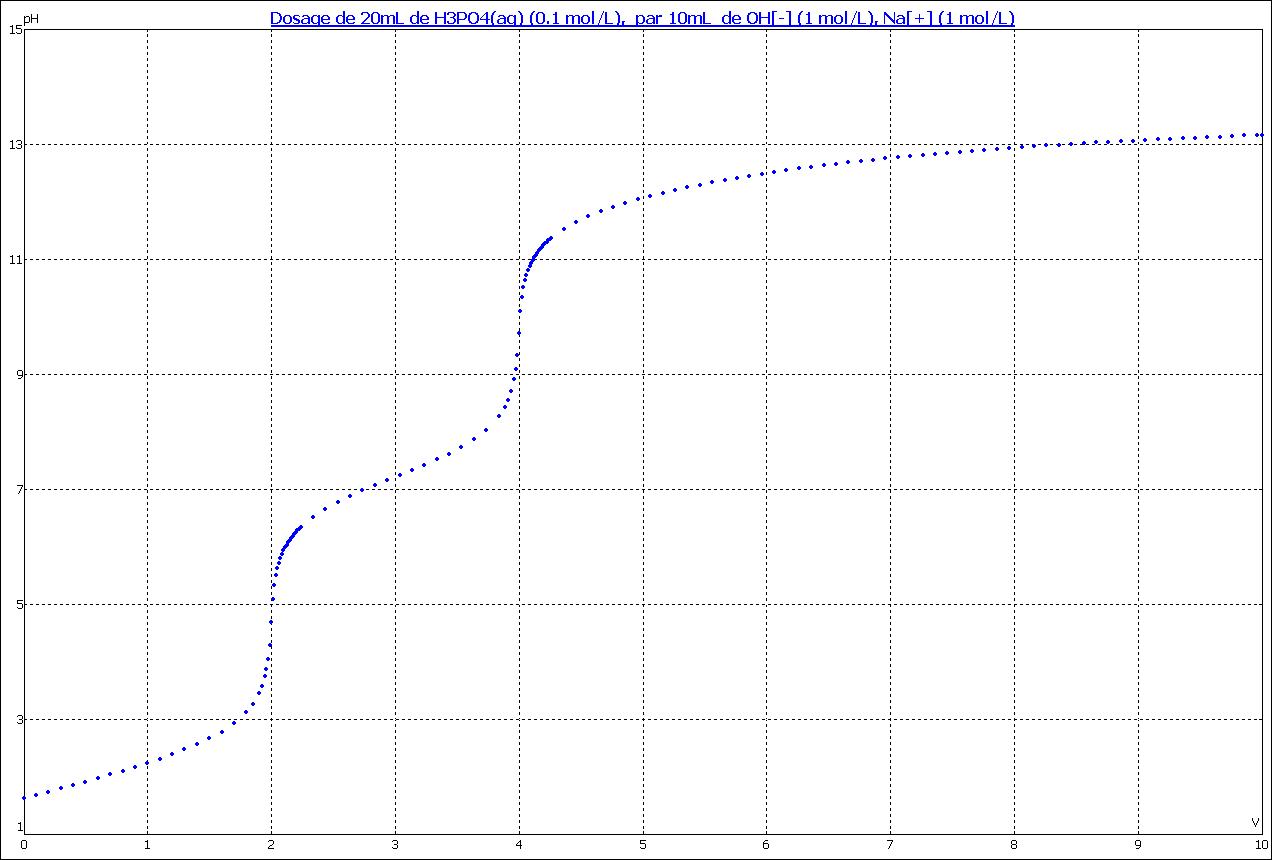
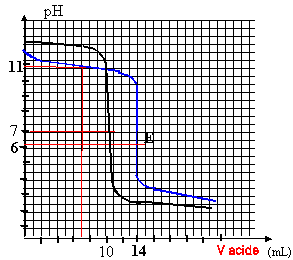
Dosage acide faible – base forte
L'équivalence acido-basique est atteinte lorsque la quantité d'ions Le saut de pH est d'autant plus important que les solutions sont concentrées et la |
|
Dosages acide-base
En effet le pH à la demi-équivalence (lorsque le volume de titrant versé correspond à la moitié du volume équivalent) est égal au pKa du couple acide faible / |
|
Dosages acidobasiques
9 fév 2018 · Quand l'acide faible est diluéi on sait qu'il se comporte comme un acide fort Son dosage présentera donc l'allure précédente mais avec un saut |
|
LES REACTIONS ACIDE-BASE 1 Le pH 11 Définition Le
Remarque : A l'équivalence du dosage d'un acide faible par une base forte le pH noté pHE est supérieur à 70 En effet à l'équivalnce il y a présence de l |
|
Dosage acide faible – base forte
?. OH. Na. NaOH . L'équation bilan de la réaction de dosage s'écrit : OH. A. OH. HA. |
|
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
Chapitre 1 Acides et bases
pH = ?log (c). La base conjuguée d'un acide fort est dite “indifférente dans l'eau” i.e. cette espèce ne 1.4.2 Évolution du pH |
|
Dosages acidobasiques
09 Feb2018 la concentration de l'acide |
|
Dosage acide fort - base forte
Etant donné la valeur du pH à l'équivalence la zone de virage de l'indicateur coloré devra contenir la valeur de. pH=7. La précision du dosage est d'autant |
|
LES REACTIONS ACIDE-BASE 1. Le pH 1.1 Définition Le pH
Remarque : A l'équivalence du dosage d'un acide fort par une base forte le pH noté pHE est de 70. 7.3.4 Repérage de l'équivalence a) A partir de la courbe |
|
Solutions tampons
Avant l'équivalence lors du dosage d'un acide faible par une base forte le pH est donné par la relation suivante (voir dosage acide faible - base forte):. |
|
Dosage acide faible-base forte
Dosage acide faible – base forte L'équivalence acido-basique est atteinte lorsque la quantité d'ions hydroxyde OH- versée est égale à la quantité. |
|
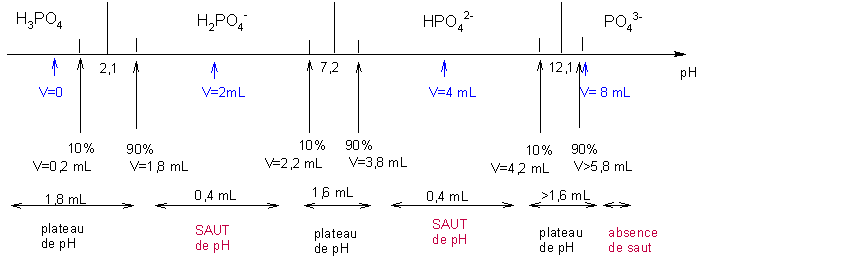
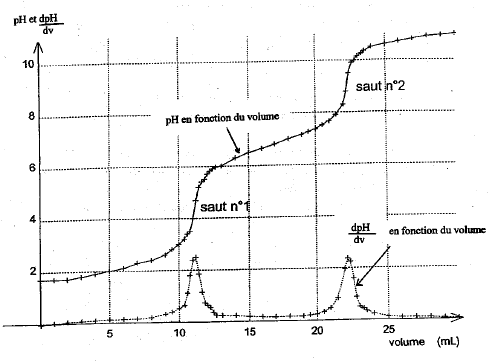
Dosage diacide faible – base forte
?. OH. Na. NaOH . Dans le cas du dosage d'un diacide H2A |
|
XI. DOSAGES 1. Réaction Elle doit être totale instantanée et
Dosage acide fort / base forte noté AF / BF. Dosage acide faible / base forte noté Af / BF. Comparaisons : - Le saut de pH à l'équivalence est plus |
|
Dosage triacide faible – base forte - Le Mans University
pH lors du dosage d’un triacide faible il faudrait que les trois valeurs de pKa ne soient pas trop proches l’une de l’autre et que la troisième acidité ne soit pas trop faible Triacide faible H 3 A constantes d’acidité K a1 K a2 et K a3 |
|
Les solutions tampons - Le Mans University
Avant l’équivalence lors du dosage d’un acide faible par une base forte le pH est donné par la relation suivante (voir dosage acide faible - base forte): 1 x x pK log c v c v c v pH pK log a a a b b b a La concentration en ions sodium dans le cas d’un dosage par la soude s’écrit : b1 a b a a a b b b c v v xc v v v c v Na |
|
Dosage acido-basique - Archiveorg
De plus à l’équivalence du dosage d’un acide fort par une base forte [H3O+] = [HO-] c’est à dire pHE = 70 à 25°C A l’équivalence la solution résultant du mélange d’acide chlorhydrique et de soude est donc une solution de chlorure de sodium ! 5 Allure de la courbe de dosage pH-métrique |
Comment calculer le pH d’un acide faible ?
Nous allons voir que celui-ci n’est qu’une solution approchée du problème. Avant l’équivalence lors du dosage d’un acide faible par une base forte, le pH est donné par la relation suivante (voir dosage acide faible - base forte): 1x x pK log c v c v c v pH pK loga a a b b b a? ? ? ? ? ?
Quelle est la différence entre un acide faible et une base forte ?
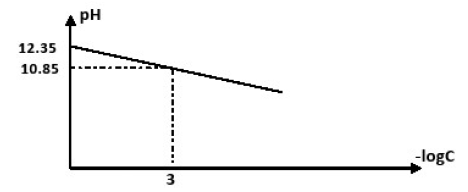
Par contre, lors du dosage d’un acide faible, on peut constater (voir dosage acide faible - base forte) qu’au voisinage de x=0,5 le pH varie peu et dépend peu de la concentration.
Comment doser un acide faible ?
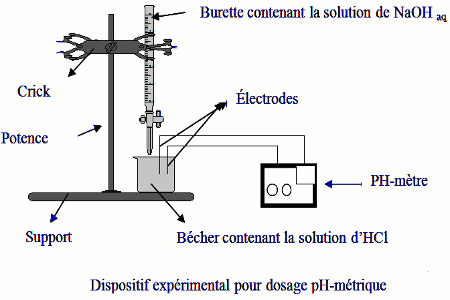
DOSAGE D’UN ACIDE FAIBLE - leçon n° 6 Cette leçon comporte trois paragraphes. 1- LA REACTION ACIDE FAIBLE - BASE FORTE On raisonnera sur l’exemple d’une solution d’acide éthanoïque dosée par une solution de soude. 1.1 Le montage. La solution d’acide faible à doser est mise dans le bécher. La solution de base forte est dans la burette graduée.
Comment mesurer le pH d'une solution d'acide faible ?
La solution d’acide faible à doser est mise dans le bécher. La solution de base forte est dans la burette graduée. Un pH-mètre, étalonné, permet de mesurer le pH après chaque ajout de soude. 1.2Equation de la réaction. Sur l'échelle des pKa (aide mémoire :O.R.B.A) on encadre les espèces chimiques initialement présentes en quantiténotable: