calcul concentration h3o+ avec ph
|
Calculs de pH
Notons h la concentration des ions H3O+ et ω la concen- tration des ions OH− Saint Joseph - LaSalle CPGE TSI Page 2 P hysique |
|
CHAP 13-ACT EXP Mesures de pH
D'où le pH : pH = 2 c) – Grace au pH que vous avez mesuré dans le 5 1 - Calculer la concentration noté [H3O+ (aq)]f puis le nombre de moles d'ions oxonium nf( |
|
Déterminer la valeur dun pH
Il faut appliquer la relation pH = -log[H3O+] ( Attention sur la calculatrice il faut utiliser la touche log et non la touche ln ( log népérien comme en |
|
Exercice 2 : « Concentration en soluté et pH »
Le pH de la solution est de 12 1 Calculer la concentration en ion oxonium H3O+ [H3O+]= 10 –pH ; [H3O+]= |
|
Log [H3O+] [H3O+] = 10-pH τ = xf / xmax
pH est bas La relation liant le pH à la concentration en ions oxonium est : Inversement : pH = - log [H3O+] [H3O+] = 10-pH [H3O+]est la concentration |
|
PH et pKa
pH = 14 + log [B] 8 Calcul de pH Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + [OH-]) / ([A-] + [H3O+] - [OH-])) |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide ou d'une base en solution est suffisamment grande la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH– |
Comment calculer la concentration en H3O+ avec le pH ?
Si on nous demande de calculer le pH, il faut utiliser la relation pH = –log([H3O+]).
Si on nous demande de calculer la concentration en quantité de matière d'ions oxonium, il faut utiliser la relation [H3O+] = 10–pH.Comment calculer la concentration de H3O ?
L-1 : aH3O+ = [H3O+] / c° ou encore, aH3O+ = valeur de la concentration en ions H3O+ exprimée en mol.
L-1 , l'activité n'ayant pas de dimension (contrairement à la concentration ).Comment calculer une concentration à partir d'un pH ?
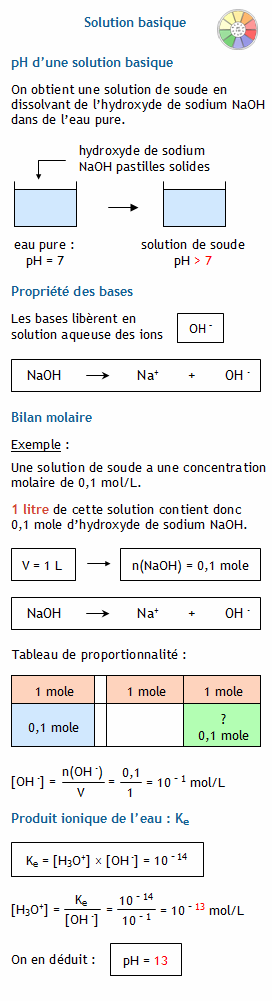
Pour une solution basique de concentration en ions hydroxyde donnée, on peut calculer le pH en utilisant le pOH ("pOH = -log[OH⁻]") et la relation "pH = 14 - pOH".
La fonction logarithmique associée au pH est "f(x) = -log(x)".- Pour trouver la concentration en ions hydronium pour répondre à cette question, nous devons trouver la racine carrée de 3,6 fois 10 puissance moins six.
En utilisant une calculatrice, la valeur numérique pour cette opération de racine carrée est d'environ 1,8973 fois 10 puissance moins trois.
|
Acides et Bases en solution aqueuse
[H3O+] = 10-5 mol/L; déterminer son pH. 3. La mesure du pH du coca-cola donne 27 |
|
Valeur du pH
➢ Si on a une solution acide on connaît [H3O+]; La formule s'applique directement. ➢ Si on a une solution basique |
|
Untitled
Une solution de pH= 3 est une solution acide dont la concentration molaire en ions H3O* est [H3O+]= 10³ mol.L¨¹. II. Théorie de Bronsted des acides et des |
|
CORRIGE
- Mesurer le pH de l'eau distillée avec le pH-mètre. - Avec c) – Grace au pH que vous avez mesuré dans le 4.1. - Calculer la concentration noté [H3O+. |
|
Log [H3O+] [H3O+] = 10-pH τ = xf / xmax
La relation liant le pH à la concentration en ions oxonium est : Connaissant σ on peut calculer [ H3O+ ]f et alors on peut calculer normalement le taux d' ... |
|
PH et pKa
pH = 14 + log [B]. 8. Calcul de pH. Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka.(([AH] - [H3O+] + [OH-]) / ([A-] + [H3O+] - [OH-])). |
|
Untitled
Une solution de pH= 3 est une solution acide dont la concentration molaire en Q1/Calculer la concentration en ions H3O+. Q2/L'acide benzoïque est-il un ... |
|
Chapitre 1 Acides et bases
L−1 et comme indiqué dans la note pré- liminaire la concentration unitaire C0 est omise. Une solution aqueuse est dite : — neutre si son pH vaut 7 |
|
Exercice 2 : « Concentration en soluté et pH ».
concentration molaire est de 125.10-2 mol / L. 4. Le pH de la solution est de 12 |
|
Coefficient de dissociation dun acide
C0 : concentration initiale de l'acide avant sa réaction avec l'eau. ▫ On rappelle que la concentration [H3O+] est liée au pH de la solution par la relation. |
|
Acides et Bases en solution aqueuse
Si une solution a une concentration en [H3O+] = 10-5 mol/L; déterminer son pH. 3. La mesure du pH du coca-cola donne 27 |
|
Chapitre 1 Acides et bases
liminaire la concentration unitaire C0 est omise. Une solution aqueuse est dite : — neutre si son pH vaut 7 i.e. [H3O+]= 10?7 mol.L?1 (à 25?C) ;. |
|
CORRECTION EXERCICE C9
Cette méthode est plus longue qu'avec un pH-mètre elle est moins précise et ne La concentration molaire en ions oxonium H3O+ vaut [H3O+] = 10-3 |
|
CORRIGE
Mesurer le pH de l'eau distillée avec le pH-mètre. Oui car le pH varie b) Calculer les concentrations [H3O+ ... En déduire la concentration en ions H3O+. |
|
Untitled
La concentration en ions oxonium de la boisson est [H3O+] = 32 mmol · L-¹. avec cº = 1 mol · L-1 cº. Écriture de la définition du pH. |
|
PH = - log [H3O+] [H3O+] = 10-pH ? = xf / xmax
La relation liant le pH à la concentration en ions oxonium est : Connaissant ? on peut calculer [ H3O+ ]f et alors on peut calculer normalement le taux ... |
|
PH et pKa
3 unités de pH = facteur 1000 [H3O+] de même concentration d'un acide faible. ([HCl] 0.1 M pH ... pH d'un mélange d'acide faible avec sa base conjuguée. |
|
Coefficient de dissociation dun acide
C0 : concentration initiale de l'acide avant sa réaction avec l'eau. ? On rappelle que la concentration [H3O+] est liée au pH de la solution par la |
Vue d’ensemble
Dans la vie quotidienne, le pH est une échelle de mesure souvent utilisée pour décrire la neutralité ou l'absence de neutralité dans les éléments d'usage courant. En sciences, le pH est la mesure d'ions dans une solution. Si vous prenez ou suivez un cours de sciences ou de chimie, vous devrez savoir comment calculer le pH basé sur la concentration ...
Comprendre ce que c'est que le pH
Sachez ce que c'est que le pH. Le pH est la concentration en ions d'hydrogène présents dans une solution. Une solution avec une grande concentration d'ions d'hydrogène est considérée comme acide et une solution avec une faible quantité d'ions d'hydrogène est considérée comme basique ou alcaline
Utiliser la concentration pour calculer le pH
Souvenez-vous de l'équation du pH. L'équation du pH est la suivante : pH = -log [H3O
How do you calculate the concentration of hydroxide ions?
If you already know pH, but want to calculate the concentration of ions, use this transformed pH equation: [H +] = 10 -pH. There also exists a pOH scale - which is less popular than the pH scale. pOH is the negative of the logarithm of the hydroxide ion concentration: pOH = -log ( [OH?]), or [OH -] = 10 -pOH.
What is the unit for the concentration of hydrogen ions?
The unit for the concentration of hydrogen ions is moles per liter. To determine pH, you can use this pH to H? formula: pH = -log ( [H?]) If you already know pH, but want to calculate the concentration of ions, use this transformed pH equation: [H +] = 10 -pH.
What is the formula for pH to H +?
The pH to H + formula that represents this relation is: pH = -log([H +]) The solution is acidic if its pH is less than 7. If the pH is higher than that number, the solution is basic, as known as alkaline. Solutions with a pH equal to 7 are neutral. Apart from the mathematical way of determining pH, you can also use pH indicators.
What is the pH of a solution?
The pH scale (pH) is a numeric scale used to define how acidic or basic an aqueous solution is. It commonly ranges between 0 and 14 but can go beyond these values if sufficiently acidic/basic. The pH value is logarithmically and is inversely related to the concentration of hydrogen ions in a solution.
Past day
Comment calculer la concentration d'une solution pH ?
Quelle est la relation entre H3O+ et le pH d'une solution aqueuse ?
Comment calculer la concentration de OH avec pH ?
. Il faut calculer [H3O+] par la relation [H3O+]x[HO-]=10-14 d'ou [H3O+] = 10-14 [HO-] Puis, on applique la formule.
|
CORRECTION EXERCICE C9 - Sciences Physiques et Chimiques
A partir de la valeur de pH mesurée, on trouve : [H3O+] = 10-3,4 = 4,0 10-4 mol Lorsqu'on dilue la solution, la concentration en ions oxonium diminue et celle La formule de l'espèce conjuguée de cette amine est l'ion trimethylammonium |
|
Télécharger le support de cours en Pdf - Chimie Générale et
voit donc que la somme du pKa et du pKb concentrations en ions H3O+ et OH- possible d'obtenir des valeurs approchées de pH par le calcul à l'aide de |
|
[H3O ] = 10
Puis, connaissant [H3O+], on va déterminer la [HO-] par la relation [H3O + ] Application Déterminer la concentration en ions oxonium et en ion hydroxyde |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 Cas d'un acide 2 5 Cas d 'un mélange d'un acide fort et d'un acide faible Soit 1 litre d'une solution de H2SO4 de concentration 0,25 mol L-1 à 25°C, l'ion H+ vient se lier : A- + H+ |
|
CORRIGE - Meck-anique
Avec précaution, ajouter quelques gouttes d'acide éthanoïque pur - Agiter b) Calculer les concentrations [H3O+ En déduire la concentration en ions H3O+ |
|
IIILeau
permet donc de calculer la concentration formelle de l'eau dans l'eau pure: mol H3O + et 10 -7 mol OH - Il restera 55,36-0,0000002 moles H2O non |
|
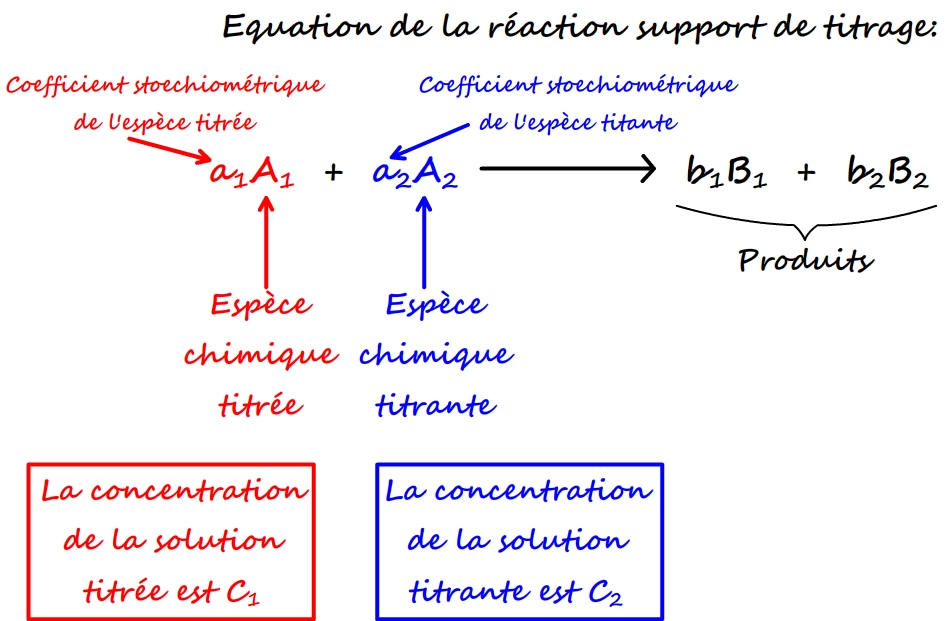
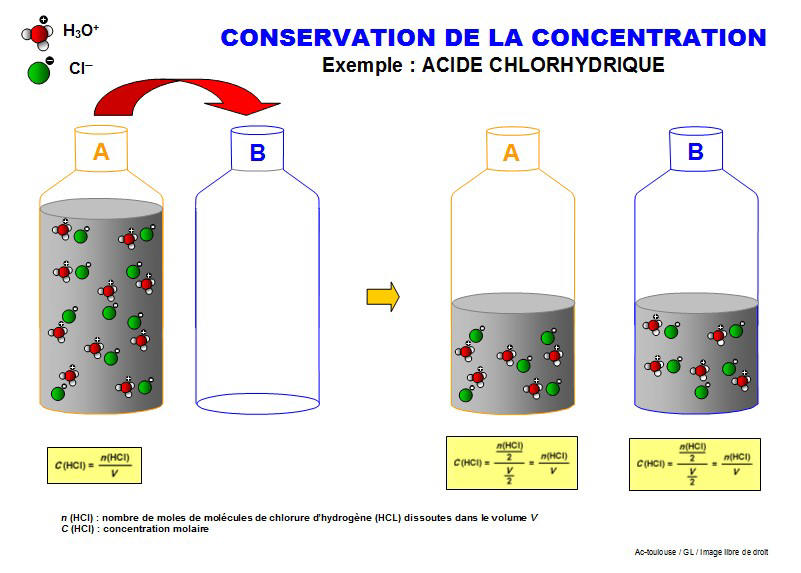
Détermination de la concentration dune solution par titrage - Jeulin
La quantité d'ions oxonium dosés est donc : n(H3O+) = CbVbE A volume constant la conductivité A l'équivalence, seuls les ions Na+ et Cl- sont présents Calcul de la concentration de la solution d'acide chlorhydrique : Ca = Cb Vb/ Va |
|
Acides et Bases en solution aqueuse
La mesure du pH du coca-cola donne 2,7, calculer la concentration en ions H3O+ 4 Quels sont le pH et le caractère d'une solution si [ OH- ] = 0,00002 mol - 1 ? |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
2) Comparer la liste d'espèces avec la donnée et déterminer le nombre n la contribution de l'autoprotolyse de l'eau à la concentration en H3O+ ou OH– |