formule de rydberg exemple
|
Etude théorique et expérimentale des atomes de Rydberg circulaires
9 mar 2006 · exemple avec le moment angulaire L d'une particule et nous avons formule très analogue que nous avons redémontrée au § I B 4 a équ (I B |
|
Les atomes
Chapitre 2 : Spectre des Hydrogénoïdes et Modèle de BOHR Cette page est mise à Formule empirique de Balmer-Rydberg Rydberg : σ = 1 / λ = R H (1/22-1/n2) |
|
SPECTRE DE RAIES ET LA CONSTANTE DE RYDBERG
Par exemple la lumière émanant d'un tube à gaz à hydrogène est rosée résultat de la raie spectrale très intense de longueur d'onde λ = 6561 nm L'espacement |
Comment déterminer la constante de Rydberg ?
constante de Rydberg: RH = 109680 cm−1. (ν est un nombre d'onde.) RH = Ry hc .
Quel est la constante de Rydberg pour l'hydrogène ?
où R est la constante de Rydberg, avec une valeur de 1,097 x 107 m-1. 1 Spectre visible de l'hydrogène. est la différence d'énergie entre le niveau initial et le niveau final, ni et nf, h = 6,63 x 10 -34 J.s = 4,14 x 10 -15eV.
Comment utiliser la formule de Ritz ?
On utilise la formule de Ritz : - pour la série de Lyman n1 = 1 (l'électron revient au niveau 1) et n2 varie de 2 (première raie) à l'∞ (dernière raie). pour n2 = 3 on obtient : 1 / λ = RH (1 / 12 - 1 / 32) soit λ = 102,5 nm
- Le rayon de Bohr est une constante physique égale à la distance entre le noyau et l'électron d'un atome d'hydrogène à l'état fondamental.
Sa valeur est donnée par la formule ��₀ = 4����₀(ℎ barre)²/��_e (��_e)².
|
SPECTRE DE RAIES ET LA CONSTANTE DE RYDBERG
Par exemple la lumière émanant d'un tube à gaz à hydrogène est rosée résultat de la raie spectrale très intense de longueur d'onde ? = 656 |
|
Chap. II : Les spectres atomiques
Constante de Rydberg. Série de Balmer : p entier > 2 Formule de Ritz ... L'élaboration d'une théorie nécessite le choix d'un modèle. |
|
Chapitre 10: Atome de Bohr
Cette formule que Johannes Robert. Rydberg généralisa en 1890 |
|
Le test de flamme
La formule de Rydberg peut être généralisée à tout ion b) Expliquer sur un exemple [H : 1 -> 2] le calcul réalisé dans la colonne « Variation d'énergie ... |
|
Exercice n°1 : (8 points) Ici absorption de ? à partir du niveau n=2
Formule de Ritz-?Balmer pour un ion hydrogénoïde : Ici absorption de ? à partir du niveau n=2 donc Donner un exemple. (1 pt). |
|
Interactions entre atomes de rubidium dans des états de Rydberg et
Dec 5 2011 l'efficacité du blocage de Rydberg |
|
Mesure de la constante de Rydberg par spectroscopie à deux
Mar 9 2006 l'hydrogène autant que les formules de Balmer et de Rydberg pouvaient le ... exemple |
|
Expérience de Balmer - Rydberg
Balmer - Rydberg. PrinciPe : quelques valeurs discrètes appelées niveaux d'énergie (modèle de Bohr). ... prévues par la formule de Rydberg-. |
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Lyman (UV) Balmer (Visible) |
|
Untitled
Que permet alors de calculer la formule de Rydberg ? (COM). Les paramètres n1 et n2 ne sont pas explicitement interprétés dans le doc 3. Réponse attendue: lien |
|
Le Expérience 9 - Cégep de Sainte-Foy
spectre de l'hydrogène pouvaient être déterminées par une formule empirique dans laquelle on retrouvait la constante de Rydberg Dans cette expérience des raies spectrales seront observées et la relation entre la constante empirique de Rydberg et les paramètres physiques théoriques découlant du modèle de Bohr sera analysée |
|
1 Exercice (sur 7 points) : ´etats de Rydberg d’un atome - ENS
1 3 On peut ´egalement pr´eparer d’autres esp`eces atomiques dans des ´etats de Rydberg Par exemple dans le cas du sodium (masse atomique A = 23 nombre d’´electrons Z = 11) on peut placer l’´electron de valence dans un ´etat tr`es excit´e les 10 ´electrons de cœur restant au voisinage du noyau S’attend-on a une di? |
|
Searches related to formule de rydberg exemple PDF
Formule empirique de Balmer-Rydberg Rydberg : ? = 1 / ? = RH(1/22-1/n2) Balmer : ? = B n2 / n2 - 4 où n est un entier égal à 3 4 5 ou 6 et B une constante où ? est le nombre d'onde et RH la constante de Rydberg associée à l'hydrogène RH = 1096 107 m-1 Cette formule empirique fut ensuite généralisée en ? = 1 / ? = RH (1/n2 |
Qu'est-ce que la formule de Rydberg ?
La formule de Rydberg est une formule mathématique utilisée pour prédire la longueur d' ondede la lumière résultant d'un électron se déplaçant entre les niveaux d'énergie d'un atome. Lorsqu'un électron passe d'une orbitale atomique à une autre, l'énergie de l'électron change.
Qu'est-ce que la constante de Rydberg de l'hydrogène?
est la constante de Rydberg de l' hydrogène. et sont des entiers tels que . En fixant et avec allant de 2 à l'infini, les raies spectrales connues sous le nom de série de Lyman convergeant vers 91 nm sont obtenues par la même méthode :
Où se trouve le Feldberg ?
Le Feldberg se trouve dans le parc naturel du Haut-Taunus, sur le territoire de la commune de Schmitten dans l' arrondissement du Haut-Taunus. Il est situé au nord de la ville de Königstein . Le plateau du Feldberg est constitué en de nombreux endroits d'un quartz typique du Haut-Taunus.
Comment calculer la formule empirique de Balmer-Rydberg ?
Formule empirique de Balmer-Rydberg. Rydberg : ? = 1 / ? = RH(1/22-1/n2) Balmer : ? = B n2 / n2 - 4. où n est un entier égal à 3, 4, 5 ou 6, et B une constante. où ? est le nombre d'onde et RH la constante de Rydberg associée à l'hydrogène.
Comment calculer la constante de Rydberg ?
C'est quoi un spectre atomique ?
Qu'est-ce qu'un ion hydrogénoïde ?
. La résolution de l'équation de Schr?inger permet de décrire rigoureusement les états quantiques de cet électron unique que l'on dénomme orbitales atomiques.
|
Spectre
Constante de Rydberg Série de Balmer : Formule de Ritz La relation de L' élaboration d'une théorie nécessite le choix d'un modèle On représente le |
|
Vers une mesure directe de la constante de Rydberg en unit
9 mar 2006 · présentation la plus connue du Modèle de Bohr, ne figure en fait que C'est l'un des aspects du "Principe de Correspondance", formulé par |
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
La position de toutes les raies s'obtient par une formule simple, la formule de Rydberg-Ritz : │ ⎠ constante de Rydberg Remarque : A) Modèle planétaire |
|
Expérience de Balmer - Rydberg - DIDALAB
à l'aide d'un spectromètre et retrouver par calculs la constante de Rydberg Équipement nécessaire quelques valeurs discrètes, appelées niveaux d' énergie (modèle de Bohr) Lorsque prévues par la formule de Rydberg- Ritz : Les raies |
|
Vers une mesure directe de la constante de Rydberg en - HAL-Inria
9 mar 2006 · présentation la plus connue du Modèle de Bohr, ne figure en fait que C'est l'un des aspects du "Principe de Correspondance", formulé par |
|
SM2 Structure électronique des atomes - I / Optique
La formule de Ritz-Rydberg permet donc d'écrire : Em − En Niels Bohr avait proposé un modèle planétaire de l'atome d'hydrogène où l'électron ne pouvait |
|
Atome dhydrogène et hydrogénoïdes
plus grandes que celles de l'hydrogène: par exemple la transition n = 2−n = approximativement la formule Eq 5 13 dite "de Rydberg" pour l'atome d'hy- |
|
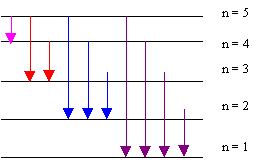
Chapitre 10: Atome de Bohr
Formule de Balmer – Rydberg: │ Modèle de Bohr : étude des orbites de l' atome H continuelle d'énergie de l'électron accéléré, Bohr, dans son modèle, eut |



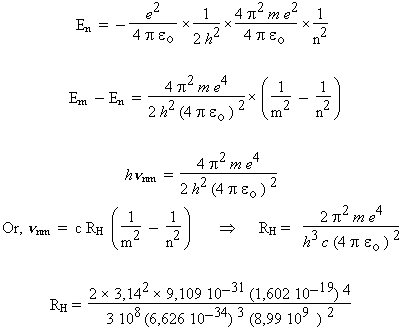




















 Atome De Bohr By Exo Supcom - telechargez pdf PDF](+1????️) Atome De Bohr By Exo Supcom - telechargez pdf](http://www.chimie-briere.com/CHIMIE110L1/ATOL1TD0506/serie_2/Image29.gif)