comptons les molecules ! 2nde Physique
|
Chapitre 8 : Les molécules
Une molécule est une entité chimique électriquement neutre formée par un nombre précis d'atomes A chaque molécule on associe un nom et une formule brute Dans la formule brute on écrit les symboles des éléments et en indices en bas à droite pour chaque élément le nombre d'atomes Ex : Cl2 ; HCl ; CH4 ; NH3 ; CO2 ; C2H6 |
Quelle est la différence entre les deux molécules ?
2)- Justifier la différence de leurs propriétés chimiques. - Les deux molécules ont la même formule brute. - Ce sont des molécules isomères. - Des isomères sont des molécules distinctes qui possèdent des propriétés chimiques différentes. V- Exercice 7 : Lire une étiquette de médicament.
Comment décrire une molécule ?
La molécule peut être décrite par son modèle moléculaire ou sa formule développée : 1)- À partir de sa formule développée, écrire la formule semi-développée de la molécule de pseudoéphédrine. 2)- Repérer, dans le modèle moléculaire, les atomes de la molécule, lorsque c’est possible. IV- Exercice 6 : Interpréter des propriétés chimiques.
Comment répartir les doublets d’une molécule ?
Répartir les doublets de la molécule en doublets liants et non liants en respectant les règles du duet et de l’octet. Exemple 2 : la molécule d’eau La molécule d’eau a pour formule brute H2O. Chaque atome d’hydrogène a besoin d’échanger 1 liaison cova- lente, l’atome d’oxygène a besoin d’échanger 2 liaisons covalentes.
Quelle est la masse des atomes ?
Masse des atomes : m(H) = 1,674×10−24g m(C) = 1,995×10−23g m(O) = 2,657×10−23g m(Na) = 3,818×10−23g Nombre d’Avogadro : N A= 6,022×1023mol Exercice 6 On souhaite pr´elever 2.4 mol de glucose de formule brute C 6H 12O 6. Combien de gramme de poudre doit-on peser lors du pr´el`evement?
Définition
Une substance constituée d’une seule espèce chimique est un corps pur. Une substance constitué de plusieurs espèces chimiques est un mélange. Un mélange est homogène si on ne peut pas distinguer ses constituants à l’œil nu ; dans le cas contraire il est hétérogène. sbb169ee77282477c.jimcontent.com
6 Chromatographie sur couche mince
Une chromatographie sur couche mince (CCM) permet de séparer et d’identifier les différentes espéces chimiques présentes dans un mé-lange homogène. Un éluant monte par capillarité le long d’une plaque recouverte de si-lice et entraîne avec lui des espéces chimiques préalablement déposées sur la plaque. Plus une espéce chimique est soluble dans l’él
Qu’appelle-t-on rapport frontal d’une espèce chimique ?
Il permet de comparer la hauteur de progression d’une espéce chimique avec la hauteur de l’éluant : (cm) (sans unité) sbb169ee77282477c.jimcontent.com
RB h
= H (cm) M front de l’éluant H h M Une fois la substance extraite il faut l’analyser pour en déterminer sa composition. sbb169ee77282477c.jimcontent.com
La chromatographie permet
de séparer puis d’identifier les espèces chimiques d’un mélange. On trace sur une plaque (feuille de papier généralement) un trait à 1 cm du bord appelé ligne de dépôt. La plaque correspond à la phase stationnaire On dépose sur le trait une goutte de substance A à analyser et une ou plusieurs gouttes de substances connues notées B, C etc.. On plong
Composition d’un mélange
Donner la composition d’un mélange consiste à donner une information (volume, masse, proportion, etc.) relative à chacune des espèces chimique pures qui le compose. sbb169ee77282477c.jimcontent.com
I Notion de solution
Quand une espèce chimique (corps pur solide, liquide ou gazeux) est dissoute dans un liquide, on obtient un mélange appelé solution. L’espèce dissoute constitue le soluté, le liquide utilisé pour la dissoudre est appelé solvant. Si ce dernier est l’eau, la solution est dite aqueuse. sbb169ee77282477c.jimcontent.com
Définition
On appelle solution, le résultat de la dissolution d’un soluté dans un solvant. Selon la structure du soluté, une solution peut contenir des molécules ou des ions. Ces dernières sont donc conductrices du courant électrique. 1 Concentration massique Cm en soluté. Définition C’est la masse de soluté exprimée en gramme par unité de volume de solution
Préparation de solutions
Par dissolution Il su t de dissoudre la masse de soluté voulue dans le volume de solvant adéquat pour obtenir la ffi solution désirée. Choisir une fiole jaugée de volume voulu. Ajouter une peu d’eau distillée dans la fiole jaugée. Verser le solide pesé dans un sabot. Rincer le sabot avec une pissette d’eau distillée. Agiter pour dissoudre le solide
Propriété
Dans le prélèvement et dans la solution fille diluée, la masse de soluté est la même : on n’ajoute que de l’eau m(mère) même masse m(fille) sbb169ee77282477c.jimcontent.com
La verrerie d’une dilution et d’une dissolution
1. La dilution Une dilution consiste à diluer une solution aqueuse (solution mère) de manière à obtenir une nouvelle solution de concentration moins élevée (solution fille). Méthode : Compléter la fiole avec de l’eau distillée jusqu’au trait de jauge en tenant compte du ménisque. sbb169ee77282477c.jimcontent.com
Définition
Facteur de dilution correspond au nombre de fois = Cm(mère) Vfille F = Cm(fille) Vmère Verser de la solution mère dans Le un facteur bécher de dilution n’a pas et prélever un volume précis de la solution mère à l’aide d’une pipette jaugée. Vider d’unité. la pipette dans une fiole jaugée du volume désiré. sbb169ee77282477c.jimcontent.com
Sur la paillasse
1 Préparation 2. La dissolution par dissolution d’un solide Une dissolution consiste à dissoudre un soluté dans un solvant. Méthode : Prélever la masse de soluté nécessaire à l’aide d’une coupelle et d’une balance. Introduire le soluté dans une fiole jaugée du volume désiré. Ajouter de l’eau distillée dans la fiole jusqu’au 2/3 et agiter jusqu’à
La verrerie d’une dilution et d’une dissolution
1. La dilution Une dilution consiste à diluer une solution aqueuse (solution mère) de manière à obtenir une nouvelle solution de concentration moins élevée (solution fille). Méthode : Verser de la solution mère dans un bécher et prélever un volume précis de la solution mère à l’aide d’une pipette jaugée. Vider la pipette dans une fiole jaugée du vo
2. La dissolution III Dosage par étalonnage
Une dissolution consiste à dissoudre un soluté dans un solvant. De nombreuses propriétés physiques des solutions, comme leur couleur ou leur masse volumique, Méthode : dé-pendent de la concentration en masse du soluté. Cette caractéristique permet de réaliser un dosage par étalonnage, Prélever c’est-à-dire la masse de de déterminer la concentrati
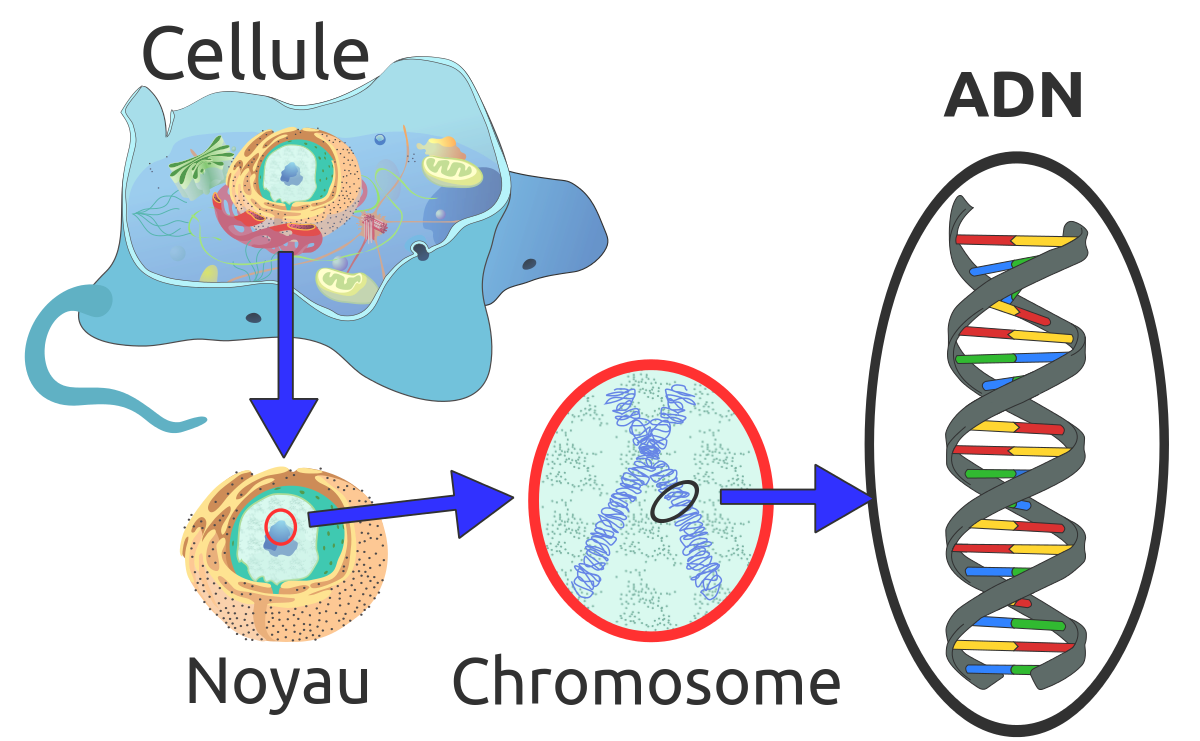
2 Le noyau
Le noyau de l’atome est constitué de particules élémentaires : les protons et les neutrons désignés sous le nom de nucléons. Pour mieux comprendre, on peut comparer le noyau à une classe : Nucléon : particule constituant du noyau. Deux sortes de nucléons (A) : Les protons (Z) Les neutrons (N = A-Z) Le noyau contient A nucléons dont Z protons et N n
Propriété
L’atome est électriquement neutre. Cela signifie qu’il y a autant de protons positifs dans le noyau que d’électrons négatifs dans le nuage électronique. sbb169ee77282477c.jimcontent.com
4 Symbole d’un atome
Un atome est symbolisé par une ou deux lettres. La première s’écrit toujours en majuscule et la seconde en minuscule. Le symbole correspond souvent au début du nom de l’atome mais certains sont issus du nom latin comme K(kalium) symbole du potassium. sbb169ee77282477c.jimcontent.com
R(atome)~R(noyau) = 10−10~10−15 = 105
Tout comme le système solaire, l’atome a une structure lacunaire. sbb169ee77282477c.jimcontent.com
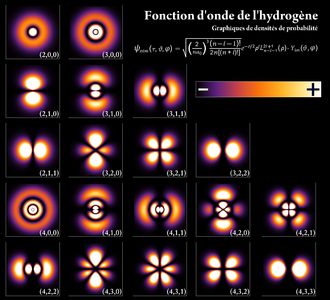
Configuration électronique d’un atome
Au cours du XX° siècle, les scientifiques ont élaboré un modèle de l’atome plus riche que le modèle de Rutherford, permettant d’interpréter la formation des ions et des molécules en précisant le rôle joué par les électrons. sbb169ee77282477c.jimcontent.com
1 Description
Le tableau périodique des éléments, également appelé table de Mendeleïev, classification périodique des éléments (CPE) ou simplement tableau périodique, représente tous les éléments chimiques, ordonnés par numéro atomique Z croissant et organisés en fonction de leur configuration électronique, laquelle sous-tend leurs propriétés chimiques. sbb169ee77282477c.jimcontent.com
Définition
Une ligne de la classification est appelée période. Une colonne est appelée famille. sbb169ee77282477c.jimcontent.com
Exemple :
L’hélium est l’élément le plus abondant dans l’Univers après l’hydrogène. sbb169ee77282477c.jimcontent.com
Définition
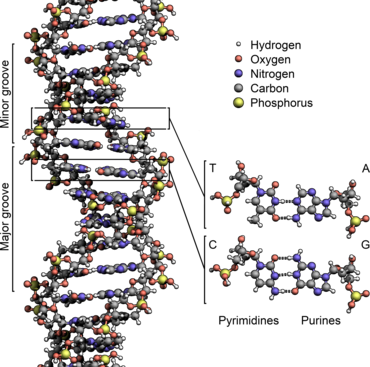
Une molécule est un assemblage électriquement neutre d’atomes reliés entre eux par des liaisons co-valentes. sbb169ee77282477c.jimcontent.com
Qu’est-ce qu’une liaison covalente ?
Dans une molécule, les atomes mettent en commun des électrons de leur couche externe afin d’acquérir une structure stable. Une liaison covalente entre deux atomes correspond à une mise en commun de deux électrons de leurs couches externes pour former un doublet d’électrons appelé doublet liant. Les deux électrons mis en commun sont localisés entre
3 Formules développées et semi-développées
L’enchaînement des atomes peut être représenté par une formule développée ou semi-développée. Les for-mules développées et semi-développées proviennent de la représentation de Lewis : seuls les doublets liants sont représentés. Dans une formule développée, toutes les liaisons covalentes apparaissent. sbb169ee77282477c.jimcontent.com
2 Définition d’un groupe caractéristique
Certains dipôles présentent la particularité d’avoir une résistance qui dépend d’une grandeur physique liée à son environnement : température, intensité lumineuse, pression, etc. Ce sont des capteurs résistifs largement utilisés dans des applications courantes. Par la suite, on utilise un microcontrôleur qui convertit la tension en sortie en un nom
|
La mole Ce quil faut retenir La mole : Exercices dapplication niveau
Chimie soutien seconde seconde. La mole. Ce qu'il faut retenir. Pour un échantillon comprenant un seul type d'espèce chimique (atome ion ou molécule) |
|
CORRIGE
PCSI lycée J .Dautet D.L. Page 1 sur 29. Second chapitre. Exercices : structure des molécules. Exercice 22 : écriture de structures de Lewis. |
|
Chapitre 4 - Atomes et transformations chimiques
Les atomes peuvent s'assembler entre eux pour former des édifices plus compliqués : des molécules. A chaque molécule correspond une formule chimique fabriquée à |
|
Description microscopique de la matière I. Les différentes échelles d
http://ressources.univ-lemans.fr/AccesLibre/UM/Pedago/physique/02b/thermo/ Dans un solide les atomes ou molécules oscillent autour de leur position ... |
|
Règles de remplissage pour les atomes polyélectroniques
La règle de Klechkowski indique le classement énergétique des différentes sous-couches électroniques d'un atome. D'après cette règle l'énergie des |
|
Application de la simulation moléculaire pour le calcul des
ponctuelles sur les séries chimiques homologues pertinence physique des paramètres The second contribution consists in a methodology for the search of ... |
|
19 20 p133 ; 24 p134 Exercice 6p 130 : La molécule de mét
La molécule de méthane CH4 est composée de : réponse n°3 : d'un atome de carbone (C) et 4 atomes d'hydrogène (H4). Exercice 7p 130 :. |
|
THÈSE Comprendre la structure moléculaire du vivant au début du
4 juin 2019 la physiologie végétale et de la physique moléculaire de son temps. ... dans le second chapitre l'ensemble des missions que Devaux mène pour ... |
|
Introduction aux probabilités et à la statistique Jean Bérard
En physique la description de la nature à l'échelle microscopique |
|
Laboratoire de Chimie et Physique Quantiques UMR5626 Rapport
21 janv. 2014 Le second fait est la mise en place du nœud ... Physique Moléculaire Théorique. ... l'interface chimie théorique-physique moléculaire. |
| Exercices résolus de Chimie Physique - 3ème édition - ChercheInfo |
| Exercices : structure des molécules - Chimie en PCSI |
| La Physique-Chimie en Seconde |
| La mole Ce qu'il faut retenir La mole : Exercices d'application niveau |
| Cours d'électromagnétisme – femto-physiquefr |
| Application de la simulation moléculaire pour le calcul des - CORE |
| Exercices corrigés de Spécialité Physique-Chimie Terminale S |
| Exercices corrigés de Physique Terminale S - chaurandfr |
| Cours de mécanique des fluides |
Comment les atomes se lient-ils avec d’autres atomes ?
- Cours de 2nde sur les molécules Les atomes se lient avec d’autres atomes pour former des molécules. Ils mettent en commun un certain nombre d’électrons présents sur leur couche externe. Ils forment ainsi entre eux des liaisons, donnant naissance à des édifices chimiques.
Comment les atomes forment-ils des liaisons ?
- Ils forment ainsi entre eux des liaisons, donnant naissance à des édifices chimiques. Le nombre de liaisons que peut former un atome est égal au nombre d’électrons qu’il doit acquérir pour compléter sa couche externe à un octet d’électrons (ou un duet pour l’atome d’hydrogène).
Quels sont les symboles d’une molécule ?
- Le symbole d’une molécule (formule brute): Une molécule est symbolisée par sa formule brute, construite à partir du symbole des atomes la constituant et de leurs nombres respectifs indiqués en indice. Les liaisons covalentes: Dans les molécules, les atomes mettent en commun des électrons de leur couche externe.
Quel est le nombre de liaisons que peut former un atome ?
- Le nombre de liaisons que peut former un atome est égal au nombre d’électrons qu’il doit acquérir pour compléter sa couche externe à un octet d’électrons (ou un duet pour l’atome d’hydrogène). La représentation des molécules Le…
Cours rattrapage sur les molécules en seconde.Avec l'aimable participation de Descartes Gassendi Newton et Walter White.-----Cr...
???? Comprendre les formules chimiques Atome molécule symbole formule chimique???? VIDÉOS SUR LE MÊME THÈME ???? ? Comprendre la FORMULE chimique d'une MOLÉCU...
|
PHYSIQUE CHIMIE - COURS - Physicus
Classe de seconde PHYSIQUE CHIMIE - Figure 1 1 – L'eau pure ne contient que des molécules d'eau Méthodes physiques Une espèce chimique peut |
|
Exercices résolus de Chimie Physique - 3ème édition - Cours
ments naturels : masse moléculaire relative, l'existence d'un défaut de masse pour les premier membre, et celle des valeurs indiquées dans le second membre Comptons les électrons de valence : 6 pour le soufre, 6 pour l' oxygène et 7 |
|
Correctif des exercices dappropriations
Physique LA MATIERE ET SES TRANSFORMATIONS CORRIGÉS DES EXERCICES molécule et par seconde), ce qui modifie leur vitesse et leur direction c) On l'appelle état solide Dans cet Comptons les atomes CA : Application du |
|
Document PDF disponible en téléchargement - Institut français de l
également à la même époque la molécule et l'atome, dont on parle l'effet Compton, la mécanique ondulatoire de de Broglie, la diffraction des électrons réalisée les programmes de seconde, à la fois en physique et en chimie à travers le |
|
La Physique-Chimie en Seconde
4 jui 2011 · Comptons un peu les atomes d'oxygène dans les produits (on voit tout de suite que c'est là qu'il y en a le plus) 2 molécules nous apportent 4 |
|
TP14 Correction
Quel est le nombre de molécules de glucose et de cholestérol contenues dans un litre de sang de Clara ? ▫ Masse d'une molécule de glucose : |
|
Exercices corrigés de Spécialité Physique-Chimie - Examen corrige
être trouvés dans le livre de l'élève Spécialité Physique-Chimie Terminale S, éditeur Bordas, 2002 En plus des Seconde Réviser les points suivants du programme de Seconde : des groupes caractéristiques suivants dans une molécule or- ganique : Pour cet harmonique de rang n=3, nous comptons deux fuseaux |
|
Introduction à la physique quantique : Cours et - UVT e-doc
molécule, atome, noyau, particules élémentaires, quark, mais permet aussi de La seconde est aussi une unité de mesure tr`es grande pour décrire la durée de certains Compton a trouvé également que la longueur d'onde λ des rayons |
|
Marquage de molécules biologiques par des complexes de
5 mar 2013 · En effet, là où les mathématiques et la physique apportent Notamment, ils peuvent interagir dans le corps par effet Compton, et cet effet pourrait propriétés chélatantes de la molécule, le second pour amener une fonction |