surfusion de l'eau exercice corrigé
|
Exercices de thermodynamique : équilibre physique du corps pur et
P1) Evolutions d'un état de surfusion vers un état d'équilibre Le potentiel chimique de l'eau liquide a pour expression : ?l = ?°l + Vl .(P – P0) + RT. |
|
Deuxième principe de la thermodynamique
Justifier qu'on observe une ébullition si on fait couler de l'eau froide sur le ballon après l'avoir rebouché. Exercice 7 : Surfusion du phosphore. Le phénomène |
|
Travaux dirigés de Thermodynamique n°7
Exercice 1 : Détente réversible d'un gaz parfait au contact d'un mélange eau+glace. Un cylindre à parois diathermes fermé par un piston |
|
Thermodynamique : changements détat (PCSI) - Nanopdf
Exercice Surfusion. Une masse m d'eau liquide est portée à -6°C dans un congélateur tout en restant à l'état liquide. On perturbe légèrement le système |
|
Exercices de Thermodynamique
(en kJ.mol?1) de la vapeur d'eau sous P = 70 bars pour différentes h et de largeur L (cf. exercice pré- ... Ce phénomène porte le nom de surfusion. |
|
PREMIER PRINCIPE DE LA THERMODYNAMIQUE 1 Calculs de
accessoires (i.e la masse d'eau de même capacité thermique que le vase et les Rappeler ce qu'est le phénomène de surfusion. ... Corrigé exercices 7 à 10. |
|
ZZZ_SuppExos_TH6_Changement Etat
? Exprimer puis calculer la chaleur latente de fusion lfus de l'eau sous la pression atmosphérique. Exercice. Exercice 5 : Cessation de surfusion. Cessation |
|
CCP Physique 1 PC 2001 — Corrigé
avec le modèle de germination de Volmer puis à la solidification des gouttes d'eau après leur éjection du canon à neige. • Après quelques rappels de mécanique |
|
Sup PCSI1 - Exercices de physique Premier Principe appliqué aux
Premier Principe appliqué aux transitions de phases - Corrigés température de la glace ne sera pas uniforme elle va fondre ... Eau en surfusion. |
|
Changement détats
Exercices - Thermodynamique |
|
Corrigé de l’exercice de physique : Surfusion
La transformation 1 !3 est un changement de température sans changement d’état donc : DH1!3 = mc(T fus T0) La transformation 1 !3 est un changement partiel d’état Notons à la ?n de cette transformation m liq la masse d’eau liquide et m sol la masse de glace avec bien entendu m liq +m sol = m1 DH3!2 = m sol ‘ solidi?cation |
|
Solidification et fusion de l'eau pure - MAXICOURS
Exercice 3 : Surfusion de l’eau On place un récipient contenant d’eau à l’extérieur un jour où la température est L’eau initialement liquide atteint la température de tout en restant à l’état liquide Soudainement la totalité de l’eau se transforme en glace |
Comment étudier la fusion de l'eau ?
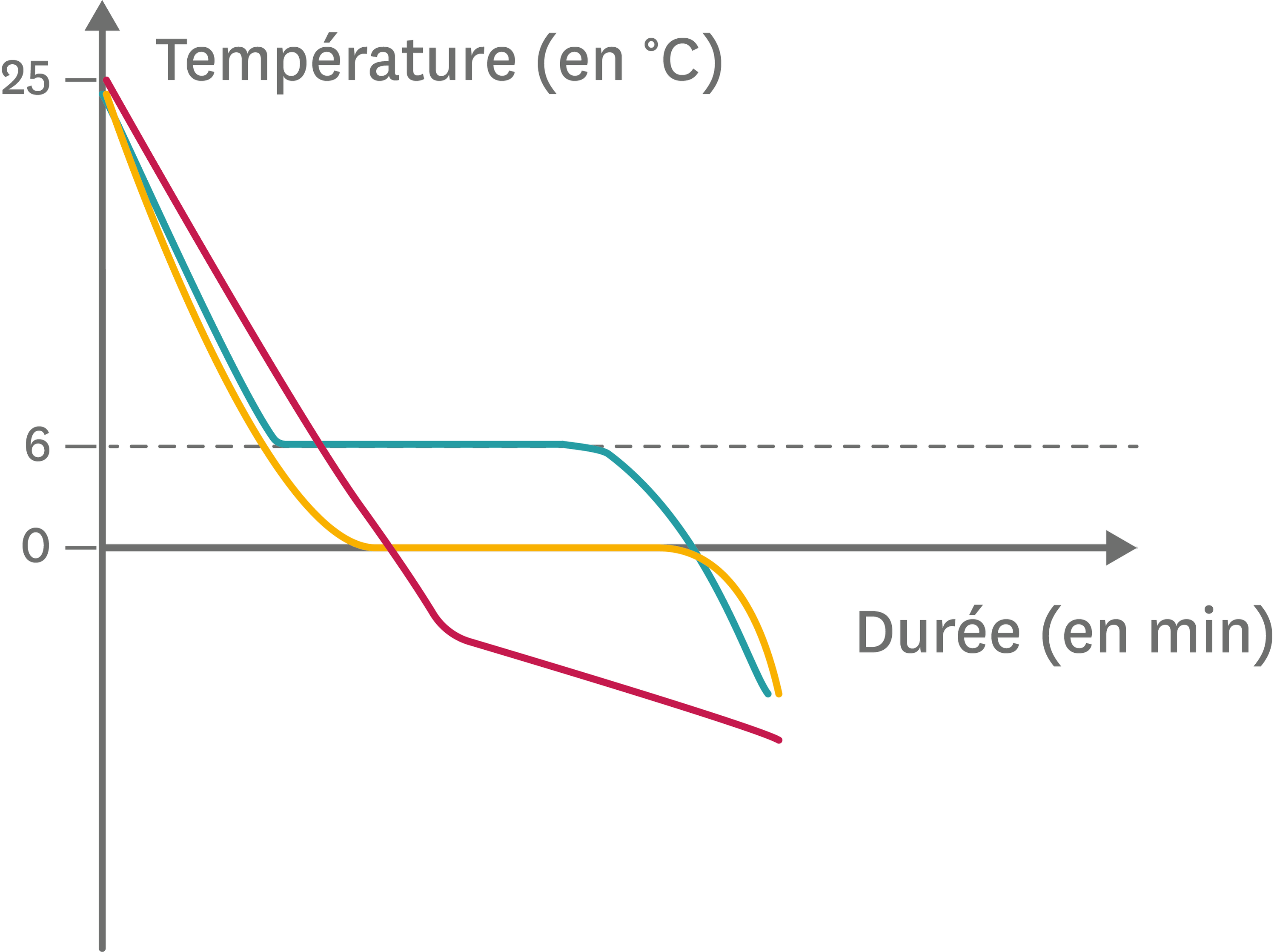
Fusion de l'eau Pour étudier la fusion de l'eau, on plonge un tube à essais contenant de la glace (constituée d'eau pure) dans de l'eau chaude, et on opère de la même manière que pour l'étude de la solidification : la température est mesurée régulièrement en utilisant un thermomètre électronique et un chronomètre.
Quelle est la température de fusion de l'eau ?
On dit que la température de fusion de l'eau est de 0 °C. Lorsque la glace et l'eau liquide coexistent, la température est de 0 °C : la fusion et la solidification de l'eau se font à température constante. Fusion et solidification de l'eau pure sont deux changements d'états inverses qui se déroulent à 0 °C.
Qu'est-ce que la tension superficielle de l'eau ?
La tension superficielle de l'eau est la propriété de la surface d'un liquide qui lui permet de résister à une force extérieure, en raison de la... Revoir la définition TENSIOACTIF , située dans la page 1 des mots en T du lexique du dictionnaire. Signification " tensioactif " publiée le 06/10/2021 (mise à jour le 08/08/2022).
Qu'est-ce que la solidification de l'eau ?
Solidification de l'eau On étudie les variations de la température au cours d’une solidification. L’eau est placée dans un tube à essais lui-même plongé dans un mélange réfrigérant ( doc. 1) constitué de glace pilée et de sel (sa température est inférieure à 0 °C).
| Corrigé de l’exercice de physique : Surfusion |
| Exercices de physique : Surfusion |
| CHAP 03-ACT EXP Dureté de l'eau-CORRIGE - legtuxorg |
| Travaux dirigés de Thermodynamique n°7 |
| CHAP 01-ACT EXP-salinité-eau-de-mer-CORRIGE |
| S Exercice : décomposition de l'eau oxygénée |
| Searches related to surfusion de l+eau exercice corrigé filetype:pdf |
|
Thermodynamique : changements détat (PCSI) - Bienvenue sur
Exercice Surfusion Une masse m d'eau liquide est portée à -6°C dans un congélateur, tout en restant à l'état liquide On perturbe légèrement le système, ce qui |
|
Travaux dirigés de Thermodynamique n°7 - CPGE TSI Lycée Louis
Exercice 1 : Détente réversible d'un gaz parfait au contact d'un mélange eau+ glace Un cylindre à parois Exercice 2 : Variation d'entropie lors d'un mélange eau liquide-glace Dans un récipient Exercice 8 : Surfusion de l'eau On place un |
|
Premier principe appliqué aux transitions de phases – CORRIGES
Sup PCSI1 - Exercices de physique Premier Principe {glace, 250 K} → {glace, 273 K} → {eau, 273 K}→{eau, 300 K} Le système ne va Eau en surfusion |
|
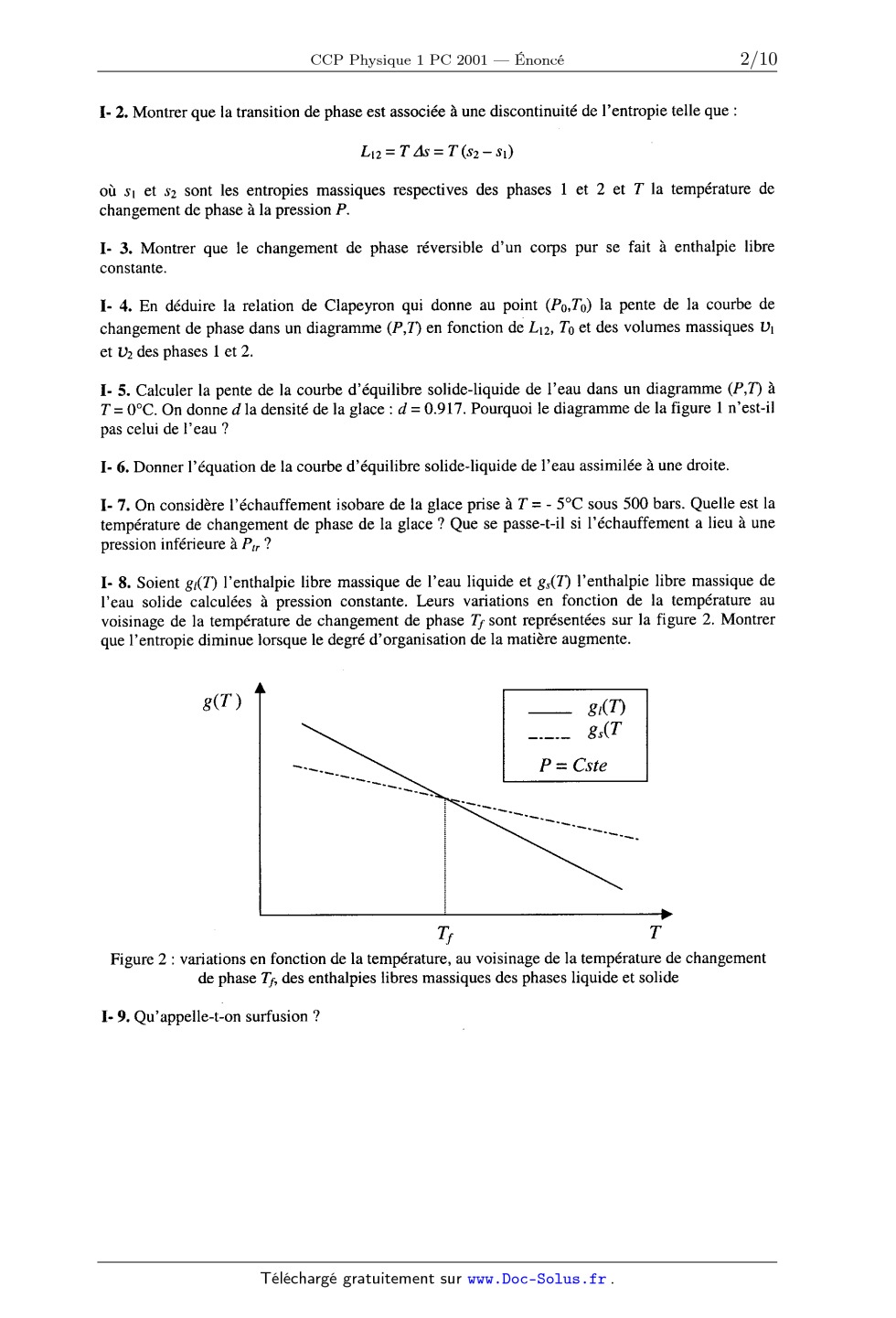
CCP Physique 1 PC 2001 — Corrigé - Doc Solus
Ce corrigé est proposé par Jean-Julien Fleck (ENS Ulm) et Yannick Alméras ( professeur en phase liquide-solide, le premier problème s'intéresse à l'étude de la surfusion avec le modèle de d'eau après leur éjection du canon à neige |
|
Changement détats
Exercices - Thermodynamique PTSI Une masse = 1 d'eau liquide est `a la température de 50∘ sous sa Ex-T6 8 Surfusion du Phosphore |
|
1 Transformation de glace en eau - Physique en sup 4
Mélange d'eau et de glace dans un calorimètre : Cessation d'une surfusion Remarque : exercice assez particulier, plutôt calculatoire, qui n'est pas dans |
|
Exercices de Thermodynamique
Exercices de Thermodynamique m3 mol−1) et l'énergie interne molaire U (en kJ mol−1) de la vapeur d'eau à Ce phénomène porte le nom de surfusion |
|
Le corps pur sous plusieurs phases - PDF4PRO
W Exercice 1 pression qu'aurait l'eau vapeur dans les mêmes conditions de volume et de Éléments de corrigé 1/9 suite à un phénomène de surfusion 2 |
|
Changements etats eau - Frédéric Elie on ResearchGate - Free
surfusion de l'eau : l'eau reste liquide au-dessous de 0°C mais c'est un état instable extrêmement complexe : pour commencer à s'initier sur ce sujet fort passionnant, consulter par exemple donnée par (le démontrer en exercice ) : |