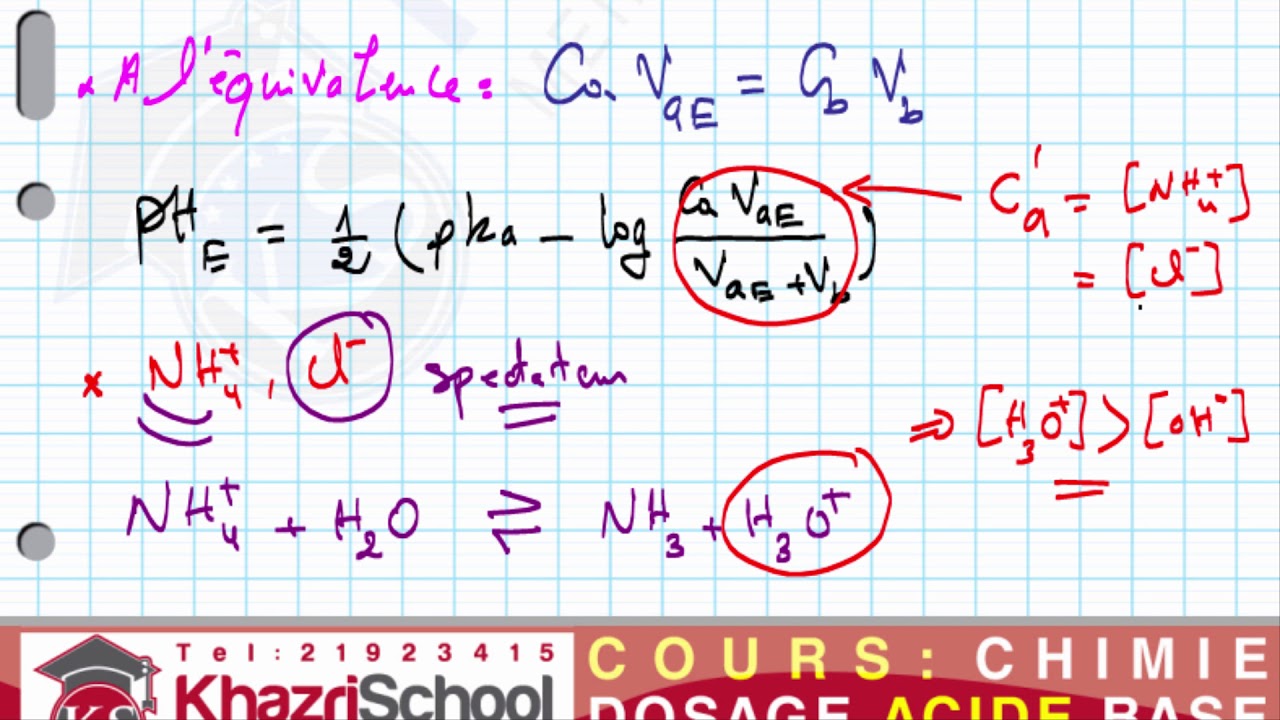dosage d'une base faible par un acide fort pdf
|
Base forte Acide fort – Base faible C ourbe Observation s
Acide fort – Base faible C ourbe Observation s • Faible variation de pH avant et ESSENTIEL DOSAGE ACIDO-BASIQUE LYCEE BEB IL KHADRA A u p oint de dem i |
|
Cours-titrage-acide-base-2ème-annnée-pdf
titrage d'une base faible par un acide fort le pH au point d'équivalence est toujours inférieur à 7 (point d'équivalence en zone acide) Page 8 8 Courbe de |
|
Doctorat de luniversité de toulouse
dosage d'un acide faible par une base forte et dosage d'une base faible par un acide fort pour la professeure P2 209 |
|
Dosages acide-base
Dosage d'un acide faible par une base forte 28 4 1 Ainsi [H3O+] = Ka et pH = pKa à la demi-équivalence 28 5 Dosage d'une base faible par un acide fort |
|
§ 7 (suite) Titrages acide-base
Courbe de titrage d'une base faible Titrage d'une base faible par un acide fort point d'équivalence pH = 1/2 pKa – 1/2 log (ca· "a / c0 ) pH = 7 + 1/2 pKa + |
|
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
LES REACTIONS ACIDE-BASE 1. Le pH 1.1 Définition Le pH
Remarque : A l'équivalence du dosage d'un acide fort par une base forte le pH noté pHE est de 70. 7.3.4 Repérage de l'équivalence a) A partir de la courbe |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
Titrage d'un acide faible par une base forte. CHAPITRE III : REACTIONS D'OXYDO-REDUCTION. 1. Généralités. 1.1. Oxydant réducteur |
|
Cour chimie : Dosage acide base
1- d'un acide fort par une base forte. ? l'équation de la réaction du dosage : H3o+ + OH -. ? P. H3o+. + 2H2. ? à l'équivalence : pH = 7 (solution neutre). |
|
Médecine Humaine
Titrage d'un acide faible par une base forte . de l'addition d'un acide fort la base faible A- se lie aux ions H+ ajoutés et forme HA. Lors de. |
|
Chapitre 1 Acides et bases
L'acide conjugué d'une base forte est dit “indifférent dans l'eau” Figure 1.3 – Gauche : Courbe de pH : dosage d'un monoacide faible (acide acétique). |
|
Dosages acidobasiques
9 févr. 2018 II Dosages acide-base. Nous allons étudier le dosage de solutions d'acide (fort ou faible) par une solution basique. |
|
XI. DOSAGES 1. Réaction Elle doit être totale instantanée et
Exemples : H3O+ + HO-. ? 2 H2O (acide fort / base forte ou l'inverse). AH + HO-. ? A-. + H2O (acide faible / base forte). |
|
Dosage acide faible – base forte
Dosage acide faible – base forte. Les relations établies classiquement le sont pour : ? un acide suffisamment faible et pas trop dilué. |
|
Médecine Humaine
Lors du titrage d'un acide fort par une base forte le. pH est donné à tout moment par la concentration des protons H+ restants |
|
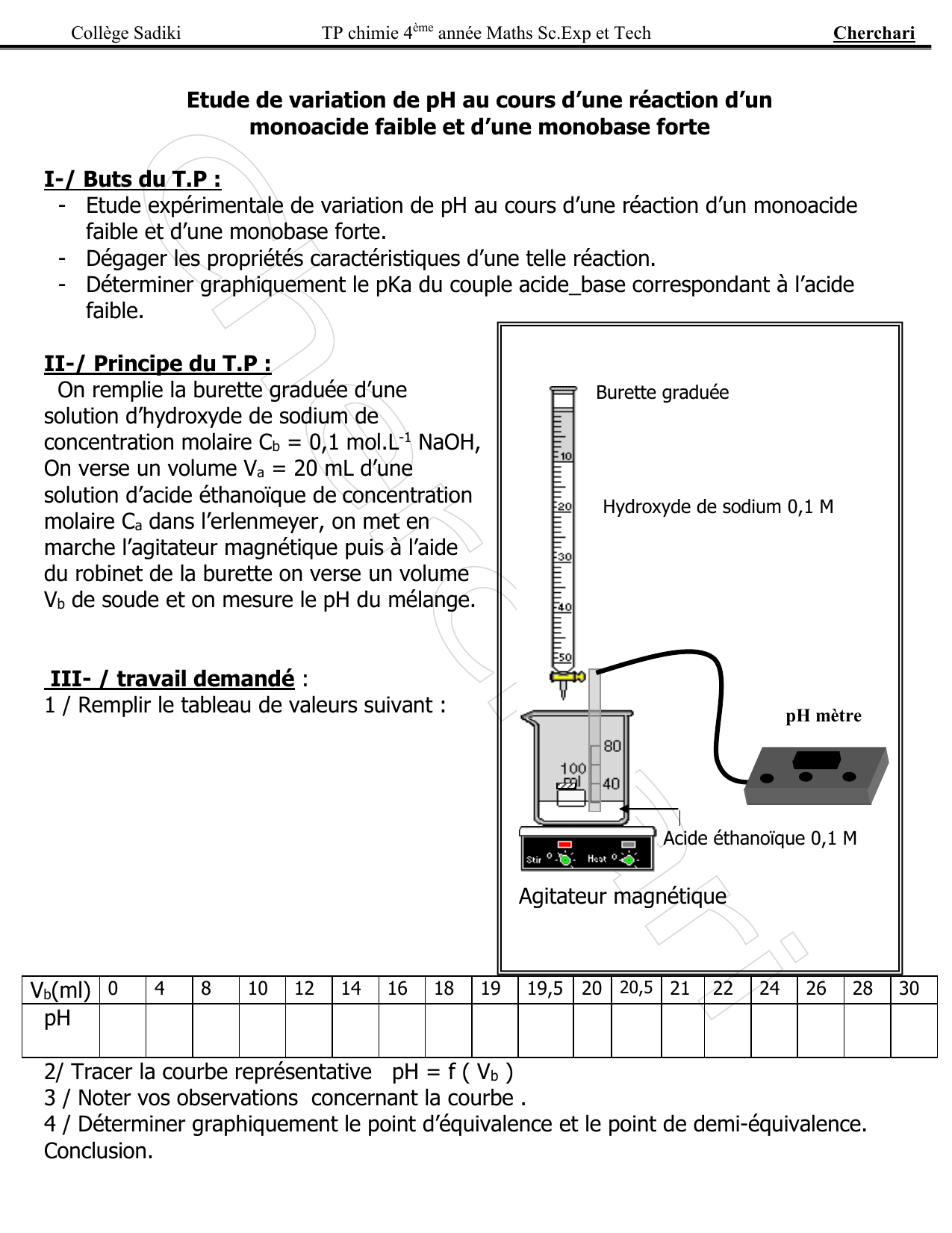
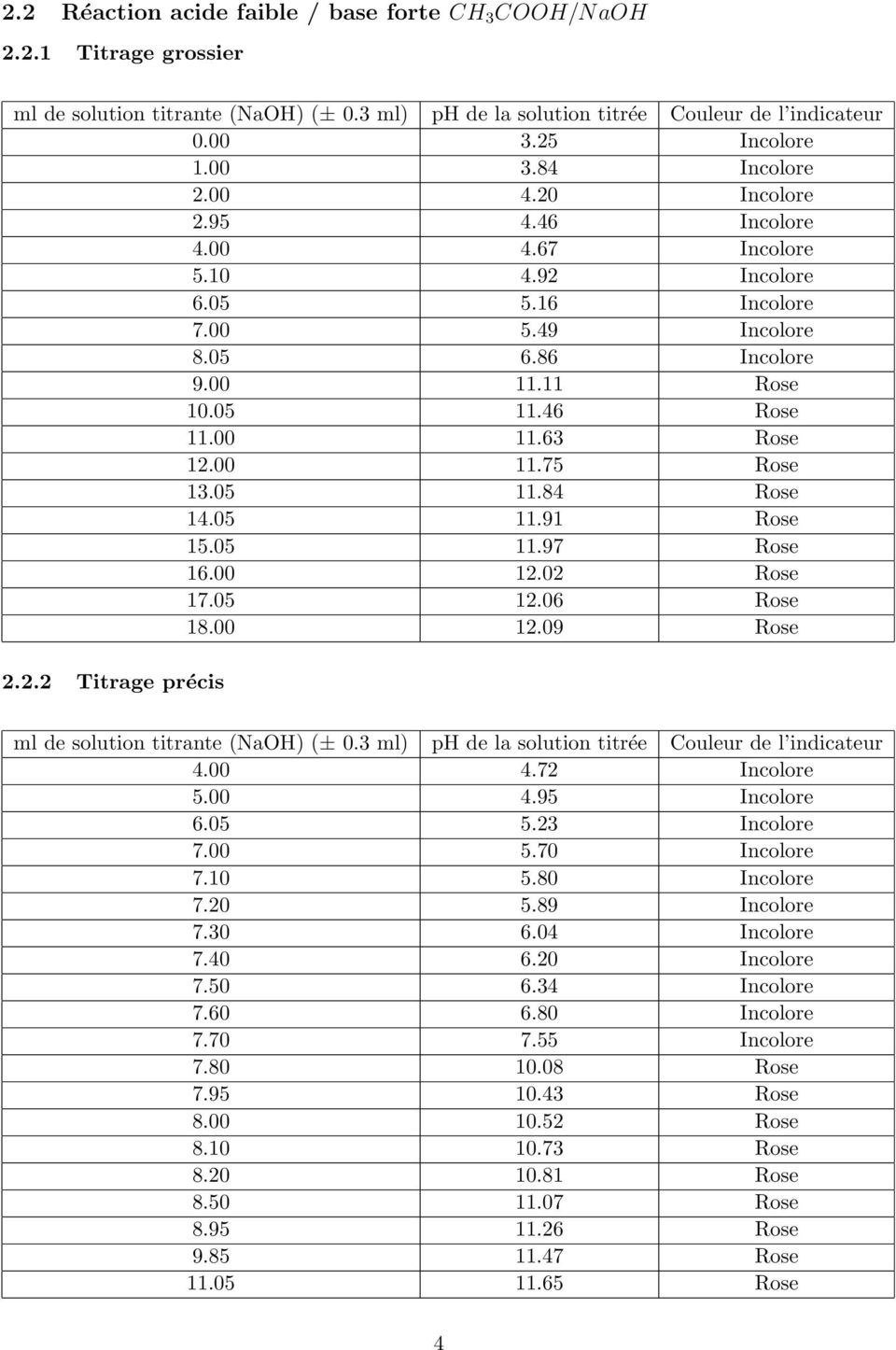
TP 3 -Titrage d’un acide fort et acide faible par une base
TP 3 -Titrage d’un acide fort et acide faible par une base forte (NaOH) But:-Détermination de la concentration des solutions d’acides chlorhydrique et acétique par la méthode du titrage (colorimétrie et PH-metrie) Principe : Le titrage est une technique de dosage utilisée en chimie analytique afin de déterminer la concentration |
|
Dosage acido-basique - Archiveorg
Le but d’un dosage est de déterminer une quantité de matière (ou une concentration) inconnue Un dosage acido-basique fait intervenir une réaction acide-base totale entre le réactif à doser et un réactif titrant de concentration connue pH Espèce majoritaire : Couleur : HIn pKi pKi -1 pKi +1 In- de HIn zone de virage de In- |
|
Base forte Acide faible Base forte Acide fort Base faible
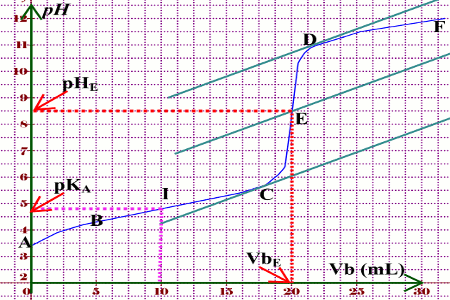
Les réactions acide-base Acide fort – Base forte Acide faible – Base forte Acide fort – Base faible Courbe Observations • Faible variation de pH avant et après l’équivalence • Saut brusque de pH au voisinage du point d’équivalence • La courbe admet un point d’inflexion c’est le point d’équivalence E • pH E |
|
ème année LES TITRAGES ACIDES-BASES
VII) Titrage d’un acide faible par une base faible : Considérons le titrage de CH 3 COOH 01 M par NH 3 01M pK a1 de NH 3 /NH 4 + = 925 pK a2 de CH 3 COOH/CH 3 COO-= 474 a) variation du pH : Au départ le pH de l’acide faible : pH = ½ pK a2 - ½ log Ca = ½ 474 - ½ log 01 pH = 287 V B |
|
Searches related to dosage dune base faible par un acide fort pdf PDF
Dosage acide fort – base forte Acide fort HA : titré concentration (à déterminer) c a volume v a: HA H O ?H O ++ A ? 2 3 Base forte NaOH titrant concentration c b volume v b (à verser à la burette) : NaOH ?Na + +OH ? L’équation bilan de la réaction de dosage s’écrit : H 3 O +OH ?2 H 2 O + ? |
Quelle est la différence entre acide fort et acide faible?
Acide fort –Base forte Acide faible –Base forte Acide fort –Base faible Courbe Observations •Faible variation de pH avant et après l’équivalence. •Saut brusque de pH au voisinage du point d’équivalence. •La courbe admet un point d’inflexion, c’est le point d’équivalence E. •pH
Quels sont les différents types de réactions acide-base?
Les réactions acide-base Acide fort –Base forte Acide faible –Base forte Acide fort –Base faible Courbe Observations •Faible variation de pH avant et
Comment faire un titrage acido-basique ?
concentration initiale. Pour réaliser un titrage acido–basique, on procède à une addition contrôlée d'une solution aqueuse de base (ou d'acide) detitre connu à un volume déterminé de la solution d'acide (ou de base) de titre inconnu, jusqu'à atteindre l'équivalence. A l'équivalence, toutes les espèces H 3 O
Comment calculer l’équivalence d’une base forte ?
Base forte NaOH titrant, concentration c b, volume v b(à verser à la burette) : NaOH ?Na ++OH?. L’équation bilan de la réaction de dosages’écrit : H 3 O +OH?2 H2O +?. L’équivalenceest atteinte lorsque : 0 H 3 O )n ( OH)versé +=?c’est à dire lorsque a va=c b. vb,éq. Pour étudier la variation du pH en fonction de v
| Dosage acide fort - base forte - Le Mans University |
| Dosage acide fort - base forte - Le Mans University |
| TP 3 -Titrage d’un acide fort et acide faible par une base |
| Base forte Acide faible Base forte Acide fort Base faible |
| Chap S- Dosage de solutions d’acide par une base forte |
| Searches related to dosage d+une base faible par un acide fort pdf filetype:pdf |
Comment calculer le dosage d’un acide fort ?
- 1 Dosage acide fort – base forte Acide fort HA : titré, concentration (à déterminer) c a, volume v a: HA H O ?H O ++ A? 2 3.
. Base forte NaOH titrant, concentration c b, volume v b(à verser à la burette) : NaOH ?Na ++OH?.
. L’équation bilan de la réaction de dosages’écrit : H 3 O +OH?2 H2O +?.
Comment calculer l’équivalence acido-basique ?
- 2- Définition de l’équivalence acido-basique ?À L’équivalence acido-basique le nombre de moles de OH–provenant de la base est égale au nombre de moles de H 3o n provenant de l’acide H3o+ =n OH - C a V a =C b V b B- Dosage 1- d’un acide fort par une base forte ?l’équation de la réaction du dosage : H 3 o + OH P H 3 o + 2H 2