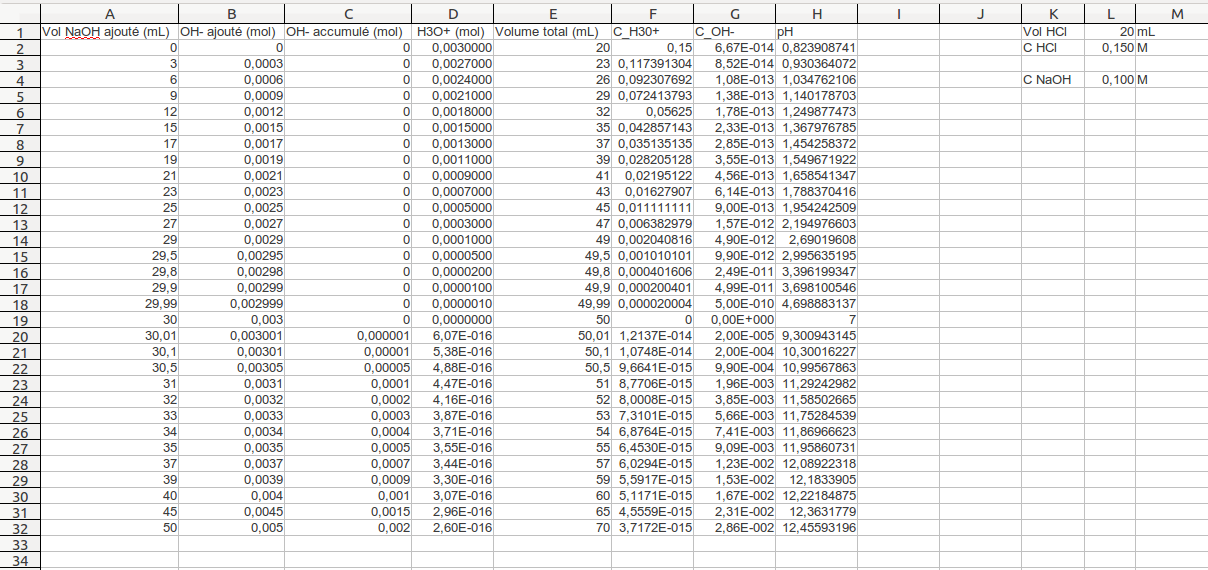
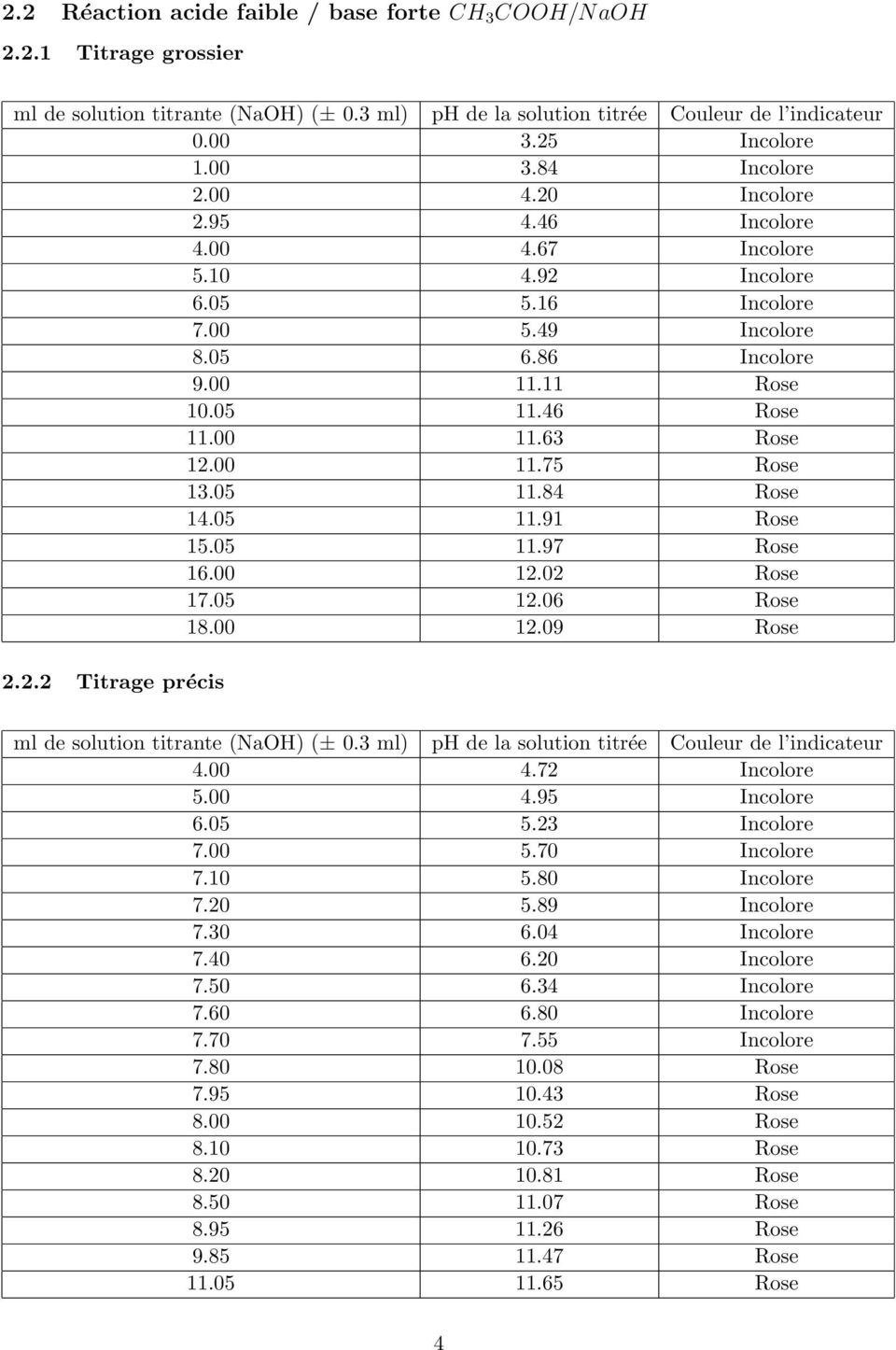
ph mélange acide faible base faible
|
§ 7 (suite) Titrages acide-base
Nous avons donc une solution d'une base faible et le pH peut être estimé à partir de l'équation approchée : pH = 7 + 1/2 pKa + 1/2 log ( ca· "a / c0 ) – pour ! |
|
Calcul du PH
Le pH d'une solution de sel d'acide faible et de base faible est celui d'un mélange d'acide faible et de base faible pH = 1/2 PK₂ b/bH + 1/2 pKa Ha/a- 11 |
|
PHDES SOLUTIONS DE MELANGE
=> Dissociation complète de l'acide => pH imposé par la base conjuguée a- de l'acide faible pH = 7 + ½ pKa + ½ log Ca 3 Sel d'acide fort et de base faible : |
|
VIEtude sommaire des mélanges
Au p E de la titration des acides faibles par des bases fortes le pH se situe souvent au-dessus de 7 parce qu'à ce moment le milieu renferme uniquement la base |
1.
3) L'échelle de pH Le pH d'une solution est compris entre 0 et 14. - Si pH < 7, la solution est acide. - Si pH = 7, la solution est neutre. - Si pH > 7, la solution est basique.
Comment déterminer le pH d'un mélange de solutions ?
Utiliser la concentration pour calculer le pH
L'équation du pH est la suivante : pH = -log[H3O+] X Source de recherche .
Cherchez à connaitre ce que chaque terme de l'équation représente.
Recherchez le terme utilisé pour la concentration.
En chimie, les crochets [ ] indiquent généralement une « concentration de ».
Comment varie le pH d'une solution par ajout d'acide ?
Plus une solution est acide, plus son pH est faible.
Exemple : le jus de citron est plus acide que le vinaigre : pH(citron) = 2,2 et pH(vinaigre) = 2,4.
De même, plus une solution est basique, plus son pH est grand.
Lorsqu'on dilue une solution acide, elle devient un peu moins acide et son pH se rapproche de 7.
Comment calculer le pH d'un mélange acide faible base forte ?
Si l'on admet que les ions OH– provenant de la dissociation de la base conjuguée de notre acide faible sont en quantité négligeable par rapport à ceux provenant de la solution titrante de base forte, on a simplement : pH = 14 + log { ctitr⋅"titr / c0 }.
|
VI..Etude sommaire des mélanges
d'hydrolyse des acides et bases faibles augmente avec la dilution!) Exemple: Mélange de 500 ml On calcule souvent le pH en négligeant l'acide faible. |
|
Dosage acide faible – base forte
Dosage acide faible – base forte un acide suffisamment faible et pas trop dilué ... x=0 ; vb=0 ; solution d'acide faible. )clog. pK(. 2. 1. pH. |
|
§ 7 (suite) Titrages acide-base
Considérons le titrage d'une solution d'un acide faible tel que l'acide acétique par exemple |
|
§ 7 (suite) Calcul du pH de solutions
Si la concentration d'un acide faible HA ou d'une base faible B en solution est suffisamment grande et leur pKa ou pKb également suffisamment grand la fraction. |
|
Chapitre 1 Acides et bases
acide si son pH est inférieur à 7 i.e. [H3O+]> 10?7 mol.L?1 (à 25?C) ; L'acide conjugué d'une base faible est un acide faible. Exemples :. |
|
ACIDE FAIBLE – BASE FAIBLE *** COUPLE ACIDE-BASE
ACIDE FAIBLE – BASE FAIBLE *** COUPLE ACIDE-BASE Mais on constate que : pH = 29 ? ... c'est un mélange équimolaire d'acide faible et de base forte. |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI
CALCUL DE PH DES SOLUTIONS AQUEUSES 2.5. Cas d'un mélange d'un acide fort et d'un acide faible. ... Titrage d'un acide faible par une base forte. |
|
PH et pKa
Plus la valeur de pKa est faible plus le Ka est grand |
|
Aucun titre de diapositive
Mélanges d'acides forts et d'acides faibles. Base Mélanges de base forte et de base faible ... Quel sera le pH d'une solution d'un acide faible à la. |
|
Solutions tampons
pH. 2. 1 x. = = . : Les solutions constituées d'un mélange d'un acide faible et de sa base conjuguée (exemple : HCH3CO3 + NaCH3CO3 ) constituent donc des |
|
VIEtude sommaire des mélanges
d'hydrolyse des acides et bases faibles augmente avec la dilution) et acide fort 2 Le pH se calcule en sachant que les deux acides sont entièrement ionisés |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
CALCUL DE PH DES SOLUTIONS AQUEUSES 2 1 2 5 Cas d'un mélange d' un acide fort et d'un acide faible Titrage d'un acide faible par une base forte |
|
Formules de Phpdf - Proximus
Mélanges équimolaires d'acide et de base faibles On néglige donc l' autoprotolyse pour un acide si le pH est à 6 et pour une base si le pH est supérieur à 7 |
|
Calcul du PH
4- pH d'une solution base forte très diluée C:= [1,0"]- 6-pH d'une solution d' acide faible très dilué 13- pH d'une solution de mélange de deux acides faibles |
|
PH et pKa - Eli Zysman-Colman
Plus la valeur de pKa est faible, plus le Ka est grand, plus l'acide est fort 4 Table de pKa pH d'un mélange d'acide faible avec sa base conjuguée |
|
§ 7 (suite) Calcul du pH de solutions - EPFL
des couples acide-base présents: acide(s) ou base(s) faibles, autoprotolyse de l' eau pH d'un mélange d'un acide faible et de sa base conjuguée Si HA est |
|
PH = pKa - BIENVENUE SUR LA PAGE DE THIERRY BRIERE
T Briere- Acides et Bases - Chap 2 4 Dans ce chapitre nous étudierons les cas suivants : Acide fort Acide faible Mélanges d'acides forts Mélanges d'acides |
|
Le pH 6 Le dosage des solutions dacides et des bases faibles
Calculer la concentration de l'espèce dosée à partir de Ve ou du pH initial de la La réaction du dosage d'un acide ou d'une base faible doit donc être Rappel : Une solution tampon est une solution formée par le mélange d'un acide faible |
|
Dosage acide faible – base forte
log pK pH a bb aa bb a − + = − + = dosage d'un acide faible (pKa=3, ca= 0 01 mol L-1) par une base forte (cb=0 01 mol L-1) x = n base versé / n acide initial |
|
Révisions sur les acides et les bases - Nicole Cortial
Exemples de réactions de dissolution de bases et d'acides faibles : • L'acide 1° ) Solution d'acide fort (AH) de concentration molaire a C a Clog pH −= |