pile électrochimique pdf
|
Les piles dispositifs mettant en jeu des transformations spontanées
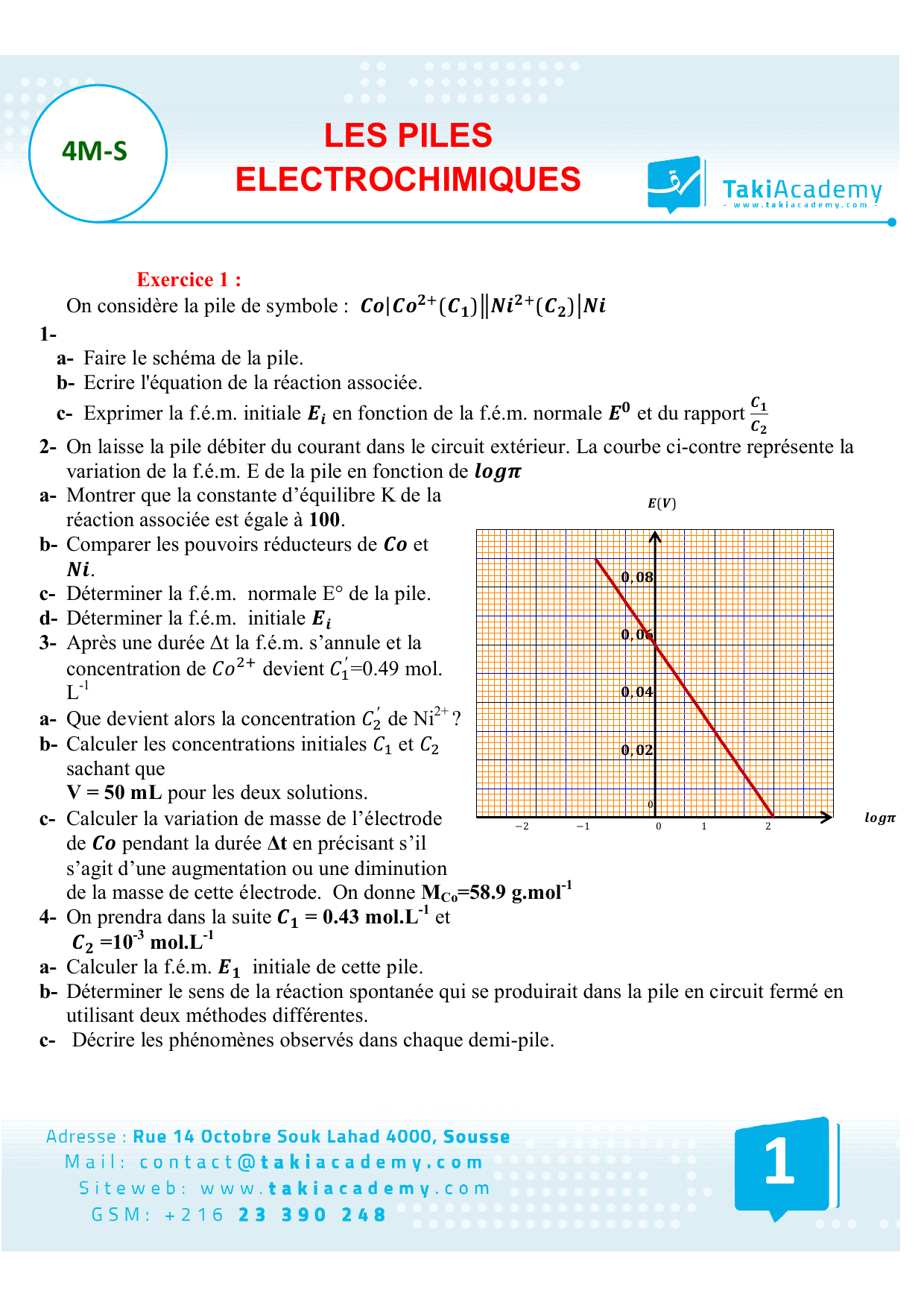
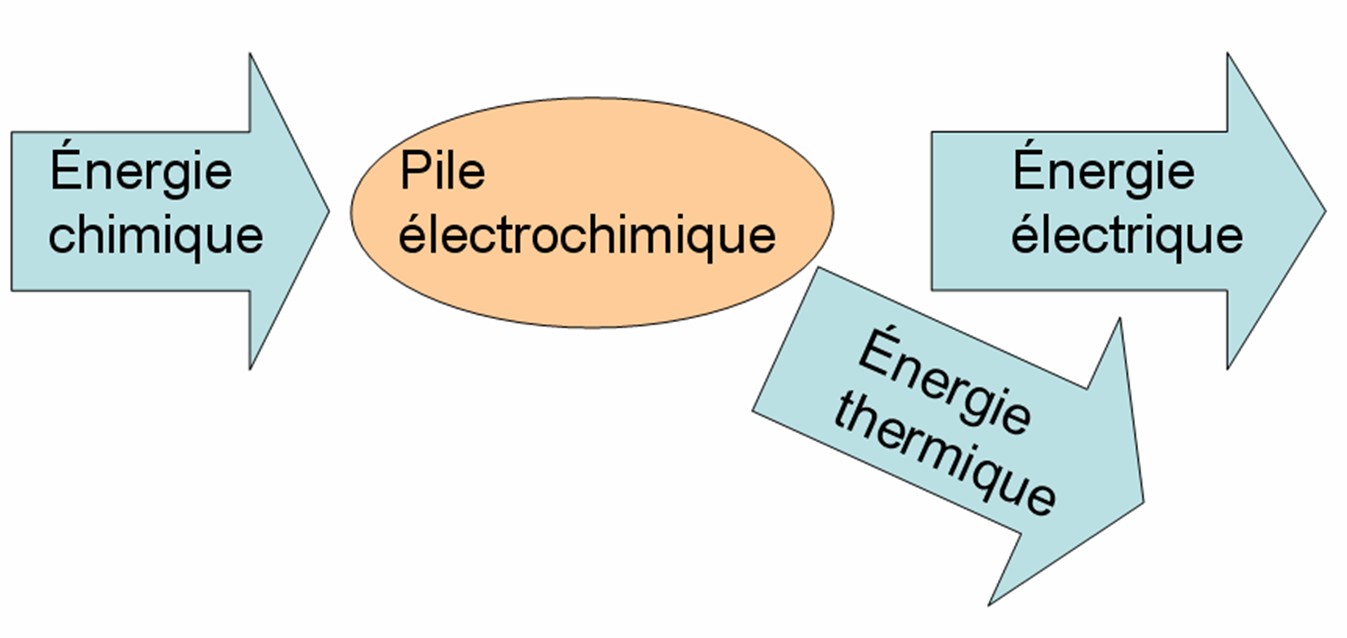
1) Définition : Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie |
|
10pilespdf
Les piles électrochimiques A : Petite parenthèse hydraulique B : Les piles au laboratoire 1 Descriptif 2 Un transfert spontané d'électrons 3 La pile |
Elle s'intéresse aux réactions chimiques, qui dans certaines conditions, créent un mouvement d'électrons et donc un courant électrique.
La pile est un générateur électrochimique.
Ce système permet de fournir de l'électricité à partir de réactions chimiques.
Quel est le rôle de la pile ?
La pile électrique ou pile jetable, est un petit générateur portable d'énergie électrique qui transforme l'énergie d'une réaction chimique en énergie électrique.
Contrairement aux batteries (ou accumulateurs), la pile est à usage unique et ne peut être rechargée.
Quel est le rôle de chaque électrode dans une pile ?
Électrodes pour les piles
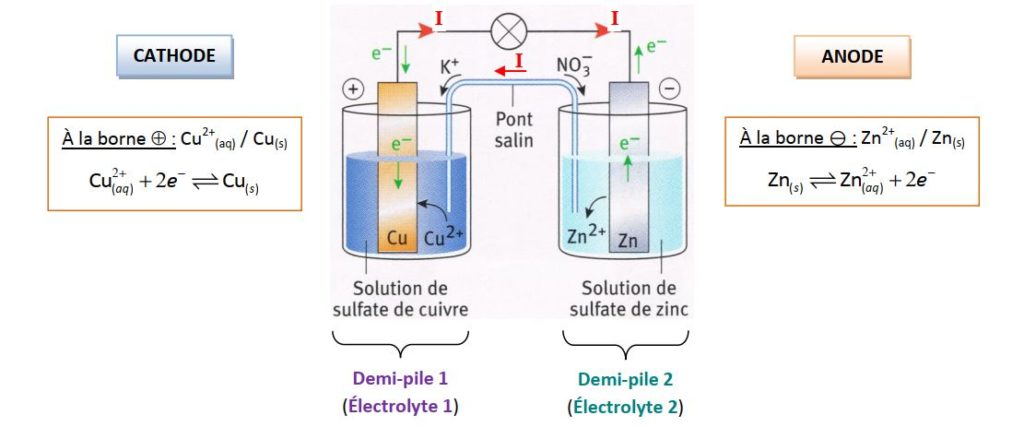
La réaction redox de la pile se déroule par moitié à chacune, qui sont le siège d'une réaction spontanée : l'une est le siège de la réaction de réduction, c'est la cathode (pôle + de la pile) ; l'autre est le siège de la réaction d'oxydation, c'est l'anode (pôle – de la pile).
Qui a inventé la première pile électrochimique ?
Historiquement, c'est le premier Congrès international d'électricité, tenu à Paris en 1881, qui a adopté le vocable volt pour l'unité de force électromotrice, en l'honneur de Volta, inventeur de la pile électrochimique.
|
Les piles électrochimiques
Les piles électrochimiques La force électromotrice ou f.e.m. d'une pile ... Une pile permet de convertir de l'énergie chimique en. |
|
I- La pile Daniell Cours chimie : Piles électrochimiques
spontanée est appelé pile électrochimique. Une pile est constituée de deux demi-piles reliées par une jonction électrochimique ou pont salin. |
|
Etude et réalisation dune pile électrochimique.pdf
Électrochimie (Thermodynamique Cinétique |
|
Les piles dispositifs mettant en jeu des transformations spontanées
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique. |
|
Chapitre 2 : Les piles électrochimiques I. Quels sont les deux types
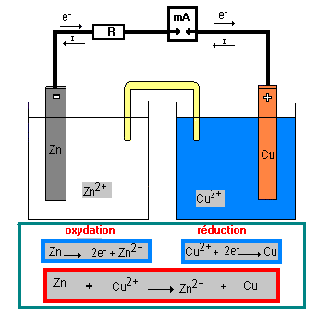
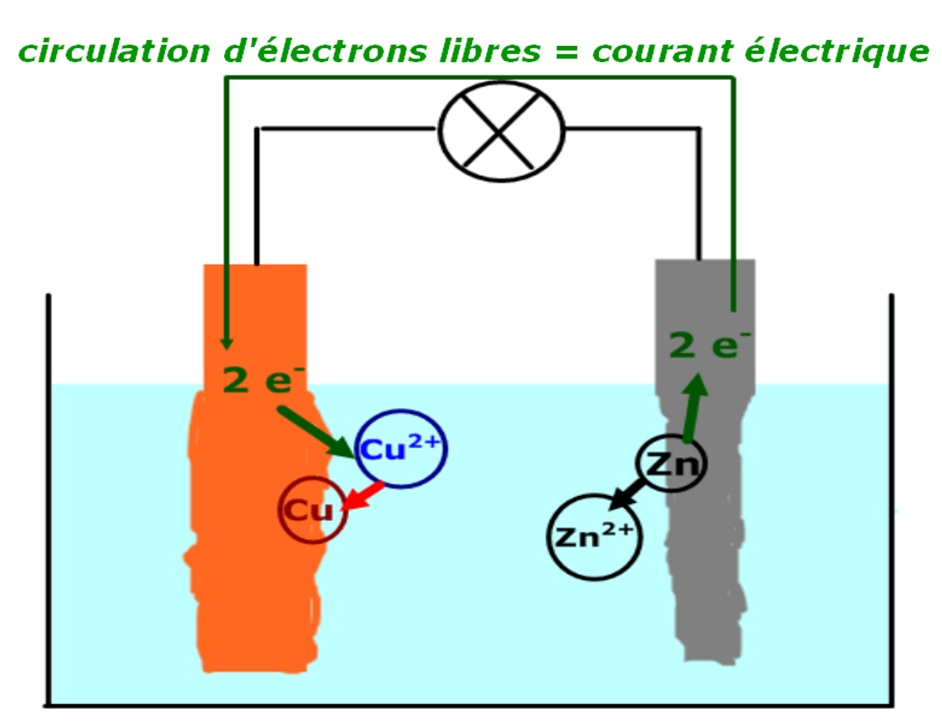
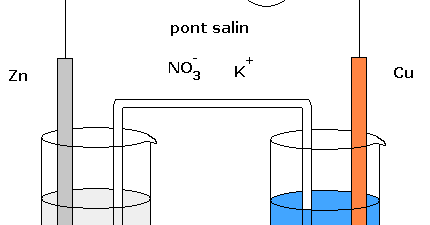
Comment fonctionne une pile électrochimique ? Prenons l'exemple de la pile Daniell (Zinc – Cuivre). Pont salin. (s). |
|
Chap 7 la pile électrochimique
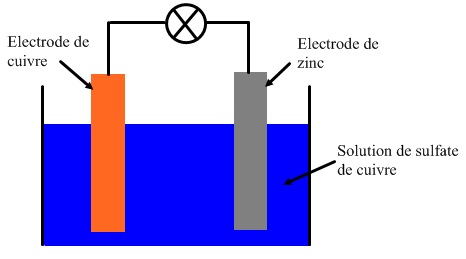
Chap 7 La pile électrochimique. Quels sont les ions responsables de la couleur bleue de la solution de sulfate de cuivre? Pourquoi une solution de sulfate |
|
Thème : Piles et électrolyses Fiche 4 : Piles et électrolyses
A l'anode Zn = Zn2+ + 2e- et à la cathode MnO2 + H3O+ + e- = MnO(OH) + H2O. Pour le fonctionnement de la pile : Zn + 2 MnO2 + 2 H3O+ = Zn2+ + 2 MnO(OH) avec le |
|
La pile électrochimique : source dénergie?
Une lame de zinc et une lame de cuivre plongées dans une solution de sulfate de cuivre constituent une pile électrochimique. Il existe une tension entre ces |
|
Linvention de la pile électrochimique par Volta
L'invention de la pile électrochimique par Volta par Jean-Jacques Samueli Docteur ès sciences physiques. & Jean-Claude Boudenot |
|
On appelle pile électrochimique tout dispositif qui permet dobtenir
1) La pile Daniell et les piles électrochimiques de type Daniell: Une pile électrochimique de type Daniell est formé par les deux. |
|
Les piles électrochimiques Cours I-/ Définition dune - TuniSchool
Les piles électrochimiques Cours Cours En d'une pile II-/ Présentation de la pile Daniell 1-/ Schéma de la pile 3-/ Équation chimique associée à la pile |
|
10-Les piles électrochimiques - Physagreg
Une pile électrochimique est un générateur qui transforme de l'énergie chimique fournie par une réaction d'oxydoréduction spontanée en énergie électrique |
|
Chap4 Pile électrochimique et énergie chimique
Comment fabriquer une pile ? DI : Les calculs citronnés ont la patate Remarque : pour augmenter la tension, il faut associer deux piles en |
|
Filière sciences de la matière Cours délectrochimie SMC Semestre 5
positif en utilisant à ce pôle un système redox de tension plus élevée que celle de l'électrode à hydrogène a Piles impolarisables : Pile Daniell : + Cu / CuSO4 |
|
Les piles électrochimiques - MMorin
Les piles électrochimiques I) Des expériences de Galani à la pile de Volta : d' inventer la première pile électrochimique II) Une transformation chimique |
|
Piles et électrolyses - Studyrama
Dans la pile, les cations circulent de la demi pile à l'aluminium vers la demi pile au nickel et les anions en sens inverse ▻ Exercice n°2 1) Les électrons circulent |
|
Chapitre 2 : Les piles électrochimiques I Quels sont les - Eklablog
Comment fonctionne une pile électrochimique ? Prenons l'exemple de la pile Daniell (Zinc – Cuivre) Pont salin (s) |
|
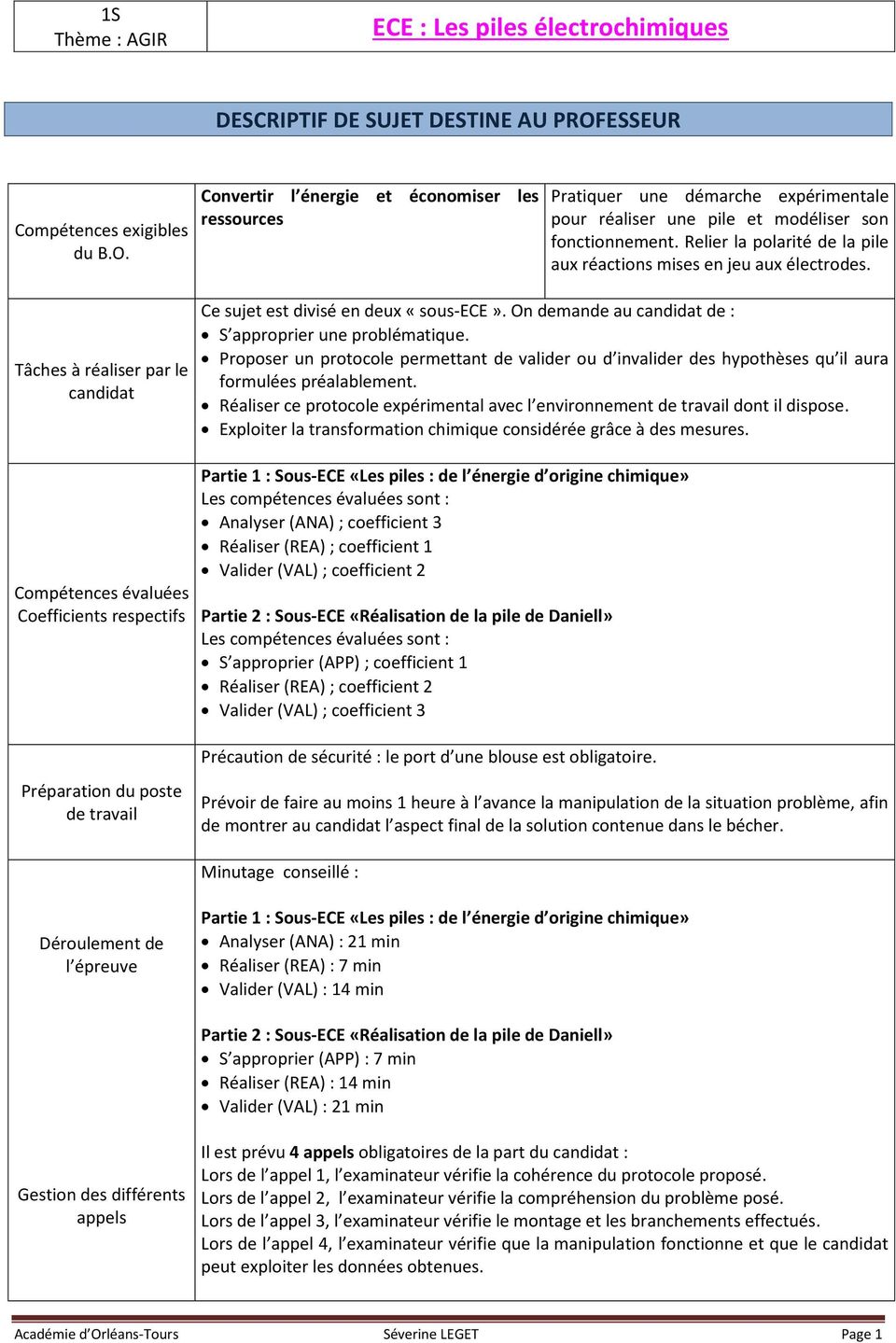
ECE : Les piles électrochimiques - Académie dOrléans-Tours
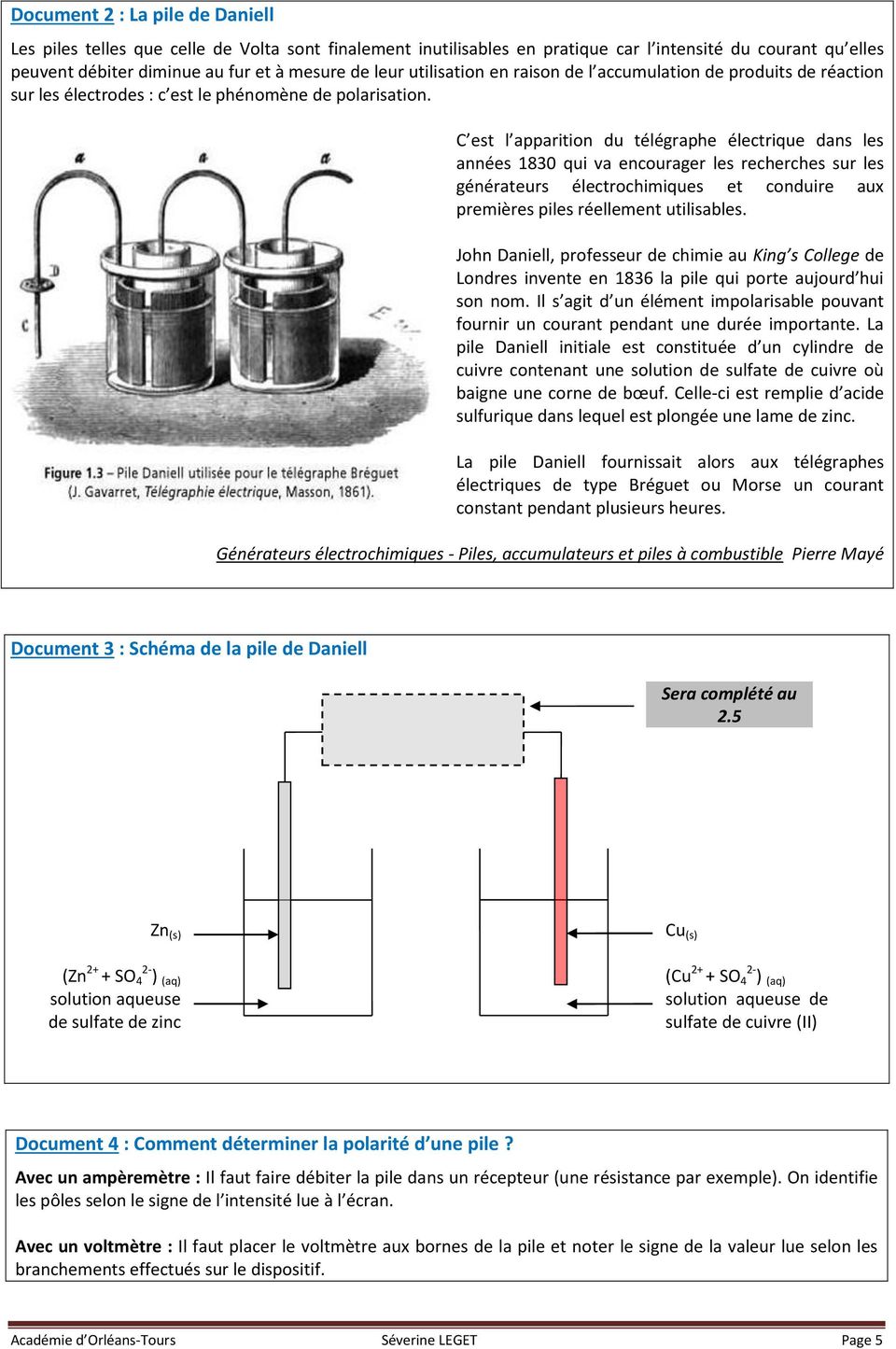
La pile Daniell fournissait alors aux télégraphes électriques de type Bréguet ou Morse un courant constant pendant plusieurs heures Générateurs |
|
Piles électrochimiques
Dans un bécher mélanger environ 20 mL d'une solution de sulfate de cuivre 0 1 mol/L et 20 mL de sulfate de zinc 0 1 mol/L - Plonger dans le bécher une lame |
|
Les piles et loxydo-réduction :
2 - Indiquer le signe des pôles de la pile formée ainsi que le sens de passage du courant Le couple du fer est oxydant vis à vis de celui du cuivre ( Volt 345 0 E |