reaction oxyde de cuivre et carbone
|
2
Etude de la réaction entre le carbone et l'oxyde de cuivre - Schéma du montage : On mélange 100 d'oxyde de cuivre et 120 de carbone Page 8 Les |
|
Chapitre 6 : Réactions doxydoréduction
Une réaction redox peut être endothermique ou exothermique L'oxyde de cuivre(II) joue le rôle d'oxydant : il oxyde le dihydrogène 113 |
|
CORRECTION DU TP N°6
VI Réaction entre l'oxyde de cuivre et le carbone : Schéma de l'expérience légendé : a Il se forme progressivement un solide rougeâtre sur les parois du |
|
Notion de la réaction chimique
dioxyde de carbone + l'eau 2-la réaction d'oxyde de cuivre II avec et le carbone a- Activité : on prépare un mélange qui constitue de carbone et l'oxyde de |
|
Réactions doxydation et de réduction
La réaction de l'oxyde de cuivre(II) avec l'hydrogène Chauffée dans un flux Le monoxyde de carbone réduit l'oxyde de fer en fer : Fe2O3 + 3CO −→ 2Fe + |
|
TP N°6 : CE QUI SE CONSERVE AU COURS DUNE
IV Réaction entre l'oxyde de cuivre et le carbone : Précautions : La réaction que nous voulons réaliser s'effectue uniquement si le carbone et l'oxyde de cuivre |
Comment se forme l'oxyde de cuivre ?
L'oxyde Cu2O qui se produit naturellement sous forme de cuprite et est obtenu sous forme de cristaux rouges ou jaunes ou de poudre par oxydation du cuivre dans un four ou par électrolyse et qui est principalement utilisé comme pigment (comme dans la céramique et dans les peintures antisalissures) et comme désinfectant
Comment ecrire une réaction d'oxydation ?
La réaction d'oxydoréduction est l'addition d'une oxydation et d'une réduction (de manière à simplifier les électrons).
L'équation d'une oxydoréduction s'écrit de la manière suivante : Ox1 + Réd2 = Ox2 + Réd1, avec Ox1 / Réd1 et Ox2 / Réd2 des couples oxydant-réducteur.Quelles sont les réactions d'oxydation ?
Une réaction d'oxydation est une réaction chimique au cours de laquelle un élément subit une perte d'électrons.
Cette perte d'électrons est due à la présence d'oxygène, ou d'une autre substance ayant des propriétés chimiques semblables, dans les réactifs.- II : COUPLES OXYDANT-REDUCTEUR
suivant que nous sommes en présence d'atomes de Fe ou d'ions Ag .
En généralisant : Cu2+ et Cu forment un couple d'oxydoréduction noté Ox/Red, ils sont dits conjugués et on représente ce couple par Cu2+/Cu.
|
Réactions doxydation et de réduction
Le carbone brûle avec une flamme jaune et des étincelles pour former le dioxyde de carbone La réaction de l'oxyde de cuivre(II) avec l'hydrogène. |
|
Ré visions sur lé bilan duné transformation chimiqué Exércicés sur
Écrire l'équation de réaction. 2. Vrai ou faux ? A : A la fin de la transformation chimique l'oxyde de cuivre et le carbone ont entièrement |
|
Exercices sur la réaction chimique NII
b) Calculer la masse molaire moléculaire du dioxyde de carbone e) Quelle masse de cuivre obtient-on par la réaction de 1 kg d'oxyde de cuivre ? Donner. |
|
CORRECTION DU TP N°6
VI Réaction entre l'oxyde de cuivre et le carbone : Schéma de l'expérience légendé : a. Il se forme progressivement un solide rougeâtre sur les parois du |
|
Le composite cuivre / nanofibres de carbone
22-Apr-2009 brune caractéristique de la présence d'oxyde de cuivre CuO (figure 2). ... De plus l'absence de réaction chimique entre C et Cu lors de la ... |
|
Http://physiquechimie.sharepoint.com Wahab Diop lycee Limamou
L'oxyde de cuivre réagit avec le carbone selon l'équation: CuO + C ? Cu + CO2. 1) Équilibrer l'équation de la réaction. 2) Sachant que le carbone est en |
|
ANNALES SCIENCES PHYSIQUES 3ème
Dans cette réaction CuO est réduit par le carbone (le carbone a été oxydé par l'oxyde de cuivre). Le carbone est le réducteur et l'oxyde de cuivre est |
|
Chapitre 6 : Réactions doxydoréduction - Objectifs
Réaction entre l'oxyde de cuivre(II) et le carbone réaction redox. 2 oxyde de dioxyde carbone cuivre cuivre(II) de carbon. |
|
Sujets de Sciences Physiques du D.E.F
b) Montre que la réaction est une réaction d'oxydo - réduction. 2°) Application Numérique : On fait un courant d'oxyde de carbone sur 64 g d'oxyde de cuivre |
|
Feuille dexercices n°1 Équilibrer les équations bilans : C3H8 + Cl2
Ex 2 : L'oxyde de cuivre (II) CuO réagit avec le carbone pour donner du cuivre et du dioxyde de carbone. L'équation de la réaction est 2 CuO + C ? 2 Cu + CO2. |
|
Oxyde de cuivre (Ii) Propriétés préparation réactions chimiques
La réaction entre l’oxyde de cuivre II et le carbone est une réaction chimique Elle se traduit par cette équation bilan : 2CuO + C 2Cu + CO 2 1 4 Notion d’oxydant et de réducteur Dans la réaction ci-dessus l’atome de carbone arrache à l’oxyde de cuivre II ses atomes d’oxygène : le |
|
Chapitre 6 : Oxydoréduction et bilan de matière Cours
-l’oxyde de cuivre est constitué d’ions Cu2+ et O2?-Le carbone est constitué d’atomes C -Le cuivre est constitué d’atomes Cu -Le dioxyde de carbone est constitué d’atomes de carbone ayant gagné des charges positives alors les atomes d’oxygène sont porteurs de charges négatives Ainsi l’ion Cu2+ gagne 2 électrons pour |
|
1 Réaction entre oxyde de de cuivre CuO (s) et Carbone C(s)
1 Réaction entre oxyde de de cuivre CuO (s) et Carbone C(s) On dispose d’un mélange oxyde de cuivre carbone Chauffer fortement un tube à essais contenant une pointe de spatule du mélange de réactifs relié par un tube à dégagement à un tube à essais contenant de l’eau de chaux |
|
Searches related to reaction oxyde de cuivre et carbone PDF
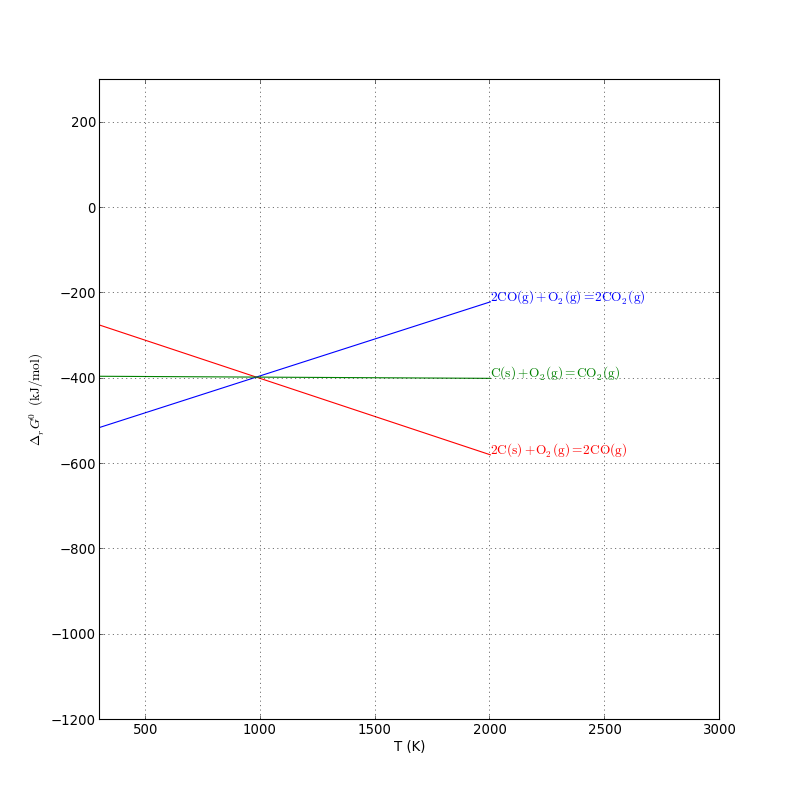
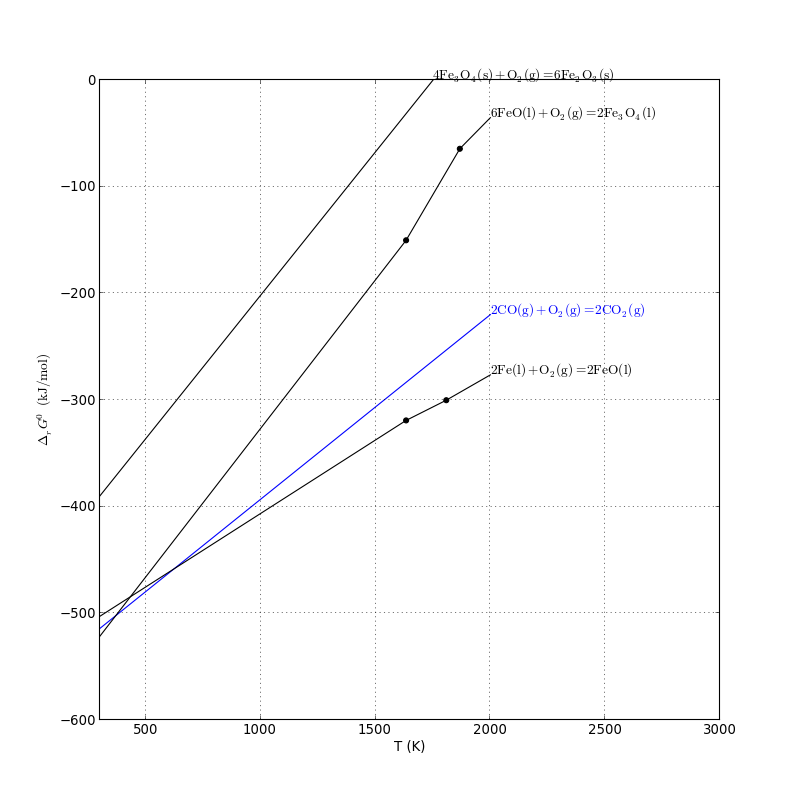
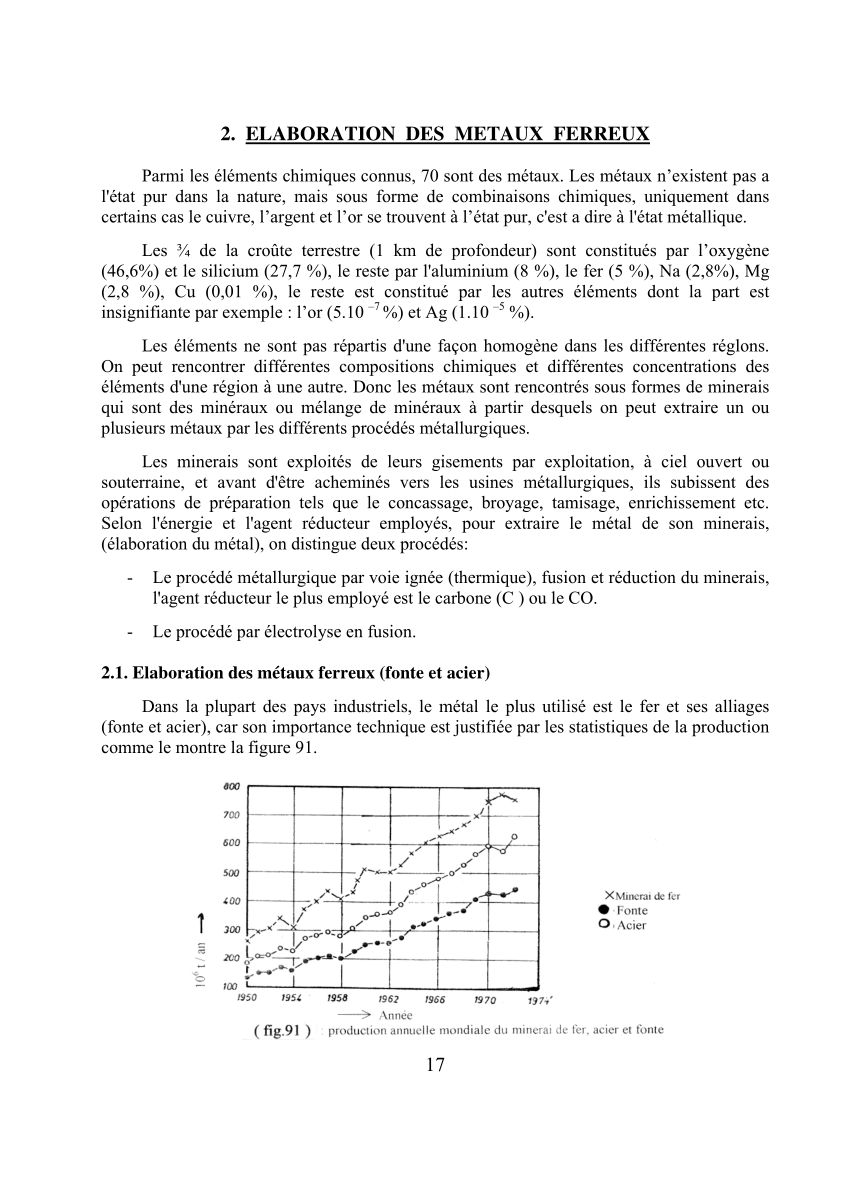
1 À haute température l’oxygène de l’air réagit avec le coke (carbone impur) pour former du monoxyde de carbone (gaz incolore toxique) : 2C +O2 ?? 2CO 2 Le monoxyde de carbone réduit l’oxyde de fer en fer : Fe2O3 +3CO ?? 2Fe+3CO2 Le fer liquide (fonte = fer impur) se rassemble en bas du haut-fourneau Le laitier liquide |
Comment calculer la réaction de cuivre et de l'oxyde de carbone ?
La réaction produit du cuivre et eau. CuO + C ? Cu + CO (t = 1200 oC). La réaction a produit du cuivre et de l'oxyde de carbone. SiO + 2S ? Cu + ?2? (t = 150-200 oC). La réaction se déroule sous vide. La réaction a produit du cuivre et de l'oxyde de soufre.
Comment fonctionne la réaction de l’oxyde de cuivre ?
La réaction de l’oxyde de cuivre(II) avec l’hydrogène +Chau?ée dans un ?ux d’hydrogène, la poudre noire d’oxyde de cuivre(II) se transforme enpoudre de cuivre rouge. De l’eau s’est formée qui se condensesur les parties froides de la paroi dutube. CuO+H2??Cu+H2O La réaction l’oxyde de fer(III) avec l’hydrogène
Quelle est la différence entre le dioxyde de carbone et le cuivre ?
Mais en y regardant de plus près, on constate que la réponse E a une différence cruciale. Le dioxyde de carbone est un oxyde non métallique par opposition à l’oxyde de cuivre, l’oxyde de sodium, l’oxyde de magnésium et l’oxyde de calcium, qui sont tous des oxydes métalliques.
Quelle est la différence entre l'oxyde cuivrique et le carbone ?
On dit que l'oxyde cuivrique s'est réduit et que le carbone s'est oxydé. Le passage de l'oxyde cuivrique au cuivre est appelé réduction : le carbone est le réducteur ou le corps oxydé. Le passage du carbone au dioxyde de carbone est une oxydation : l'oxyde cuivrique est l'oxydant ou le corps réduit.
| 1 Réaction entre oxyde de de cuivre CuO (s) et Carbone C(s) |
| Réactions d’oxydation et de réduction |
| Chapitre 6 : Oxydoréduction et bilan de matière Cours |
| Série des exercices sur les réactions d’oxydo-réduction 1BIOF |
| Exércicés sur la transformation chimiqué |
| Notion de la réaction chimique |
| Searches related to reaction oxyde de cuivre et carbone filetype:pdf |
Quelle équation représente l'oxydation du cuivre ?
. Cette réaction se nomme oxydation.
. Le cuivre est appelé réducteur, car c'est lui qui donne des électrons.
Comment s'appelle l'oxydation du cuivre ?
. Dans les faits, le rôle de l'oxydant est souvent joué par l'oxygène.
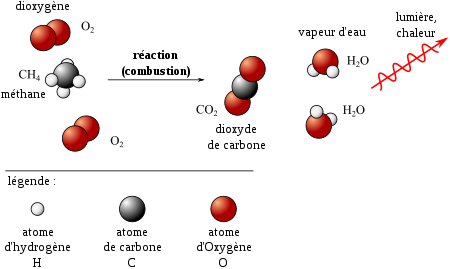
. Ainsi, dans la réaction chimique qui implique le carbone et l'oxygène, par exemple, il y a formation de dioxyde de carbone par oxydation.
Quelles sont les réactions d'oxydation ?
. Ce procédé s'applique néanmoins principalement aux minerais oxydés.