titrage hcl par naoh
|
8—Titration*of*Acids*andbases*
Standardization of the sodium hydroxide solution is accomplished by titrating 25 00 mL of a HCl solution of known concentration Your instructor will demonstrate the technique for pipetting exactly 25 00 mL HCl into the Erlenmeyer flask Rinse your buret twice with about 5 mL of the NaOH solution |
|
A Guide to Titration
(i) between a solution of a strong acid (HCl) and a solution of a strong base (NaOH) (ii) between a solution of a weak acid (acetic acid CH 3 COOH) and a solution of a strong base (NaOH) 1 2 Equivalence Point End Point and Choice of Indicator An acid-base titration is complete when exactly the right amount of base has been added to react |
|
Dosage de l’acide chlorhydrique par titrage acidobasique
HCl (le titré) est titré avec une solution de NaOH (le titrant) : NaOH (1) (aq) + HCl (aq) ® NaCl (aq) + H 2 O (l) il faut arrêter le titrage dès qu'il ne reste plus de HCl à faire |
|
§ 7 (suite) Titrages acide-base
Dans le cas particulier du titrage d’une acide fort (HCl par exemple) par une base forte (NaOH par exemple) : – pour 0 < ! < 1 il y a un excès d’acide et le pH est donné par pH ≈ – log (c / c0) ⇒ pH = – log { c a⋅(1– !)· V 0 / [c0· (V 0 + V titr)] } = – log { c a⋅(1– !)· \"a / c0 } |
Comment titrage-t-on une solution d'un acide faible ?
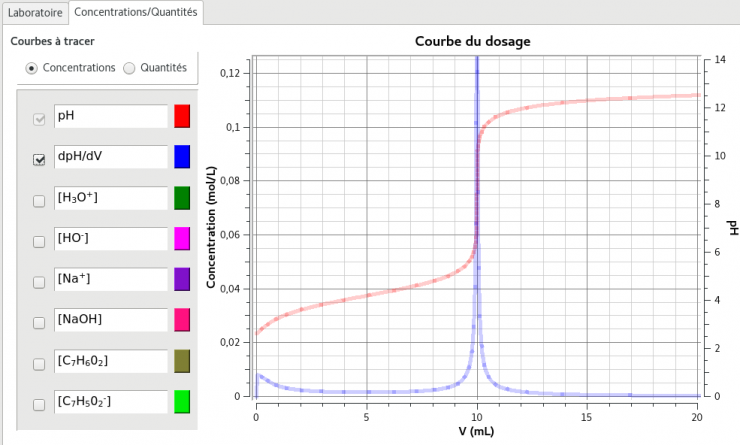
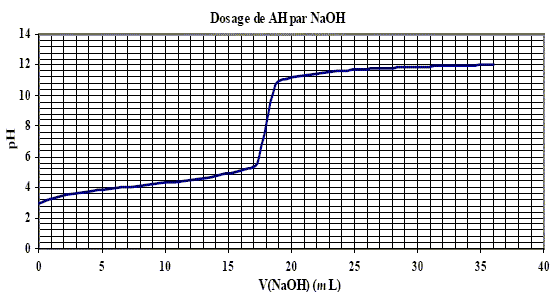
Considérons le titrage d’une solution d’un acide faible, tel que l’acide acétique par exemple, par une base forte, comme NaOH. La fonction pH = ƒ(!) dans ce cas est du 3e degré. Les approximations présentées jusqu’ici s’appliquent toutefois aux différents domaines de la courbe : – Pour ! = 0 , l’acide faible est pur.
Quel est le point d'équivalence du titrage d'une base forte par un acide fort ?
Dans le cas du titrage d’une base forte par un acide fort, la courbe de neutralisation varie lentement pendant l’addition de l’acide, puis présente une partie quasi-verticale pendant laquelle le pH change brusquement de plusieurs unités. Le pH du point d’équivalence est encore égal à 7.
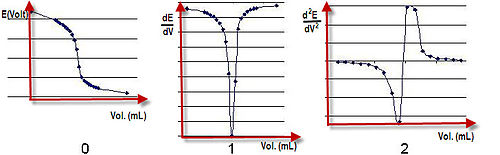
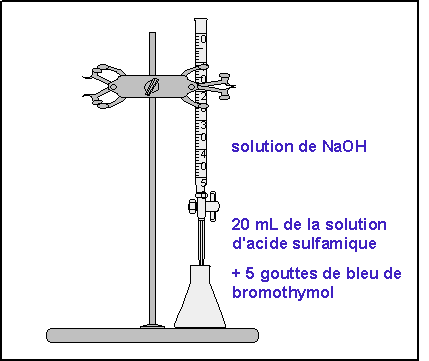
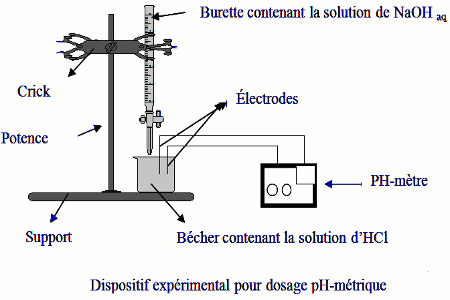
Comment mesurer le pH d’un titrage acide-base ?
Le pH à chacun de ces points est généralement différent de 7. Lors d’un titrage acide-base, on détecte le point d’équivalence (fin de la réaction de neutralisation) en mesurant le pH à l’aide d’un pH-mètre ou en employant un indicateur coloré qui change de couleur dans une zone de pH donnée.
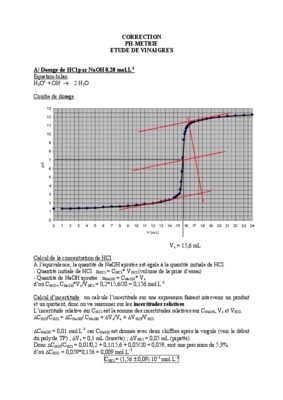
Quelle est la valeur de la concentration obtenue par la méthode de titrage ?
2.4. Pour estimer l'incertitude sur la valeur de la concentration obtenue par cette méthode de titrage, l'expérimentateur est amené à reproduire un grand nombre de fois la même manipulation dans les mêmes conditions. Un des titrages réalisés donne une valeur de concentration très élevée en ions Fe2+ par rapport aux autres.

Titration of HCl vs NaOH Volumetric Analysis Class 11 Titration Technique

HCl-NaOH Titration (pH)

Titration: Practical and Calculation (NaOH and HCl)
|
Cours de Chimie - Informatique Titrage acide/base
17 avr. 2013 Table 1 Calcul du nombre de moles HCl dans la solution titrée. Le volume de solution NaOH à ajouter pour atteindre la neutralité est donc. |
|
1 TP Nº2 (Semestre 1) : Dosage dune base forte (NaOH) par un
TP Nº2 (Semestre 1) : Dosage d'une base forte (NaOH) par un acide fort (HCl). 1. Introduction : Les réactions acido-basiques résultent du transfert d'un |
|
Labo théorique : Dosage de lacide chlorhydrique par titrage
La concentration de HCl est calculée en considérant qu'au point d'équivalence le nombre de moles de. NaOH (de la solution titrante) ajouté est égal au nombre de |
|
TRAVAUX PRATIQUES DE CHIMIE I
Chapitre III : Vérification de la concentration d'une solution de HCl préparée par un dosage acido-basique Dosage de la solution préparée par NaOH … |
|
TP CH …… :Titrage pH métrique (dosage de HCl par NaOH)
:Titrage pH métrique (dosage de HCl par NaOH). Lors d'un titrage acido-basique on peut utiliser le pH comme grandeur observable. La tracé de la courbe. |
|
TP 3 -Titrage dun acide fort et acide faible par une base forte (NaOH)
Le titrage est une technique de dosage utilisée en chimie analytique afin de déterminer la Titrage d'un acide fort HCl par une base forte NaOH. |
|
1 CORRECTIF EXERCICES EN CHIMIE SUR LES TITRAGES (6
Volume de la solution de NaoH = 01 L. INCONNUE : Ca = C HCl ? FORMULE : Ca = . RESOLUTION : Cb ? C NaOH = n. |
|
Labo théorique : Dosage de lacide chlorhydrique par titrage
La concentration de HCl est calculée en considérant qu'au point d'équivalence le nombre de moles de. NaOH (de la solution titrante) ajouté est égal au nombre de |
|
TP CHIMIE-1 & TP CHIMIE-2
HCl acide chlorhydrique j joule. H2SO4 acide sulfurique Titrer le NaOH jusqu'au point d'équivalence (fermeture du robinet). |
|
LABORATOIRES CHIMIE 2 UE : Chimie 2
colorimétrique. Première série de titrages. • Préparation d'une solution de base NaOH par dissolution. • Titrage par une solution d'acide chlorhydrique HCl. |
|
Lab Practical: Acid-Base Titration - University of Illinois
b) The standardized solution of NaOH (part a) is used to titrate a solution of HCl Write the balanced equation for this reaction Calculate the molarity of the HCl solution if it requires 13 50-mL of NaOH to titrate 15 0-mL HCl solution to the endpoint c) Finally the standardized solution of NaOH (part a) is used to titrate a solution of |
|
Labo théorique : Dosage de l’acide chlorhydrique par titrage
HCl (le titré) est titré avec une solution de NaOH (le titrant) : NaOH (1) (aq) + HCl (aq) ® NaCl (aq) + H 2 O (l) il faut arrêter le titrage dès qu'il ne reste plus de HCl à faire réagir À ce |
|
TP 3 -Titrage d’un acide fort et acide faible par une base
TP 3 -Titrage d’un acide fort et acide faible par une base forte (NaOH) But:-Détermination de la concentration des solutions d’acides chlorhydrique et acétique par la méthode du titrage (colorimétrie et PH-metrie) Principe : Le titrage est une technique de dosage utilisée en chimie analytique afin de déterminer la concentration |
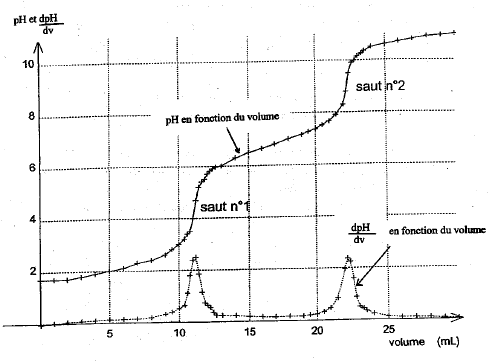
Comment calculer le titrage de l’acide triprotique avec du NaOH ?
Par exemple, le titrage de l’acide triprotique H3PO4 avec du NaOH est illustré sur la figure 6.3.6 et présente deux étapes bien définies : le premier point médian correspond au pKa1, et le second point médian correspond au pKa2.
Comment calculer le titrage d’acide ?
Pour ces deux titrages, le nombre de moles d’acide initial présent est de 0,00500 mol (0,100 molL-1 x 0,0500 L). Le du titrage se produit lorsque la quantité de base ajoutée est égale à la quantité d’acide initial.
Quelle courbe de titrage pour l’acide phosphorique ?
Courbe de titrage pour l’acide phosphorique (H3PO4), un acide polyprotique typique. La courbe pour le titrage de 25,0 ml d’une solution de H3PO4 0,100 M avec du NaOH 0,100 M ainsi que les espèces en solution à chaque Ka est présentée.
Comment fonctionne le titrage d’un acide fort avec une base forte ?
Le titrage (a) d’un acide fort avec une base forte et (b) d’une base forte avec un acide fort (a) Comme du NaOH 0,20 M est lentement ajouté à 50,0 ml de HCl 0,10 M, le pH augmente lentement au début, puis très rapidement à l’approche du point d’équivalence, et enfin augmente lentement une fois de plus.
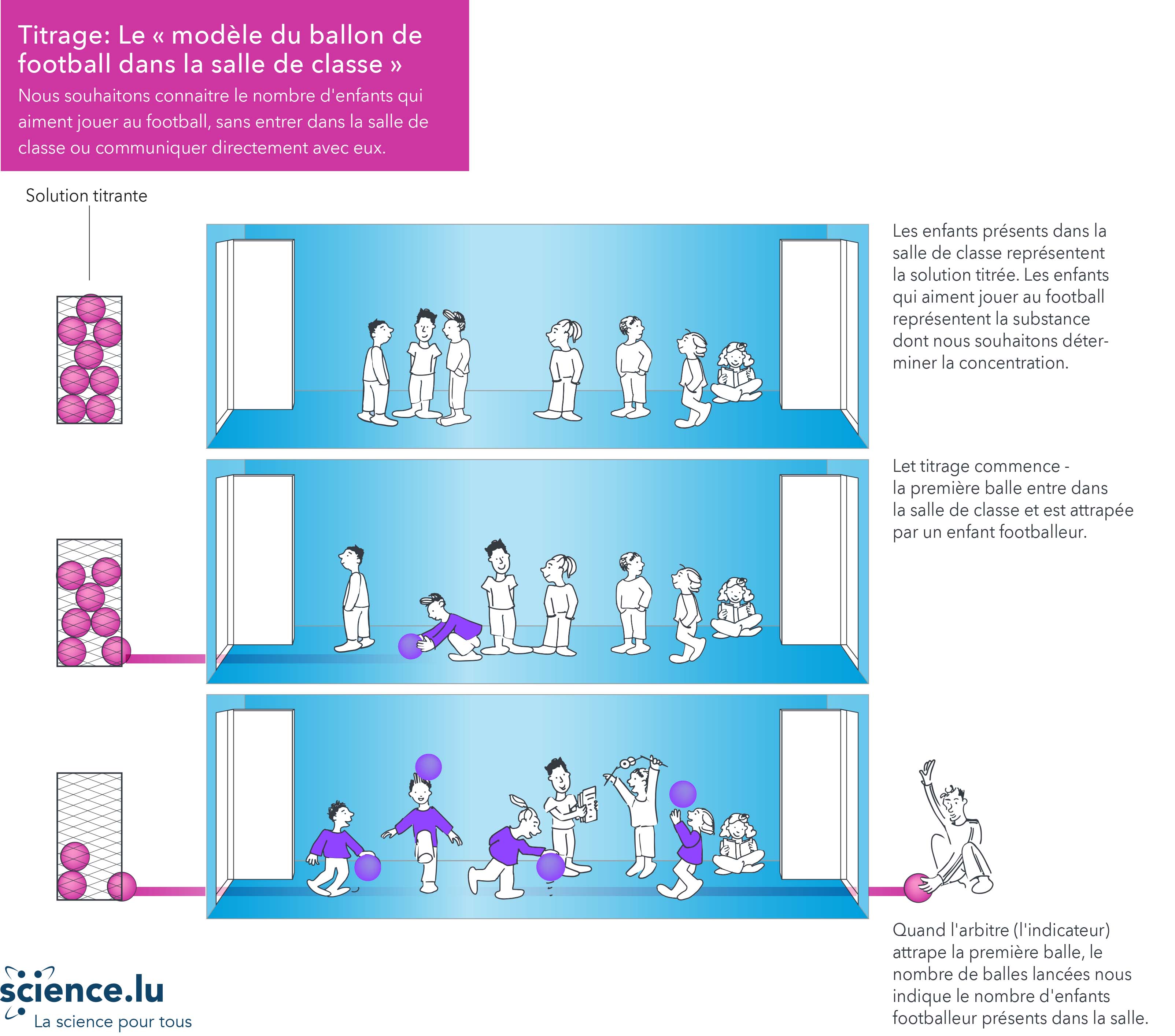
Comment doser une solution de NaOH par une solution de HCl ?
Comment écrire une réaction de titrage ?
. NH3(aq) + H3O+(aq) = NH4+(aq) + H2O pour le dosage d'une solution d'ammoniac par une solution d'acide fort.
Comment titrer un acide ?
Quelle est l'équation de la réaction entre l'acide chlorhydrique et l hydroxyde de sodium ?
. La réaction globale est la suivante: Na+ + OH- + H+ + Cl- <--> H2O + NaCl (sel de table).
|
TP 3: Acides et Bases
5 oct 2007 · Enfin, la troisième partie est le titrage de l'acide acétique en solution pur ou complété par du HCl ou du NaOH (acide et base forts) à des |
|
TP CH :Titrage pH métrique (dosage de HCl par NaOH)
:Titrage pH métrique (dosage de HCl par NaOH) Lors d'un titrage acido-basique, on peut utiliser le pH comme grandeur observable La tracé de la courbe |
|
TRAVAUX PRATIQUES DE CHIMIE I - Université Ibn Khaldoun de
Préparation de 100 mL d'une solution de NaOH 0,01 N à partir de la solution mère Chapitre III : Vérification de la concentration d'une solution de HCl préparée par un dosage acido- Chapitre IV : Titrage de l'acidité totale d'un lait |
|
E 1 FICHE GENERALE - AC Nancy Metz
NaCl E 4 TITRAGE DU THIOCYANATE DE POTASSIUM 5 mL de HCL au 1/ 2 2 NaOH + 2 HCl 2 H2O + 2 NaCl SECURITE : HCl : C R34-37 S26-45 |
|
Dosage pH-métrique dun acide fort par une base forte
Figure 72 : effet de dilution sur la courbe de titrage acide fort - base forte 93 Figure 122 : évolution du pH au cours de titrage de HCl par NaOH |
|
1) Principes et objectifs 2) Mode opératoire 3) Titrage dun acide fort
3) Titrage d'un acide fort par une base forte On titre une solution d'acide chlorhydrique HCl dans le bécher, par de la soude NaOH à 0 1 mol L-1 |
|
Les titrages acido-basiques en Terminale S - Aix - Marseille
3 mai 2007 · expérimentale pour laquelle le titrage acido-basique est toujours un grand classique chaque 5 Exploitation de la courbe de titrage pH = f(V ) |
|
1 CORRECTIF EXERCICES EN CHIMIE SUR - collège saint-louis
L'indication fournie par le fabricant (0,833 mol/L) est donc très proche de celle obtenue par titrage (0,827 mol/L) 9) DONNEES : NaOH (aq) + HCl → NaCl (aq) + |
|
Principe : Le dosage Le dosage Le dosage Partie I : Manipulations
On souhaite vérifier la quantité d'ions H3O+ présents dans une solution d'acide chlorhydrique HCl à 0,1mol L-1 à l'aide d'une solution titrante de soude NaOH |