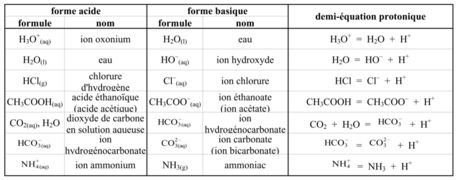
ion oxonium et hydroxyde
|
Evidence for Oxonium Ions in Ethereal “Hydrogen Chloride”
Evidence for Oxonium Ions in Ethereal “Hydrogen Chloride” CorinC WagenandEricN Jacobsen DepartmentofChemistryandChemicalBiologyHarvardUniversityCambridgeMassachusetts02138UnitedStates ABSTRACT:Althoughsolutionsofhydrogenchlorideinetherealsolventslikediethyletherordioxanearecommonlyem-ployedinthelaboratory |
|
Oxonium ions for easy aryne chemistry
Oxonium ions for easy aryne chemistry Joanna Wencel-Delord Triaryloxonium salts are used as aryne precursors under mild and operationally simple conditions allowing high functional- group |
|
PARTIE II : COMPRENDRE Chapitre 13
• Dans toute solution aqueuse il y a simultanément présence d’ions hydroxyde HO – et d’ions oxonium H 3O + (ou hydronium) • La valeur du pH d’une solution aqueuse est directement liée à la concentration des ions oxonium : pH = - log [H3O +] |
What is a primary oxonium ion?
Those with n = 1 are called primary oxonium ions, an example being protonated alcohol (e.g. methanol ). In acidic media, the oxonium functional group produced by protonating an alcohol can be a leaving group in the E2 elimination reaction. The product is an alkene. Extreme acidity, heat, and dehydrating conditions are usually required.
Does Oxatriquinane react with water?
Oxatriquinane and oxatriquinacene are unusually stable oxonium ions, first described in 2008. Oxatriquinane does not react with boiling water or with alcohols, thiols, halide ions, or amines, although it does react with stronger nucleophiles such as hydroxide, cyanide, and azide .
What is an example of a pyramidal oxonium ion?
Oxygen is usually pyramidal with an sp 3 hybridization. Those with n = 1 are called primary oxonium ions, an example being protonated alcohol (e.g. methanol ). In acidic media, the oxonium functional group produced by protonating an alcohol can be a leaving group in the E2 elimination reaction. The product is an alkene.
How oxonium ions are formed in acidic media?
In acidic media, the oxonium functional group produced by protonating an alcohol can be a leaving group in the E2 elimination reaction. The product is an alkene. Extreme acidity, heat, and dehydrating conditions are usually required. Other hydrocarbon oxonium ions are formed by protonation or alkylation of alcohols or ethers (R−C− + O −R 1 R 2 ).
|
CORRECTION EXERCICE C9
Lorsqu'on dilue la solution la concentration en ions oxonium diminue et celle des ions hydroxyde augmente. n°13 p°335 L'acide des fourmis. |
|
Documents de Physique-Chimie – M. MORIN 1
ion ammonium / ammoniac. NH4. + / NH3 ion oxonium / eau. H3O+ / H2O eau / ion hydroxyde. H2O / OH- dioxyde de carbone dissous / ion hydrogénocarbonate. |
|
Chapitre C4 cours
(ion oxonium) prédomine le BBT change de couleur et devient bleu. solution d'hydroxyde de sodium ou dans toute autre solution basique : (c'est aux ... |
|
Chapitre 3 15 Ions dérivés de leau 1.Lhydrogène se trouve dans la
de l'ion H3O+. Le schéma de la molécule de l'ion oxonium est donc : b. Dans l'ion hydroxyde un des doublets liants de l'oxygène devient non liant |
|
RÉACTIONS ACIDO-BASIQUES
Le pH et la concentration en ions oxonium H3O+ varient en sens inverse du pH d'une solution permet de calculer sa concentration en ion hydroxyde. |
|
Fiche 4 : Titrage par suivi conductimétrique
En ajoutant une goutte de soude on ajout des ions hydroxyde qui réagissent avec les ions oxonium présents |
|
[H3O ] = 10
Déterminer la concentration en ion oxonium ou hydroxyde connaissant le pH. Ce qu'il faut savoir. ? Il faut d'abord déterminer la concentration en ions |
|
Quelques notions de conductimétrie
On peut procéder par exemple |
|
H2O + H2O = H3O + HO Ke = [H3O ] × [HO ] . H2O + H2O = H3O +
Produit ionique de l'eau. On définit le produit ionique Ke de l'eau comme le produit des concentrations molaires effectives des ions oxonium et hydroxyde :. |
|
RÉACTIONS ACIDO-BASIQUES
Le pH et la concentration en ions oxonium H3O+ varient en sens inverse : lorsque [H3O+] augmente le pH de la solution diminue et inversement Ex : - si [H3O+] |
|
Ch 1 acides bases
L-1 (la concentration effective en ions oxonium) le pH est sans unité Caractéristiques : La réaction donne autant d'ions oxonium que d'ions hydroxyde |
|
Chapitre 3
Concentration en ions oxonium dans un soda de pH = 35 : Par définition [H3O + (aq)] = 10-pH L'acide cède un proton à l'ion hydroxyde : CH3 – COOH |
|
Les réactions acido-basiques
oxonium H3O+ appartenant au couple H3O+(aq) / H2O(l) Les solutions d'hydroxyde de sodium ou de potassium contiennent en très grande quantité l'ion |
|
Documents de Physique-Chimie – M MORIN 1
ion ammonium / ammoniac NH4 + / NH3 ion oxonium / eau H3O+ / H2O eau / ion hydroxyde H2O / OH- dioxyde de carbone dissous / ion hydrogénocarbonate |
|
Ion hydroxyde HO - StephBill
CATIONS ANIONS NOM FORMULE NOM FORMULE Ion oxonium H3O+ (aq) Ion hydroxyde HO- (aq) Ion ammonium NH4 + (aq) Ion sulfate SO4 2- (aq) Ion |
|
Activite documentaire
Dans une solution aqueuse les concentrations molaires volumiques en ions oxo- nium et en ions hydroxyde sont calculables à partir du pH mesuré : [H3O+] = 10-PH |
|
Chap 1 la securite chimique dans lhabitat
La base conjuguée de l'eau H2O est l'ion hydroxyde HO- L'acide conjugué de l'eau H2O est l'ion oxonium H3O+ L'eau H2O est acide dans le couple H2O/HO |
|
Chapitre 1 Acides et bases
où H3O+ est l'ion hydronium ou oxonium aussi appelé “proton hydraté” puisqu'il s'agit d'un proton (H+) attaché à une molécule d'eau La concentration [H3O+] |
|
+ H3O+ Réactions acide-base - Notion dé - PhysiqueChimie
Toutes les solutions aqueuses contiennent des ions oxonium H3O+ et des ions hydroxyde HO- Réactions acide-base - Notion d'équilibre chimique |
Comment calculer H3O+ avec OH ?
? Si on a une solution basique, on connaît [HO-]. Il faut calculer [H3O+] par la relation [H3O+]x[HO-]=10-14 d'ou [H3O+] = 10-14 [HO-] Puis, on applique la formule.Quelle est la relation entre H3O+ et le pH d'une solution aqueuse ?
Le pH d'une solution est défini comme l'opposé en signe du logarithme décimal de l' activité des ions H3O+ présents dans la solution : pH = - log aH3O+.Comment évolue le pH et la concentration en ions oxonium ?
Et ainsi de suite jusqu'à la concentration [H3O+] = 10-14 mol. L-1 où pH = 14. Ainsi, plus la concentration en ions oxonium est faible, plus le pH augmente et plus la solution est basique. Inversement, plus la concentration en ions oxonium est importante, plus le pH diminue et plus la solution est acide.- Si on nous demande de calculer le pH, il faut utiliser la relation pH = –log([H3O+]). Si on nous demande de calculer la concentration en quantité de matière d'ions oxonium, il faut utiliser la relation [H3O+] = 10–pH.
Quels sont les ions oxonium ?
Comment trouver H3O+ avec OH ?
. Il faut calculer [H3O+] par la relation [H3O+]x[HO-]=10-14 d'ou [H3O+] = 10-14 [HO-] Puis, on applique la formule.
Comment se forme l'ion oxonium ?
Quelle est la relation qui lie le pH au pOH ?
|
[H3O ] = 10
Déterminer la concentration en ion oxonium ou hydroxyde connaissant le pH Ce qu'il faut savoir ➢ Il faut d'abord déterminer la concentration en ions oxonium |
|
CORRECTION EXERCICE C9 - Sciences Physiques et Chimiques
Lorsqu'on dilue la solution, la concentration en ions oxonium diminue et celle des ions hydroxyde augmente n°13 p°335 L'acide des fourmis 13 1 Le pH d' une |
|
RÉACTIONS ACIDO-BASIQUES - Sciences Physiques et Chimiques
Le pH et la concentration en ions oxonium H3O+ varient en sens inverse : lorsque du pH d'une solution permet de calculer sa concentration en ion hydroxyde |
|
CATIONS ANIONS NOM FORMULE NOM FORMULE Ion oxonium
CATIONS ANIONS NOM FORMULE NOM FORMULE Ion oxonium H3O+ (aq ) Ion hydroxyde HO- (aq) Ion ammonium NH4 + (aq) Ion sulfate SO4 2- |
|
11,7 7 6,7 3,3 210 1,010 210 510 10 5,010 210 Basique Neutre
En déduire la concentration en ion Oxonium de cette solution 1 HNO3 donne 1 Il y a-t-il des ions Hydroxyde dans la solution préparée ? Si oui ; quelle est |
|
Réactions acido-basiques - Free
Ajouter maintenant quelques gouttes d'hydroxyde de sodium (0,1 mol L-1) Le proton H+ initialment présent sur l'ion oxonium est capturé par la molécule |
|
Chp 6 reaction chimique par echange de proton eleve bis
Comment évolue le pH d'une solution si la concentration en ions oxonium H3O Ecrire l'équation de la réaction entre les ions oxonium et les ions hydroxyde |
|
Dosage dune solution aqueuse dhydroxyde de - Nicole Cortial
molaires en ions oxonium, 3 H O + et en ions hydroxyde, HO − attendues pour cette solution 3° question : a) Écrire l'équation de la réaction de dosage |
|
ACIDE/BASE ET
finale des ions oxonium et établir un tableau d'avancement du système chimique → la solution d'hydroxyde de sodium dans le bécher et relever le pH après |
|
Cours 2 Force dun acide - Physik & Chimie avec Mme Tournaire
Lors de cette dissolution il y a toujours apparition d'ions oxonium H3O+ Une solution aqueuse d'hydroxyde de sodium (Na+ + HO-‐) est préparée par |










![New Compounds Oxonium Salts of Khellin - [PDF Document] New Compounds Oxonium Salts of Khellin - [PDF Document]](https://0.academia-photos.com/attachment_thumbnails/44102981/mini_magick20190215-22357-ptb0tg.png?1550223000)