concentration molaire h3o+
|
Calculating the [H3O ] [OH ] pH and pOH in Aqueous
1 The concentration of hydroxide ions OH–(aq) in a solution at 25°C is 0 150 mol/L Determine the concentration of hydronium ions H3O+(aq) in the solution 2 A solution of lithium hydroxide LiOH(aq) is made by placing 2 00 mol of the base into 1 50 L of solution |
How do you calculate H3O ion concentration?
Net [H+]=10 -pH Also [H + ] = [H 3 O + ] because a single H + combines with a single water molecule to give H3O+ without involving OH - as you did in attempt 2. The pH is close to 7. So the hydronium ion concentration of water can't be neglected. [H3O+fro water + H3O+ from acid] [OH-]=10^-14
What is the chemical formula for H3O & H2O?
Its concentration relative to hydroxide is a direct measure of the pH of a solution. It can be formed when an acid is present in water or simply in pure water. It's chemical formula is H 3O +. It can also be formed by the combination of a H + ion with an H 2O molecule.
How does dilution affect molarity?
Dilution is the addition of solvent, which decreases the concentration of the solute in the solution. In both dilution and concentration, the amount of solute stays the same. This gives us a way to calculate what the new solution volume must be for the desired concentration of solute. From the definition of molarity,
Is HNO3 a stoichiometric solution?
Although Ka for HI is about 108 greater than Ka for HNO3, the reaction of either HI or HNO3 with water gives an essentially stoichiometric solution of H3O + and I− or NO − 3. In fact, a 0.1 M aqueous solution of any strong acid actually contains 0.1 M H3O +, regardless of the identity of the strong acid.
Overview
0 energy points In this video, we'll solve for [H₃O⁺] and pH in two different worked examples. First, we'll walk through the possible approaches for calculating [H₃O⁺] from pOH. Then, we'll find the pH of pure water at 50°C from the value of the autoionization constant at 50°C. Created by Jay. khanacademy.org
Want to join the conversation?
Log in khanacademy.org

La concentration molaire Sciences et technologies Alloprof

Calculer la concentration molaire en ions H3O+ oxonium hydronium

Calculer une concentration massique et molaire Exercice Chimie
|
CORRECTION EXERCICE C9
La concentration molaire en ions oxonium H3O+ est liée au pH de la solution S : [H3O+] = 10-34 = 4 |
|
H2O + H2O = H3O + HO Ke = [H3O ] × [HO ] . H2O + H2O = H3O +
On définit le produit ionique Ke de l'eau comme le produit des concentrations molaires effectives des ions oxonium et hydroxyde : Ke = [H3O. |
|
Acides et Bases en solution aqueuse
L-1 => [H3O+] = = 3°. Définition du pH : La concentration molaire en ions hydronium d'une solution aqueuse détermine son caractère acide |
|
Chapitre 16 – Théorie de Brönsted. Notion déquilibre chimique
Le pH du suc gastrique vaut 15 ; la concentration en ions H3O+ y est donc Une masse m d'hydroxyde de sodium de masse molaire M contient une quantité. |
|
DÉTERMINATION DE CONCENTRATIONS DIONS PAR
Relation entre quantités et concentrations pour les espèces H3O contenant des ions Xi de concentration [Xi ] et de conductivité molaire ionique ?i une. |
|
PH = - log [H3O+] [H3O+] = 10-pH ? = xf / xmax
La relation liant le pH à la concentration en ions oxonium est : Inversement : [H3O+]est la concentration molaire en ion oxonium en mol.L-1. |
|
TD1 : Acides et bases
5. a) La concentration [H3O+] est donnée par le pH de cette solution : où cHCl = nHCl/1L est la concentration molaire de la solution commerciale. |
|
Classe de Ter Spé ?? Cours n°2 « Analyser un système chimique
a- pH et concentration molaire des ions oxonium H3O+: L'acidité ou la basicité d'une solution dépendent des valeurs des concentrations en ions oxonium H3O+. |
|
PH ET CONCENTRATION EN ION H3O+
L'objectif de cette activité est d'apprendre à mesurer le pH d'une solution acide et à en déduire sa concentration en ions H3O+ 1 ) DÉFINITION ET MESURE |
|
Log [H3O+] [H3O+] = 10-pH ? = xf / xmax - physique chimie terminale S
Un acide : c'est une espèce chimique qui peut perdre un proton H+ (à savoir ? CH3COOH acide [H3O+]est la concentration molaire en ion oxonium en mol |
|
Chimie des solutions 1 - Cours et applications - Allophysique
Il est lié à la concentration molaire en ions H3O+ en solution par la relation : pH = -log(H3O+) Dans une solution aqueuse il y a des ions H3O + et des |
|
Acides et Bases en solution aqueuse
La concentration molaire en ions hydronium d'une solution aqueuse détermine son caractère acide basique ou neutre Le pH d'une solution est égal à la |
|
Le pH et sa mesure - LEtudiant
Lorsque le pH augmente la concentration molaire en ions oxonium de la solution aqueuse [H3O +] diminue ? Le pH d'une solution aqueuse est fonction de sa |
|
IIILeau
La concentration molaire réelle d'une espèce chimique notée [ ] se calcule en divisant le nombre de moles de cette espèce ( « le soluté » ) effectivement |
|
Calculer la concentration en ions H3O+ ou en ions OH- à partir du
Avis 45 |
|
Calculer la concentration en ion H3O+ à partir du pH - TS - Kartable
Avis 45 |
|
Exercice 2 : « Concentration en soluté et pH »
Déterminer la concentration en ion oxonium H3O+ de chacune de ces eaux Concentration en ion oxonium : [H3O + ] = 10 –pH |
|
TS Chimie Détermination dune constante dacidité par deux
b) Calculer les concentrations molaires finales des espèces chimiques majoritaires D'après l'équation modélisant la réaction : [H3O+]éq = [CH3CO2 -]éq |
Comment calculer la concentration molaire de H3O+ ?
Si on nous demande de calculer le pH, il faut utiliser la relation pH = –log([H3O+]). Si on nous demande de calculer la concentration en quantité de matière d'ions oxonium, il faut utiliser la relation [H3O+] = 10–pH.Quelle est le nombre de moles d'ion H3O+ ?
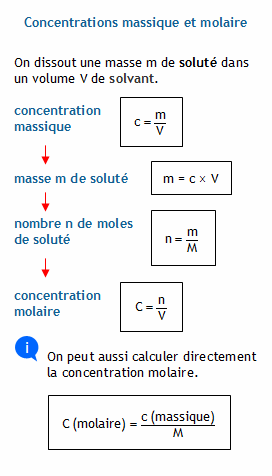
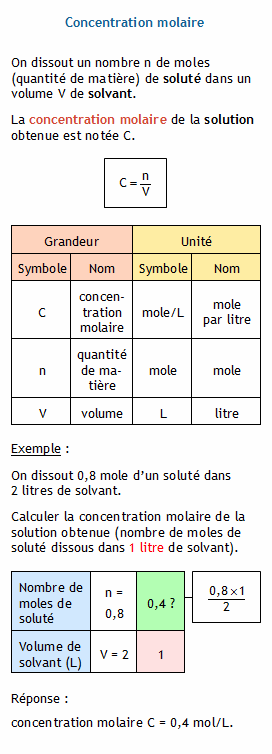
L'équation pour la concentration molaire est �� = �� �� , où �� est la quantité de matière du soluté en moles, �� est la concentration molaire exprimée typiquement en moles par litre et �� est le volume de la solution, typiquement exprimé en litres.Comment on peut calculer la concentration molaire ?
Formule du pH
Remarque : le signe - devant le logarithme indique tout simplement que le pH et la concentration en ions oxonium [H3O+] ont une relation inversée : quand la concentration en ions oxonium augmente, alors le pH diminue.
Comment calculer la concentration molaire de H3O+ ?
. Si on nous demande de calculer la concentration en quantité de matière d'ions oxonium, il faut utiliser la relation [H3O+] = 10–pH.
Comment calculer la molarité des ions H3O+ ?
. L-1 , l'activité n'ayant pas de dimension (contrairement à la concentration ).
. Acidité d'une solution : On a vu que dans l'eau pure à 25°C, aH3O+ = 10-7 et donc le pH de l'eau pure à 25°C est 7.
Quelle est la concentration en ions H3O+ ?
. Si le pH est connu, on peut calculer la concentration des ions oxonium en solution.
. Une solution a un pH égal à 3,5.
Comment on calcule la concentration molaire ?
|
Télécharger le support de cours en Pdf - Chimie Générale et
Une solution est dite neutre, acide ou basique suivant le rapport des concentrations en ions H3O+ et OH- La concentration molaire en ions H3O+ dans une |
|
CORRECTION EXERCICE C9 - Sciences Physiques et Chimiques
La concentration molaire en ions oxonium H3O+ est liée au pH de la solution S : [ H3O+] = 10-3,4 = 4,0 10-4 mol L-1 L'avancement final de la réaction est : x |
|
IIILeau
Calculons la concentration molaire de l'eau (considérée comme soluté ) mol H3O + et 10 -7 mol OH - Il restera 55,36-0,0000002 moles H2O non dissociées |
|
[H3O ] = 10
Il faut d'abord déterminer la concentration en ions oxonium par la relation [H3O + ] = 10 -pH ➢ Puis, connaissant [H3O+], on va déterminer la [HO-] par la |
|
ACIDE - BASE en solution aqueuse
On caractérise l'acidité ou la basicité d'une solution par la concentration molaire de cette solution en ions H3O+ (ions hydronium) La relation est vérifiée par la |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
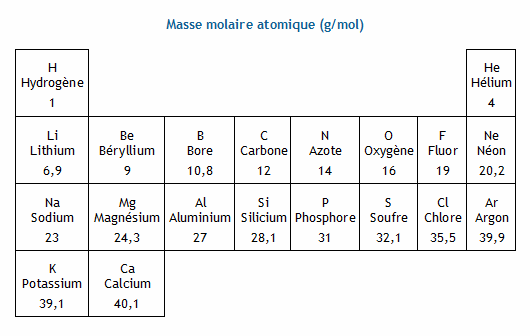
La masse molaire d'un atome est la masse d'une mole d'atomes acide dans l' eau comme le nombre de mol d'ion H3O+ susceptible d'être libérés par un litre |
|
Filière Sciences de la Matière Chimie Cours Chimie des Solutions
La concentration molaire d'une espèce chimique en solution CA est la quantité de acide dans l'eau comme le nombre de mol d'ion H3O+ susceptible d'être |
|
Acides et Bases en solution aqueuse
[OH-] = 10-4 mole L-1 => [H3O+] = = 3° Définition du pH : La concentration molaire en ions hydronium d'une solution aqueuse détermine, son caractère acide, |
|
11,7 7 6,7 3,3 210 1,010 210 510 10 5,010 210 Basique Neutre
[H3O+] en mol/L = 10-pH = 10-14 / [ HO-] Déterminez la concentration molaire de l'acide nitrique dans cette solution Concentration en ion oxonium : [H3O |