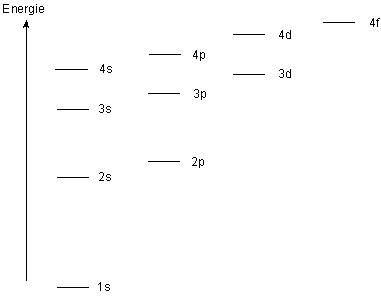configuration electronique oxygene
Comment se forme l'ion O2 ?
. Sa configuration électronique est donc (K)2(L)6 donc il lui manque 2 électrons pour compléter sa couche externe L et respecter la règle de l'octet: L'atome d'oxygène forme deux liaisons.
Quel est l'atome possédant la structure électronique 1s2 2p2 2p6 3s2 3p2 ?
. L'oxygène peut alors obtenir 2 charges négatives.
|
La configuration électronique, les cases quantiques et les
Pour l'oxygène, la configuration électronique est: 1s22s22p4 C'est-à-dire que 2 électrons pour l'oxygène sont dans le premier niveau - premier sous niveau, 2 |
|
Corrigé
atomiques pour obtenir la configuration électronique d'un atome L'oxygène va facilement gagner 2 électrons afin d'acquérir la configuration stable semblable |
|
Chapitre 3 :Structure électronique des atomes
Chapitre 3 : Structure électronique des atomes Structure de la matière Page 1 sur 5 I Nombres quantiques A) Origine théorique La résolution de l'équation de |
|
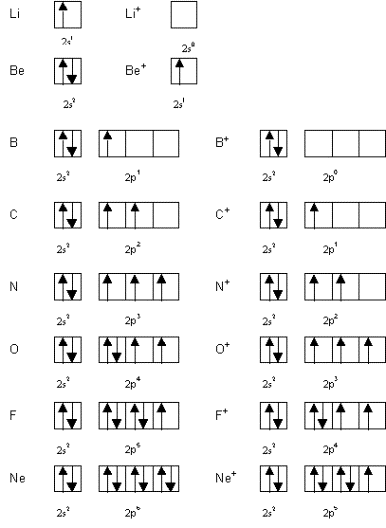
CONFIGURATION ÉLECTRONIQUE DES ÉLÉMENTS LA
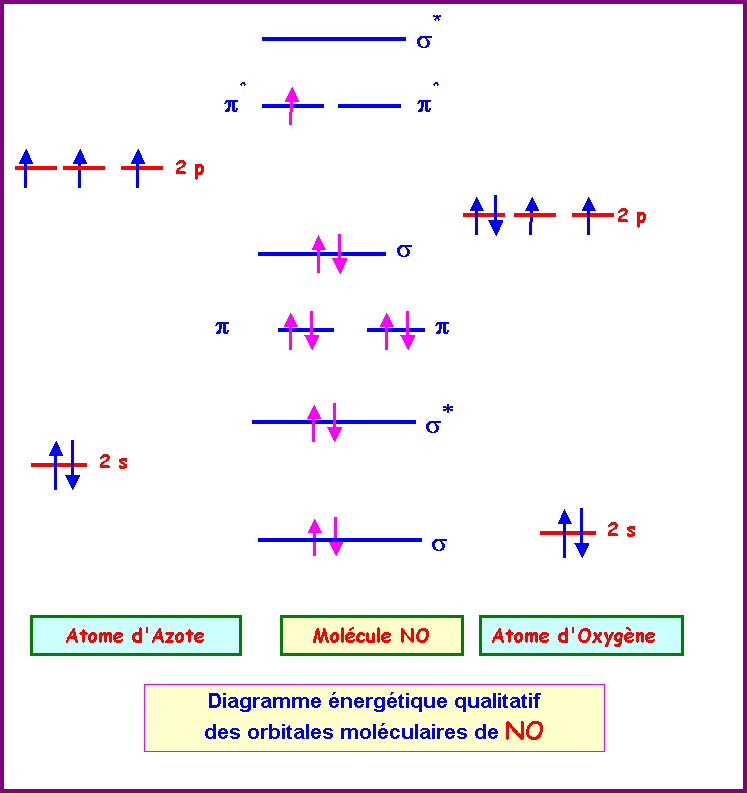
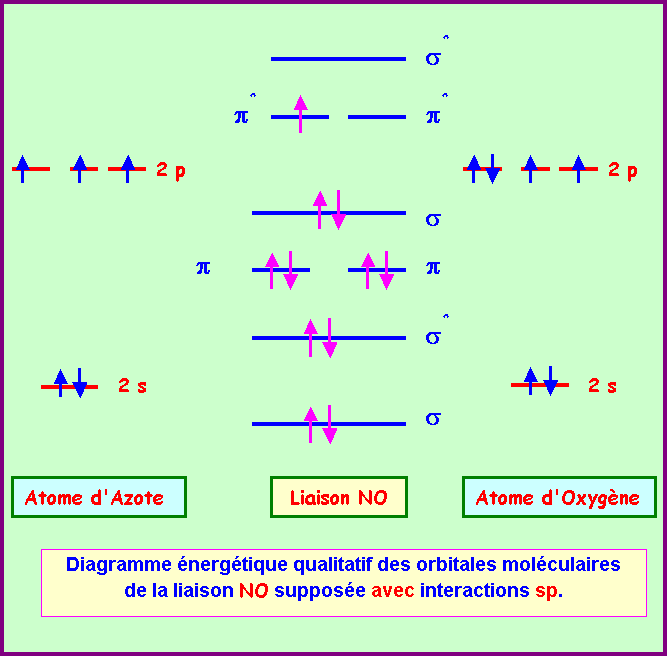
Si la configuration de gauche était la bonne, l'azote atomique serait monovalent et l'oxygène atomique aurait des propriétés différentes de celles que nous lui |
|
Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points
3 mar 2020 · Exercice 1 : (4 points) configuration (ou structure) électronique d'un atome Oxygène Période 3 Couche n = 3 Al Aluminium S Soufre Cl |
|
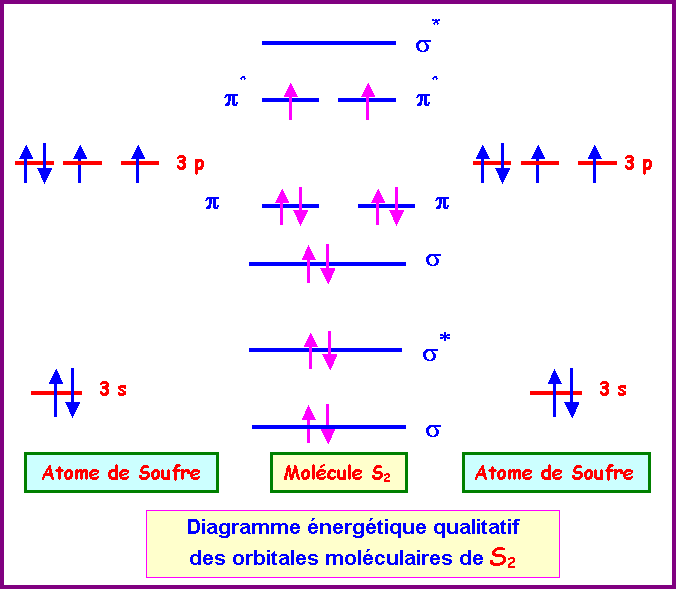
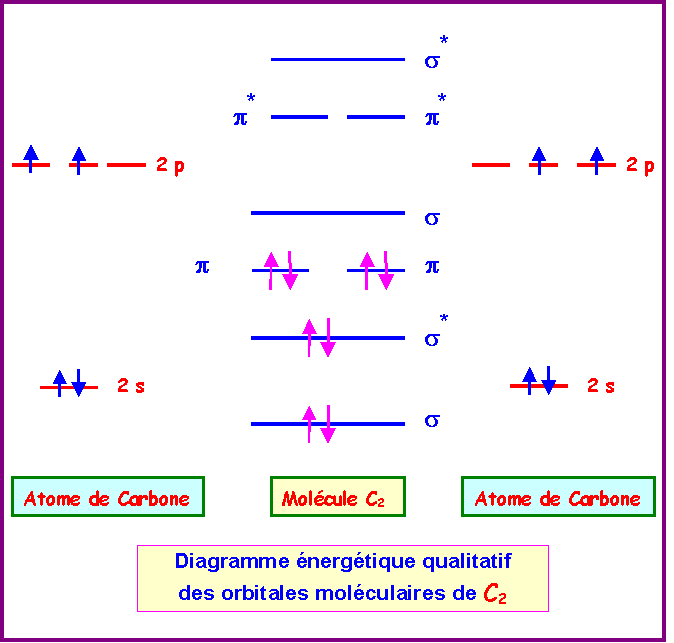
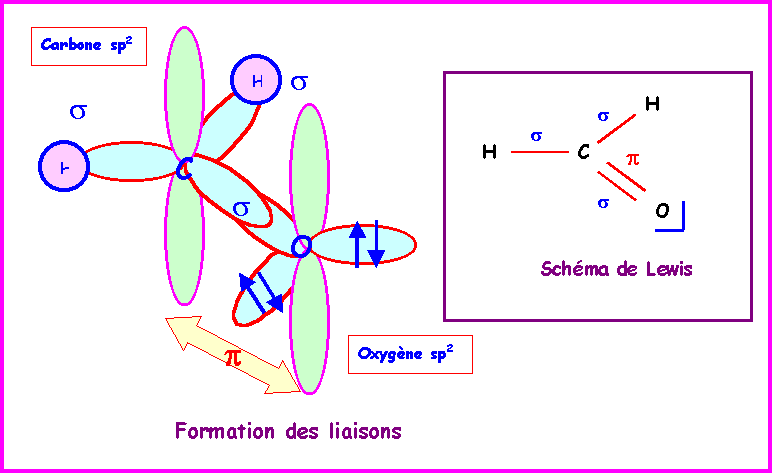
Modélisation moléculaire
L'oxygène fournit 2 électrons au système π 6 2 3 Halogènes Les halogènes ont pour configuration électronique ns2np5 (où n est le nombre quantique |
|
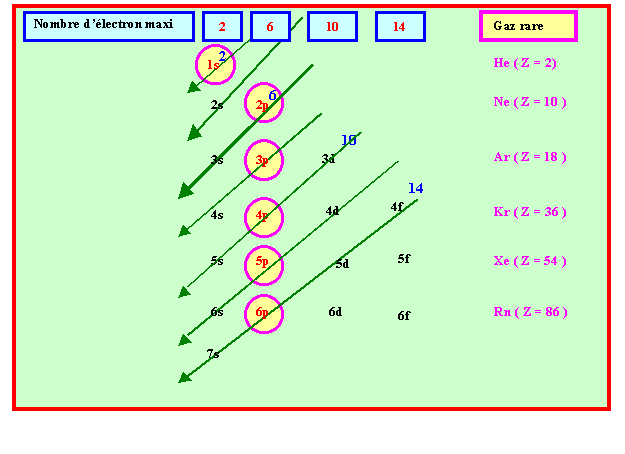
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
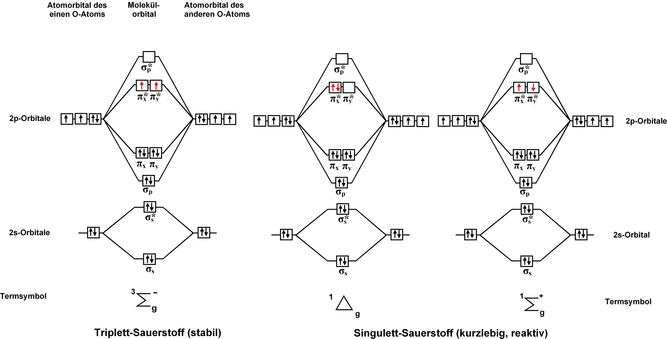
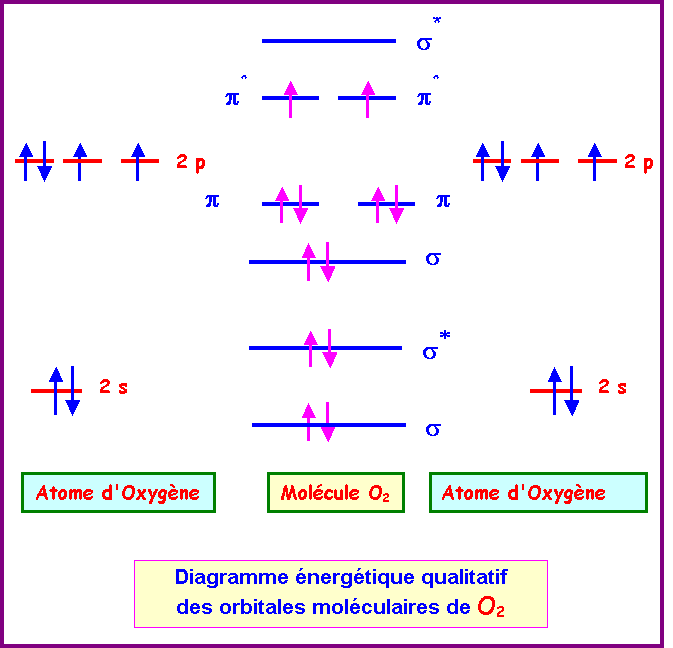
former des molécules de manière à atteindre la configuration électronique de type Il existe des exceptions à cette règle notamment l'oxygène de l'air O2 que |
|
CORRIGE - lutesupmcfr
Oxygène et chlore vont former préférentiellement les ions O2 − et Cl − qui ont la configuration électronique du gaz rare qui les suit dans la classification |
|
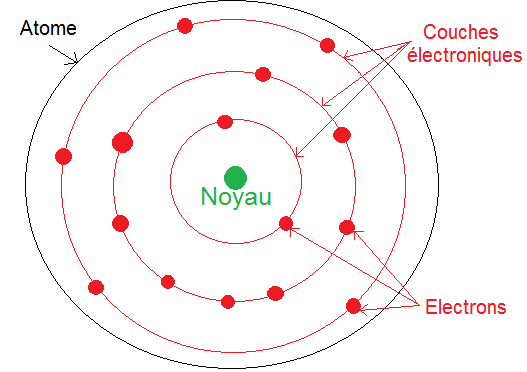
LA STRUCTURE ELECTRONIQUE DES ATOMES
Les trois premières couches, seules utiles au lycée, s'appellent (K), (L) et (M) ➁ Chaque couche possède un certain nombre de « places » Toutes les places ne |