CO3 H2CO3 HCO3
|
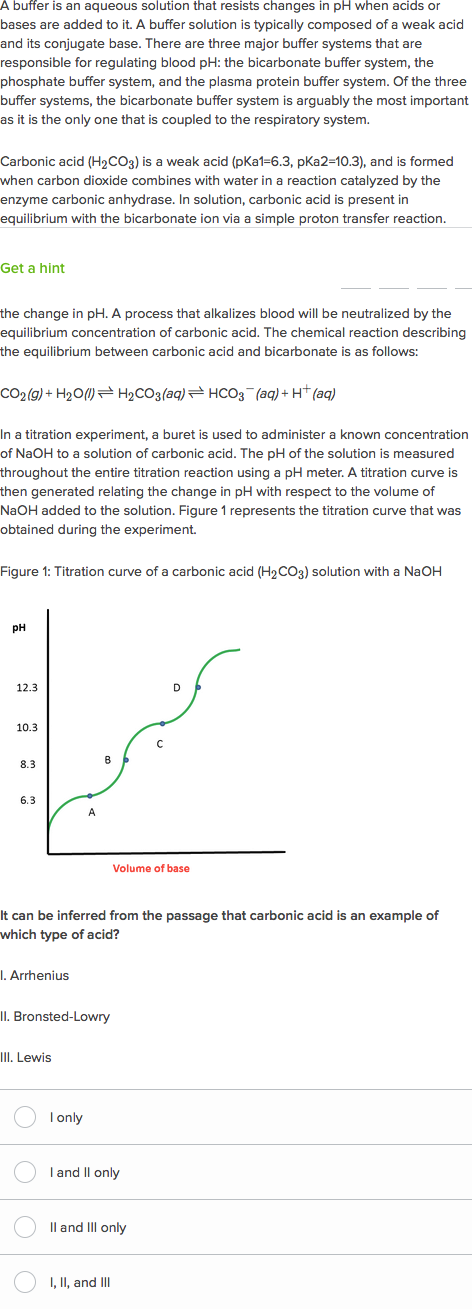
CO2 + H2O ↔ H2CO3 ↔ H+ + CO3
↔ H+ + CO3- PH = Pk + log HCO3- H2CO3 H+ = Ka x 0 03 x PaCO2 (40) H2CO3 = 0 03 x PaCO2 (40) HCO3- (24 à28) Equilibre constant grâce système tampons rein |
|
Equilibre acidobasique
pH = 610 + log [HCO3 - ] / [H2CO3] Page 7 pH = 61 + log [HCO3-] apCO 2 ▫[HCO3 -] = composante métabolique et rénale ▫ pCO2 = composante pulmonaire |
|
CO2 / H2CO3 / HCO3
- / CO3 HCO3 - (bicarbonate) et CO3 2- (carbonate) Il se forme en particulier dans l'eau par solvatation du dioxyde de carbone : CO2 (aq) + H2O(l) H2CO3 |
|
Les réactions acido-basiques
CO2H2O(aq) = HCO3 -(aq) + H+ 3) Pour les bases fortes Les solutions d'hydroxyde de sodium ou de potassium -(aq) / CO3 2-(aq) HCO3 -(aq) = CO3 2-(aq) + |
|
COMMENT ÉCRIRE UN COUPLE ACIDE‑BASE ?
CO2 H2O ou H2CO3 : dioxyde de carbone dissous ou acide carbonique HCO3 – : ion hydrogénocarbonate CO3 2– : ion carbonate |
|
Chapitre 1 Acides et bases
– vaut 64 à 25◦C couple HCO3 – / CO3 2– : CO3 2– + H+ = HCO3 – couple H2O / HO– : H2O = HO– + H+ CO3 2– + H2O ⇌ HCO3 – + HO– Le pKa du couple HCO3 |
|
Chimie équilibres acido-‐basique
3 mar 2015 · Quand la solution devient saturée en H2CO3 le gaz CO2 s'échappe de -‐ : pKA1 = 6 HCO3-‐ / CO3 2-‐ : pKA2 = 10 masses molaires en g mol |
|
ACIDIFICATION DE LOCÉAN
Le CO2 dissous réagit avec l'eau : CO2 + H2O H2CO3 L'acide carbonique se dissocie : H2CO3 HCO3 - + H + L'ion bicarbonate aussi : HCO3 - CO3 2- + H |
|
Équilibre calco-carbonique en termes physico-chimiques
28 jui 2017 · H2CO3 + OH- ---->HCO3 - + H2O HCO3 - + OH----->CO3 2- + H2O 1/2(pK1 HCO3- CO3-- Les formes de l'acide carbonique Répartition des |
|
TEMA 6. Química de las aguas naturales. Procesos ácido-base en
H2CO3 + CO3. 2‒. 2HCO3. ‒ que a tenor de la 'realidad' química de las especies [H2CO3] = [HCO3. ‒][H+] / Ka = 14 ⨯ 10‒5 M. Así pues |
|
Hidrologia USAL
H2CO3 ⇄ HCO3. – + H+. (2). Y finalmente |
|
SISTEMA DE CARBONATOS
[HCO3¯]. [CO2]. = 4.45 ∗ 10. −7. pK a1. =6.35. HCO. 3. -. H+ + CO. 3. 2-. K 2. = H. + • CT |
|
TEMA 3. EQUILIBRIOS ACIDO–BASE
atm ⇒ C TCO3 ≠cte |
|
El dióxido de carbono como forma sostenible de reducir el pH del
Por todo ello las diferentes formas de carbono inor- gánico que se pueden encontrar en el agua son CO2. (incluyendo H2CO3) |
|
TEMA 2
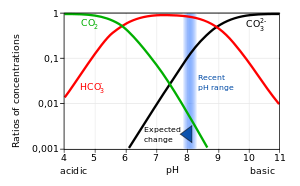
H2CO3. * ↔ HCO3. - ↔ CO3. = K1 = ---- ; K2 = ----. Como se aprecia en la gráfica a pH = 3 la especie predominante es H2CO3; a pH = 8 es HCO3. - y a pH = 13 es |
|
Investigación - Determinación del estado de equilibrio de un
un conjunto de ecuaciones la relación del Ca2+ |
|
1 Chapter 12: Acids and Bases: Ocean Carbonate System James
30 abr 2001 CO3. 2- = α2 CT. The derivations of the equations are as follows: αο = H2CO3 / CT = H2CO3 / (H2CO3 + HCO3 + CO3). = 1 / ( 1+ HCO3/H2CO3 + CO3/ ... |
|
Tema 8: Ácidos y bases
4.En la reacción H2CO3 + H2O → HCO3. –. + H3O. +. identifica las especies que 9.Identifica el ácido conjugado del CO3. 2– en la reacción: CO3. 2–. + H2PO4. |
|
EL USO DE LA ECUACIÓN DE HENDERSON- HASSELBALCH
H2CO3 D HCO3. - + H+. Keq = 1.58 x 10-4. pK = 3.8. -------------------------. CO2 + H2O D HCO3. - + H+. Keq = 7.9 x 10-7 pK = 6.1. La constante de equilibrio |
|
9 chemistry of carbonic acid in water
dissolved carbonic acid H2CO3 with a = [H2CO3] + [CO2aq] dissolved bicarbonate |
|
CO3 H2CO3 HCO3
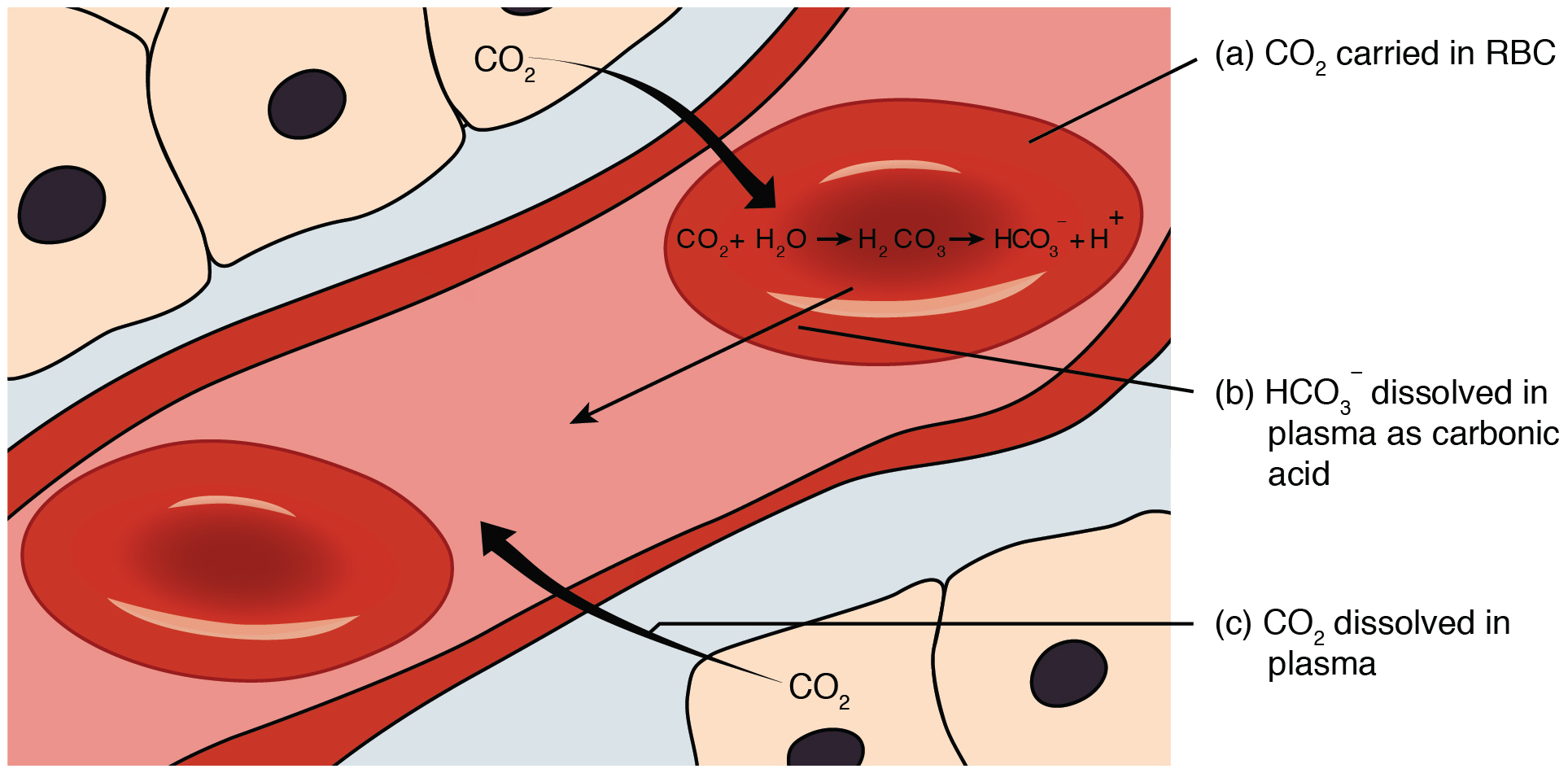
(05) Le dioxyde de carbone (CO2) forme de l'acide carbonique H2CO3 qui |
|
PH dune solution de carbonate de sodium
Calculer le pH d'une solution de carbonate de sodium 0.0012 M (pKa1 (H2CO3/HCO3. -) = 6.30 ; pKa2 (HCO3. -/CO3. 2-) = 10.33). • Espèces présentes :. |
|
CO2 + H2O ? H2CO3 ? H+ + CO3- PH = Pk + log HCO3- H2CO3
H+ + CO3-. PH = Pk + log HCO3-. H2CO3. H+ = Ka x 0.03 x PaCO2 (40). H2CO3 = 0.03 x PaCO2 (40). HCO3- (24 à28). Equilibre constant grâce système tampons |
|
ACIDIFICATION DE LOCÉAN
H2CO3. - = acide carbonique. HCO3. - = ion bicarbonate. CO3. 2- = ion carbonate. H + = ion hydrogène. Le CO2 dissous réagit avec l'eau : CO2 + H2O H2CO3. |
|
10 CHEMISTRY OF CARBONIC ACID EQUILIBRIA IN WATER
CO2 dissous (noté CO2aq) acide carbonique dissous H2CO3 avec a = [H2CO3] + [CO2aq] bicarbonate dissous |
|
PH dune solution de dioxyde de carbone
Calculer le pH d'une solution de dioxyde de carbone 0.025 M (pKa1 (H2CO3/HCO3. -) = 6.3 ; pKa2 (HCO3. -/CO3. 2-) = 10.33). CO2 + H2O ? H2CO3. |
|
Retour pH dun mélange dune solution de carbonate de sodium et d
6.30 ; pKa2 (HCO3 CO3. 2- H3O+ |
|
PH dune solution dhydrogénocarbonate de sodium
CO3. 2- H3O+ |
|
Exercice exoph17r
6.30 ; pKa2 (HCO3. -/CO3. 2-) = 10.33). • Espèces présentes : OH- H2CO3 |
|
CO3 H2CO3 HCO3
2 1 (0,5) H2CO3(aq) + H2O(l) ⇆ HCO3 – (aq) + H3O+ (aq) 2 2 (0,5) Le dioxyde de carbone (CO2) forme de l'acide carbonique H2CO3 qui, en réagissant |
|
CO2 + H2O ↔ H2CO3 ↔ H+ + CO3- PH = Pk + log HCO3- H2CO3
H+ + CO3- PH = Pk + log HCO3- H2CO3 H+ = Ka x 0 03 x PaCO2 (40) H2CO3 = 0 03 x PaCO2 (40) HCO3- (24 à28) Equilibre constant grâce système |
|
ACIDIFICATION DE LOCÉAN
H2CO3 - = acide carbonique HCO3 - = ion bicarbonate CO3 2- = ion carbonate Le CO2 dissous réagit avec l'eau : CO2 + H2O H2CO3 L'acide |
|
Résumé Introduction
Les groupes carboxyliques du PAA peuvent se dissocier ainsi : COOH COO H Dissociation des carbonates dans l'eau : H2CO3 HCO3 H HCO3 CO3 2- H |
|
PH dune solution de carbonate de sodium - Umtice
Calculer le pH d'une solution de carbonate de sodium 0 0012 M (pKa1 (H2CO3/ HCO3 -) = 6 30 ; pKa2 (HCO3 -/CO3 2-) = 10 33) • Espèces présentes : |
|
PH dune solution de dioxyde de carbone - Umtice
Calculer le pH d'une solution de dioxyde de carbone 0 025 M (pKa1 (H2CO3/ HCO3 -) = 6 3 ; pKa2 (HCO3 -/CO3 2-) = 10 33) CO2 + H2O → H2CO3 |
|
Examen du 28 mai 2009 - durée : 2 heures - lutesupmcfr
Le pH du sang est tamponné par le couple H2CO3/HCO3 - Dans le sang d'une c) Calculer la concentration de l'espèce CO3 2- Montrer qu'elle est |
|
10 CHEMISTRY OF CARBONIC ACID EQUILIBRIA IN WATER
acide carbonique dissous, H2CO3 avec a = [H2CO3] + [CO2aq] bicarbonate dissous, HCO3 − avec b = [HCO3 −] carbonate dissous, CO3 2− avec c = [ CO3 |
|
Chimie équilibres acido-‐basique
Quand la solution devient saturée en H2CO3, le gaz CO2 s'échappe de la on peut envisager la réaction : 2 HCO3 -‐ CO3 2-‐ + CO2(aq) ⎯⎯→←⎯⎯ |
|
Acidification de Locéan - UNESCO
CO3 2- = ion carbonate H + = ion hydrogène Le CO2 dissous réagit avec l'eau : CO2 + H2O H2CO3 L'acide carbonique se dissocie : H2CO3 HCO3 |












![Solved: 2] PKa Of Carbonic Acid H2CO3 Is 636(3 Marks Solved: 2] PKa Of Carbonic Acid H2CO3 Is 636(3 Marks](https://s1.studylibfr.com/store/data/001344353_1-33bc73391dffeeb52c201d54f4a904f2.png)





![Co2 + H2o ↔ H2co3 ↔ H+ Hco3- [j3no2mr5e34d] Co2 + H2o ↔ H2co3 ↔ H+ Hco3- [j3no2mr5e34d]](https://static.docsity.com/documents_pages/2012/12/23/a2df437ecd6921504c224369fe608ffa.png)