procedure d'enregistrement des medicaments en algerie
|
LA POLITIQUE PUBLIQUE DU MEDICAMENT EN ALGERIE
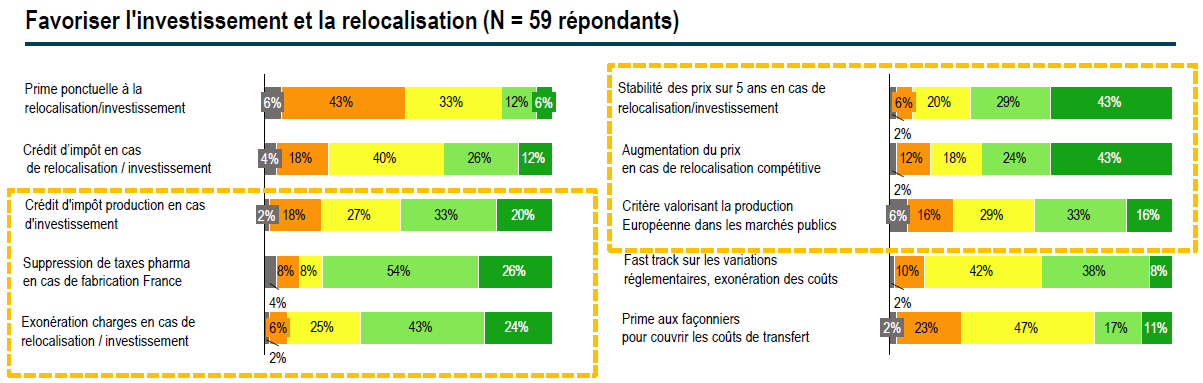
De même la lenteur et la longueur des procédures d'enregistrement et d'approbation des programmes d'importation déstabilisent l'approvisionnement du marché |
|
Dossier dAMM
25 fév 2016 · La demande d'enregistrement d'un médicament en Algérie est adressée à la direction des produits pharmaceutiques du Ministère de la Santé de la |
|
Lenregistrement dun médicament générique en Algériepdf
1 jan 1995 · Le dossier d'AMM contient tous les éléments concernant le médicament des informations sur le cycle de développement la qualité pharmaceutique |
|
12 Joumada El Oula 1442
27 déc 2020 · — La présentation du dossier d'enregistrement sous le format CTD est applicable à toute demande d'enregistrement d'une demande de renouvellement |
|
Autorisation de mise sur le marché
FIGURE 2: PROCESSUS D'ENREGISTREMENT D'UN MEDICAMENT EN ALGERIE Le dossier technique est élaboré par le fabricant plus précisément par une équipe composée |
|
AMMpdf
Les documents du dossier d'AMM « Format CTD » sont présentés en 5 Modules : - Module 1 : Dossier administratif - Module 2 : Résumés de qualité non cliniques |
|
ENREGISTREMENT DUN MÉDICAMENT GÉNÉRIQUE FABRIQUÉ
8 oct 2014 · Procédure en Algérie : décision d'enregistrement FIGURE 1: PROCESSUS D'ENREGISTREMENT D'UN MEDICAMENT EN ALGERIE Page 22 ENREGISTREMENT D'UN |
|
JOURNAL OFFICIEL
14 juil 2021 · 2020 fixant la composition du dossier d'enregistrement des médicaments à usage de la médecine humaine Art 14 — Le présent arrêté sera |
|
24 Rabie El Aouel 1443
31 oct 2021 · — La demande d'enregistrement est déposée auprès de l'agence nationale des produits pharmaceutiques par le pharmacien directeur technique de l' |
Un laboratoire qui souhaite commercialiser un médicament doit déposer une demande d'autorisation de mise sur le marché auprès d'une agence du médicament.
Elle repose sur un dossier d'évaluation établi à partir des données précliniques et cliniques issues des précédentes phases de développement.
Comment faire l'inventaire des médicaments ?
Chaque mois, il faut réaliser un inventaire pour chaque produit.
Il faut recompter les boîtes des produits en stock, convertir le nombre obtenu en unités de compte, comparer le résultat à l'existant des fiches de stock puis mettre celles-ci à jour.
Comment enregistrer un médicament en Algérie ?
La demande d'enregistrement d'un médicament produit en Algérie est adressée à la direction de la pharmacie (DP) du Ministère de la Santé, de la Population et de la Réforme Hospitalière (MSPRH) (cf. figure2). d'exploitation, ainsi que la validation des sites de production et des laboratoires de contrôle.
Quels sont les acteurs des produits pharmaceutiques en Algérie ?
La Pharmacie Centrale des Hôpitaux (PCH).
Le Ministère de la Santé, de la Population et de la Réforme Hospitalière (MSPRH).
L'Agence National des Produits Pharmaceutiques (ANPP).
L'Institut Pasteur d'Algérie (IPA).
|
Autorisation de mise sur le marché
Procédure en Algérie : décision d'enregistrement. La mise sur le marché d'un médicament en Algérie est conditionnée par une décision d'enregistrement dans |
|
Décret exécutif n° 20-323 du 6 Rabie Ethani 1442 correspondant au
Rab. II 7 1442 AH JOURNAL OFFICIEL DE LA REPUBLIQUE ALGERIENNE N° 69. 6 Rabie Ethani 1442 ... et du contrôle à l'enregistrement des médicaments radio. |
|
JOURNAL OFFICIEL DE LA REPUBLIQUE ALGERIENNE N° 78 12
Jum. I 12 1442 AH d'enregistrement des médicaments à usage de la médecine humaine. ————. Le ministre de l'industrie pharmaceutique |
|
JOURNAL OFFICIEL
Jum. I 12 1442 AH 26 décembre 2020 fixant la procédure de l'évaluation documentaire et/ou technique du dossier d'enregistrementet et la liste des médicaments ... |
|
JOURNAL OFFICIEL
Jum. I 12 1442 AH JOURNAL OFFICIEL DE LA REPUBLIQUE ALGERIENNE N° 78 ... au 26 décembre 2020 fixant la procédure de fixation des prix des médicaments. |
|
????? ???????????????????? ?????????????????????? ????
Raj. 29 1415 AH La procédure d'enregistrement des médicaments à usage humain en Algérie .......... 49. I.2.1 Avant la création de l'Agence Nationale des ... |
|
GUIDE DE LENREGISTREMENT DES MEDICAMENTS
de la procédure d'enregistrement des médicaments destinés à dans les pays suivants : France Allemagne |
|
Recommandation de procédure de traitement des retraits/rappels de
MARS 2016 – RECOMMANDATION DE PROCÉDURE RETRAITS/RAPPELS DE LOTS DE MÉDICAMENTS À USAGE HUMAIN DANS UNE PHARMACIE D'OFFICINE. - 1 -. RECOMMANDATION. |
|
Arrêté du 12 Joumada El Oula 1442 correspondant au 27 décembre
Jum. I 12 1442 AH DE LA REPUBLIQUE ALGERIENNE DEMOCRATIQUE ET POPULAIRE ... d'enregistrement des médicaments à usage de la médecine humaine. |
|
Guide de lenregistrement des médicament Biosimilaires
Shaw. 18 1439 AH 6.2.2.3. Procédure d'enregistrement. 15. 7. PHARMACOVIGILANCE. 17. 8. INTERCHANGEABILITE. 18. 9. PROCEDURE APPLICABLE POUR LES MEDICAMENTS ... |
|
Les procédures denregistrement dun médicament en Europe - Leem
Pour l'enregistrement d'un médicament dans plus d'un état membre de l'Union La procédure de reconnaissance mutuelle (ou MRP pour Mutual Recognition |
|
Stratégies denregistrement des produits de santé - Aurore - Unilim
Les différents types de procédure d'enregistrement des médicaments : l'Europe En France, l'obtention d'une AMM préalablement à la commercialisation d'un |
|
Procédures dAMM - Ministère des Solidarités et de la Santé
Reconnaissance mutuelle (autorisation délivrée par l'AFSSAPS pour la France) : Procédure obligatoire depuis 1998 pour tout médicament ayant déjà une AMM |
|
PROCEDURE NATIONALE DENREGISTREMENT (France)
Généralités sur Procédures d'enregistrement Médicament mis sur le marché européen Nécessité d'une autorisation par les autorités compétentes nationale |
|
DOSSIER TECHNIQUE - Thesesante
L'ANSM est l'équivalent de L'EMA en France, créée en 2011 par la loi du 29 décembre à la prise d'une décision finale sur l'inscription ou pas d'un médicament sur la américains produisirent des procédures d'acceptation de lots par plans |
|
Autorisation de Mise sur le Marché de Médicaments à - ANSM
AMM nationale et en procédure de reconnaissance mutuelle et procédure décentralisée médicaments et des demandes post-AMM/enregistrement ( modifications, Changement relatif à l'exploitant de l'AMM en France : une autorisation de |
|
INTRODUCTION
Raison pour laquelle le code du médicament et de la pharmacie a consacré ses premiers l'absence d'une procédure d'enregistrement spécifiques aux médicaments génériques transparence de l'HAS France (Haute Autorité de Santé) |