base faible
|
§ 7 (suite) Calcul du pH de solutions
pH d’une solution d’une base faible La même stratégie que pour un acide faible est appliquée au cas d’une base faible B : B + H 2O BH+ + OH– Cette fois la solution contient les quatre espèces B BH+ H 3O+ et OH– dont les concentrations sont inconnues Le système de quatre équations à résoudre pour |
|
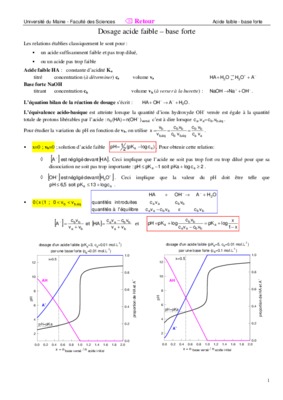
§ 7 (suite) Titrages acide-base
Le titrage d’une base faible par un acide fort est également le symétrique du cas du titrage d’un acide faible par une base forte: La solution initiale est constitué d’une base faible Si celle-ci n’est que faiblement protonée on aura: pH ≈ 7 + 1/ 2 { pK a + log (c a / c0)} avec pK a = pK e – pK b |
|
Chap TS acide-base
Une base faible B1 est plus forte qu'une autre base faible B2 si à concentrations égales l'avancement de sa réaction avec l'eau est plus grand que celui de la réaction de la base B 2 avec l'eau Soit xF1 > x F2 avec xF1 et x F2 |
|
ACIDES FAIBLES — BASES FAIBLES
ACIDES FAIBLES — BASES FAIBLES Exercice 1 : 1 Donner la définition d’un acide d’une base 2 Définir un couple acide/base 3 Donner les formules chimiques des bases conjuguées des acides suivants : a) H -COOH b) C6H5-COOH c) HCN d) HF e) HNO2f) H2PO4 — 4 Donner les formules chimiques des acides conjugués des bases suivantes : a |
Comment classer les bases faibles ?
On classe les bases faibles en fonction de leur constante d'acidité. Les bases faibles ont un pK a inférieur à 14. Pour un pK a négatif, on dit qu'elles sont « indifférentes ». Dans une réaction acido-basique, le schéma général est le suivant : une base d'un couple réagit avec un acide d'un autre couple selon l'équation : .
Quelle est la différence entre une base forte et une base faible ?
Base forte - base faible Toujours selon Brønsted, une base est une espèce chimique susceptible de capter un ou plusieurs protons . Dans la pratique, ces protons peuvent être pris à des molécules d’eau, formant alors des ions hydroxydes . On prendra en compte ici uniquement des monobases.
Quelle est la condition préliminaire pour une base faible ?
Pour une base faible, la condition préliminaire est pc < pKb –1. On vérifiera a posteriori que l’approximation était justifiée en calculant les valeurs de [A–] et [BH+], pour respectivement le cas d’un acide faible ou d’une base faible.
Comment savoir si une base est faible ?
Une base faible est une base qui ne se dissocie pas totalement dans l' eau . Lorsqu'une base faible B − est mise en présence d'eau, il se produit la réaction suivante : La réaction n'est pas totale mais équilibrée, la base reste toujours présente en solution. On classe les bases faibles en fonction de leur constante d'acidité.
|
PH et pKa - Eli Zysman-Colman
pH d'une solution de base forte pH = 14 + log [B] 8 Calcul de pH Formule générale pour le pH de solutions d'acide/base faible: [H3O+] = Ka (([AH] - [H3O+] + |
|
COURS DE CHIMIE GENERALE Semestre 1 SVI - Université Cadi
Cas d'une base forte 2 4 Cas des bases faibles 2 5 Cas d'un mélange d'un acide fort et d'un acide faible |
|
Révisions sur les acides et les bases - Nicole Cortial
donc la base la plus forte, dans l'eau Les couples acide faible / base faible ont tous des constantes d'acidité comprises entre 1 et 14 10 |
|
Déterminer si une base est fort ou faible
Une base est forte si elle se dissocie totalement lors de sa mise en solution On a alors la relation [HO-]=C • Une base est faible si elle se dissocie partiellement |
|
Chapitre 1 Acides et bases
faible ssi la dissociation est une réaction équilibrée ssi pKb > 0 ssi pKa < pKe Dans le cas d'une base forte, totalement dissociée dans l'eau, la concentration |
|
VIEtude sommaire des mélanges
d'hydrolyse des acides et bases faibles augmente avec la dilution) si la base faible possède une constante de basicité et une concentration assez faibles) |
|
Le pH 6 Le dosage des solutions dacides et des bases faibles
A la fin de ce chapitre vous devrez être capable de • Reconnaître/citer les espèces chimiques mis en jeu dans le dosage : acide ou base, fort ou faible |
|
Les acides et bases en solution aqueuse - Groupe Transition
Echelle et table des constantes d'acidité Ka (pKa) 4 5 Coefficient d'ionisation ( de dissociation) d'un acide ou d'une base faible Pourcentage d'ionisation (de |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
LES ACIDES FAIBLES ET LES BASES FAIBLES : CONSTANTE D'ACIDITE ASSOCIEE 9 indifférente : c'est la base faible conjuguée de l'ion ammonium NH4 |
|
Calcul du PH
4- pH d'une solution base forte très diluée 8- pH d'une solution d'une base faible très diluée 15- pH d'une solution de mélange de deux bases faibles |