devoir pile premiere s
|
CONTRÔLE DE PHYSIQUE CHIMIE PREMIÈRE S Sujet 1
CONTRÔLE DE PHYSIQUE CHIMIE PREMIÈRE S Sujet 2 Tous les calculs et affirmations seront justifiés ! Attention aux chiffres significatifs ! Exercice n° 1 (4 points) Pour doser par spectrophotométrie une solution bleue de sulfate de cuivre Cu 2+ +SO 4 2- on a préparé 5 solutions de concentrations différentes La mesure de |
|
Exercices de physique-chimie Première Spécialité
2/ En utilisant un tableur ou une calculatrice calculer la moyenne de la s erie de mesures conserv ees 3/ Calculer l’ ecart type de la s erie de mesure par une m ethode statistique 4/ En d eduire l’incertitude sur la mesure puis donner une estimation du volume molaire d?un gaz Vm dans les conditions |
Qu'est-ce que la pile Daniell ?
La pile Daniell, schématisée ci-dessous, débite un courant électrique qui circule, à l’extérieur de celle-ci, de l’électrode du cuivre (pôle positif de la pile) vers l’électrode de zinc (pôle négatif). Les électrons, responsables du passage du courant, circulant en sens inverse, de l’électrode de zinc vers l’électrode de cuivre.
Comment fonctionne une pile ?
Une pile est constituée de deux demi-piles, contenant chacune une électrode plongeant dans une solution ionique : un électrolyte. Ces demi-piles sont reliées par un pont salin qui permet le transfert d’ions d’une solution à l’autre.
Quels sont les différents types de piles ?
Les piles les plus courantes sont les piles salines ou alcalines constituées d’une électrode en zinc et contenant du dioxyde de manganèse. Seul l’électrolyte diffère : dans une pile alcaline, l’électrolyte est une solution basique (d’hydroxyde de sodium par exemple). Une pile alcaline est plus chère qu’une pile saline, mais plus performante.
Comment calculer la tension courant d'une pile ?
1/ Faire le schema du montage electrique permettant d'e ectuer la mesure de la caracteristique tension-courant d'une pile. 2/ Tracer la caracteristique tension courant U = f(I) de cette pile. 4/ En deduire les valeurs de la tension a vide E de la pile et de sa resistance interne r.
|
Ch16_pile_al_zn_masse_co2_pr
Devoir surveillé Durée : 1h Exercice n°1 : Etude de la pile Aluminium-Zinc 6 En déduire la polarité de la pile Pour chacune des demi-piles |
|
Thème : Piles et électrolyses Fiche 4 - Studyrama
5) Dans une pile l'anode s'enrichit en électrons ici par la réaction L'autre borne est donc l'anode c'est la borne + ; dans le premier cas il y a |
|
Sentraîner : Piles et oxydoréduction Exercice - Lycée Ismael Dauphin
Lorsque la voiture démarre l'accumulateur fonctionne comme une pile Compléter les deux premières lignes du tableau d'avancement ci-dessous |
|
Première générale - Oxydo-réduction - Exercices - Devoirs
Écrire l'équation de la réaction d'oxydoréduction modélisant la transformation chimique entre le diiode I2 et la cystéine notée Cys–S–H 2 4 L'action |
|
DS9pdf
S Exercice I : (7 pts) Un alcool de formule brute C4H100 a quatre 5) Ecrire l'équation de la réaction globale qui intervient quand la pile débite |
|
Les piles dispositifs mettant en jeu des transformations spontanées
s'agit de la borne ? de la pile ? Des électrons sont captés par la solution ionique d'ions cuivre II selon la demi-équation électronique : Cu |
|
DEVOIR SURVEILLE N°7
1 jui 2018 · Correction du devoir surveillé n°7 (1ère S) Exercice 1 : Etude d'une pile 1 La demi-équation de la transformation de l'aluminium en ions |
|
Exercices de révisions : Physique-chimie
Écrire les deux demi-équations d'oxydoréduction des deux couples auxquels le peroxyde d'hydrogène appartient 3 En déduire l'équation de la réaction étudiée ( |
|
DEVOIR COMMUN N°1 PHYSIQUE-?CHIMIE PSI ______ vendredi
2 oct 2015 · L'azote est au degré d'oxydation ?II dans l'hydrazine et ses acides alors qu'il est au degré d'oxydation 0 dans le diazote Il s'agit à chaque |
|
Thème : Piles et électrolyses Fiche 4 - Studyrama
LE TALENT C'EST D'AVOIR ENVIE CHIMIE Série S Nº : 37004 Fiche Corrigés 5) Dans une pile l'anode s'enrichit en électrons ici par la réaction Al(s) = |
|
Sentraîner : Piles et oxydoréduction Exercice - Lycée Ismael Dauphin
Ecrire l'équation bilan d'oxydoréduction qui se produit dans l'accumulateur au plomb Correction Exercice : L'accumulateur au plomb et le démarrage automobile |
|
Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
3) Ecrire l'équation de la réaction chimique globale de fonctionnement de la pile et calculer sa constante d'équilibre 4) Faire un schéma de la pile sur |
|
DS 8 sur les chap
Devoir surveillé Durée : 1h Exercice n°1 : Etude de la pile Aluminium-Zinc (9 pts) On réalise une pile au laboratoire dans deux compartiments séparés |
|
Oxydo-réduction - Exercices - Devoirs - Physique et Maths
3 Écrire l'équation de la réaction d'oxydoréduction modélisant la transformation chimique entre le diiode I2 et la cystéine notée Cys–S–H |
|
Devoir surveillé : mécanique de Newton et piles - Moutamadrisma
Exercice n°2? : Constitution et étude d'une pile : 15pts Données : • Réaction entre le métal cuivre et l'ion argent (I) : Équation : 2 Ag + (aq) + Cu(s) |
|
Piles et accumulateurs - Physique / Chimie – Lycée
La première pile alcaline a été conçue en 1959 par les chimistes Lewis Urry Karl Kordesch et P A Marsal Ces piles ont une durée de vie plus longue que |
|
Exercices de physique-chimie Première Spécialité
2/ Écrire les demi-équations électroniques d'oxydoréduction 3/ En déduire l'équation de la réaction 4/ Identifier le réactif oxydé et le réactif réduit |
|
C) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
Le premier compartiment se compose d'une plaque de cuivre plongée dans La plaque de zinc qui représente le pôle négatif de la pile s'appelle l'anode |
|
Piles et oxydoréduction cours exercices corrigés Première 1S
Piles et oxydoréduction cours exercices corrigés Première Télécharger en linge des Fichiers PDF qui contient des Cours et exercices corrigés + des résumés |
|
Devoir n°1
On réalise une pile formée à partir des couples Zn2+ / Zn et Fe2+ / Fe Chaque solution a pour volume V= 100 mL et la concentration initiale des ions positifs est C |
|
DS 8 sur les chap
Devoir surveillé Durée : 1h Exercice n°1 : Etude de la pile Aluminium-Zinc (9 pts) On réalise une pile au laboratoire dans deux compartiments séparés |
|
Première générale - Oxydo-réduction - Exercices - Physique et Maths
Oxydo-réduction - Exercices Exercice 1 Exercice 2 1/4 Oxydo-réduction - Exercices Physique – Chimie Première S obligatoire - Année scolaire 2019/ 2020 |
|
Piles et électrolyses - Studyrama
(aq) + 2 Al(s) peut rendre compte de la transformation de la pile La constante ( aq)) dans un deuxième tube en U Les électrodes sont en graphite et |
|
Sentraîner : Piles et oxydoréduction Exercice : Laccumulateur au
Lorsque la voiture démarre, l'accumulateur fonctionne comme une pile Compléter les deux premières lignes du tableau d'avancement ci-dessous Equation |
|
DS no8 Piles, accumulateurs & électrolyse Exercice 1 – La pile sous
molaire initiale en ions zinc et en ions cuivre : [Cu2+] = [Zn2+]=1,0 mol L-1 L' électrode positive de cette pile est l'électrode de cuivre 1 1 Légender le schéma de |
|
Exercices de révisions : Physique-chimie
Afin de préparer au mieux votre rentrée, il est fortement conseillé de faire ces exercices la deuxième quinzaine du mois d'août Bon courage Partie A : La |
|
Piles et accumulateurs - Physique / Chimie – Lycée
Lorsque la pile fonctionne, l'électrode de zinc est rongée et des ions La première pile alcaline a été conçue en 1959 par les chimistes Lewis Urry, Karl |
|
DEVOIR SUR LOXYDORÉDUCTION
c) Dans une pile électrolytique contenant une solution de AgNO3(aq), la masse d 'argent qui se dépose au bout de 2h est de 10,78 g Quelle est l'intensité du |
|
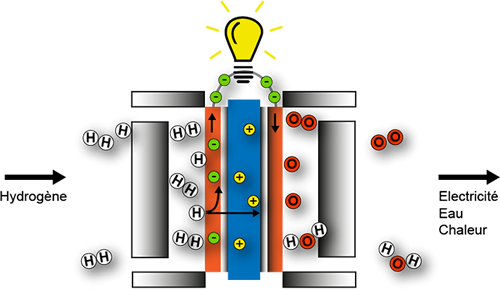
Devoir Surveillé n° 5 – option PSI - Chimie en PCSI
28 avr 2016 · PREMIER EXERCICE ETUDE D'UNE PILE À COMBUSTIBLE Les céramiques : des matériaux traditionnels à l'énergie du futur |