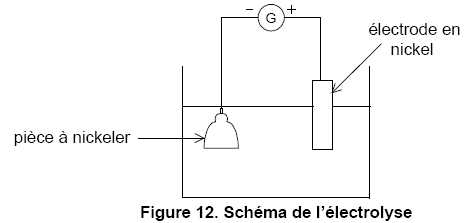
dosage du cuivre par l'edta
|
259 Le cuivre extrait à lEDTA dans les sols de France
quantités de cuivre extraites par l'EDTA sont supérieures à celles des formes échangeables (extraites par des sels neutres) mais restent en bonne corrélation avec le potentiel d'offre du sol Choix d'un seuil pour estimer les probabilités de carence pour les cultures sensibles Dans le passé le test à l’EDTA a permis de prévoir la |
|
Activités expérimentales de chimie des matériaux
de complexation des deux cations par l’EDTA sont proches ce qui ne permet pas de doser sélectivement les ions Cu2+ et Zn2+ L’ajout de thiosulfate de sodium (jouant le rôle d’ion masquant par complexation du cuivre) permet de doser uniquement l’ion Zn2+ Un premier dosage de la solution |
|
Complexométrie et dosages titrimétriques des cations métalliques
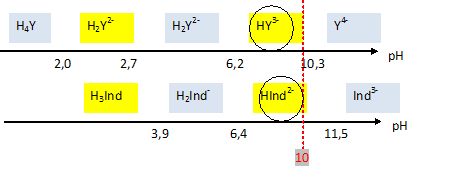
complexation des cations par l'EDTA sont totales On pourra alors utiliser l'EDTA comme réactif de dosage Effet du pH : II apparaît donc que plus le pH du milieu de réaction est alcalin ( c'est à dire que plus l'EDTA est déplacé vers la forme Y4-selon la réaction H 2Y 2-+ 2OH-→ Y4-+ 2H 2O) plus on favorise la formation des complexes |
|
Dosage de Cu2+ par l’EDTA Dosage de Cu2+ par lEDTA
introduit dans une cuve du spectrocolorimètre On mesure l'absorbance à la longueur d'onde choisie puis on remet le contenu de la cuve dans le bécher Simuler la courbe de dosage à l’aide d’un logiciel ad hoc Sous quelle forme se trouve principalement Cu2+? Écrire la RP Calculer sa constante |
|
Dosage du cuivre (II) par iodométrie
PRINCIPE DU DOSAGE 1- + 1/2 Iz + e- JC0 = 050 v Cette réaction apparemment impossible se fait parce que l’iodure de cuivre (1) est insoluble (pK = 12) Dans ce cas le potentiel normal apparent du couple CU (II)/Cu 1 devient égal à 084 V (012 + 006 x 12) |
|
TP n°3
•Faire un premier dosage mL par mL et repérer la valeur approximative V2Eapprox de solution d’EDTA versée correspondant au virage bleu clair de la solution •Effectuer un deuxième titrage plus précis l’équivalence sera repérée à la goutte près Noter V2E le volume de solution d’EDTA versée à l’équivalence C 2 |
Quelle est la concentration de l'EDTA ?
TITRAGE D'UNE SOLUTION D'EDTA Considérons le titrage de 100 mL d 'une solution du sel disodique de l' acide éthylènediaminetétraacétique ou EDTA (Na2H2Y), de concentration 10-2 moLL-I, par une solution de soude l mol.L-1 (concentration suffisamment élevée pour que le dilution soit considérée négligeable).
Quel est le réactif de dosage de l'EDTA ?
Le réactif de dosage est l'EDTA. EDTA signifie EthylèneDiamineTétraAcétique acide. L'EDTA est aussi appelé complexon III, ou chélaton, ou versène ... 4 couples 2 couples La forme totalement protonée de l'EDTA est généralement notée H6Y2+, la forme totalement déprotonée Y4-. H2Y2- ; HY3- ; Y4-.
Comment calculer le précipité d’iodure cuivreux ?
Il est très facile de démontrer que la moindre goutte d’iodure de potassium, permet d’obtenir le précipité d’iodure cuivreux. La réaction est donc : cl.l*+ + 2 1- + CU1 & + 1/2 11. l mole Sr09- correspond donc à 1 mole CU (II). 2. INCONVENIENTS DE LA METHODE. Nous nous attacherons au virage du jaune à l’incolore de l’iode.
Quel est le précipité rouge d'oxyde de cuivre ?
Ire part : Ajouter NaOH 10 N, on observe un beau pré- cipité rouge d’oxyde de cuivre 1, Cu,O soluble ‘dans le thiosulfate ou l’ammoniaque (bleuissement à l’air). 2= part : Ajouter de l’ammoniaque, il n’y a aucun pré- cipité mais le bleuissement caractéristique des complexes amino cuivre (1) s’oxydant en amino cuivre (II) au contact de l’air.
|
Dosage de Cu2+ par lEDTA
Dosage de Cu2+ par l'EDTA. 1) Généralités a) Grandeurs spectrocolorimétriques. Soit un faisceau parallèle Déterminer le titre en cuivre de la solution fournie ... |
|
Activités expérimentales de chimie des matériaux
Après ajout du thiosulfate de sodium un nouveau dosage effectué par l'EDTA permet (partie sur le dosage du cuivre et du zinc dans le laiton). * Institut ... |
|
1 Epreuve de Travaux Pratiques Agro-Paris Tech 2017 Sujet MG n
On obtient ainsi la solution S destinée aux dosages ultérieurs. 5. Dosage complexométrique du cuivre. Il est possible de doser les ions cuivre (II) par l'EDTA |
|
Dosage des ions cuivre et détermination de la formule de la
Travail préparatoire : L'EDTA est un ligand hexandente dont la formule peut être résumée sous la forme Y4-. En fonction du pH sa forme en solution. |
|
Deux aspects de la chimie du cuivre
2.4.1. Lors du dosage des ions Cu2+ par l'EDTA pourquoi faut-il éviter de se placer en milieu trop acide ou trop basique ? |
|
Untitled
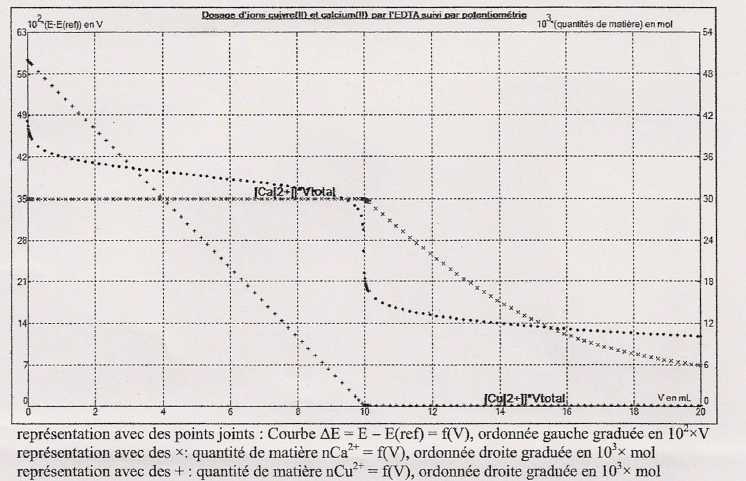
13/03/1992 mise au point méthodologique dosage du cuivre à l'électrode spécifique lors de la titration à l'EDTA. A-) DOSAGE DU CALCIUM |
|
* Sommaire. - Lé but de ce travail est lapplication des titrages
à pH = 10 et à pH = 8 pour le dosage du cuivre(II) par l'acide éthylène diaminetétracétique (E.D.T.A.) |
|
LEXTRACTION LIQUIDE-LIQUIDE UN PROCEDE PROMOTEUR
EXTRACTION DU CUIVRE. Afin d'effectuer le dosage de cuivre (II) par l'EDTA il faut |
|
LES REACTIONS DE COMPLEXATION 1. Les complexes 1.1
Exemple : Titrage des ions magnésium par l'EDTA. Pour cela on utilise un volume v0 = 10 mL d'une solution contenant l'ion Mg2+ de concentration C0. On |
|
COMMENT SE COMPORTE LE CUIVRE DANS LES SOLS
un sol est le dosage du cuivre à l'EDTA. Or ces analyses de sols par extraction EDTA rendent compte du cuivre total et pas seulement de la biodisponibilité |
|
Dosage de Cu2+ par lEDTA
Dosage de Cu2+ par l'EDTA Simuler la courbe de dosage à l'aide d'un logiciel ad hoc. ... Déterminer le titre en cuivre de la solution fournie. |
|
Dosage des ions cuivre et détermination de la formule de la
Dosage des ions cuivre(II) dans la solution de sulfate de cuivre. Travail préparatoire : L'EDTA est un ligand hexandente dont la formule peut être résumée |
|
1 Epreuve de Travaux Pratiques Agro-Paris Tech 2017 Sujet MG n
Synthèse et analyse d'un complexe du cuivre (II) cuivre (II) et un dosage de l'éthylènediamine. ... Solution titrée d'EDTA à 0010 mol.L-1. |
|
* Sommaire. - Lé but de ce travail est lapplication des titrages
à pH = 10 et à pH = 8 pour le dosage du cuivre(II) par l'acide éthylène diaminetétracétique (E.D.T.A.) |
|
Deux aspects de la chimie du cuivre
2.4.1. Lors du dosage des ions Cu2+ par l'EDTA pourquoi faut-il éviter de se placer en milieu trop acide ou trop basique ? |
|
Complexométrie et dosages titrimétriques des cations métalliques
On pourra alors utiliser l'EDTA comme réactif de dosage. Effet du pH : II apparaît donc que plus le pH du milieu de réaction est alcalin ( c'est à dire que plus |
|
Travaux Pratiques de Chimie PC Oral
17 mai 2015 Solution aqueuse de ligand EDTA (2Na+ H2 2?. ) à environ 1×10?2 mol?L-1. • Solution aqueuse de sulfate de cuivre (Cu2+ |
|
Spectrophotométrie visible – Complexe Ni-EDTA dosage du cuivre
Nickel du complexe (Ni-EDTA) et du cuivre. Puis |
|
Untitled
17 févr. 1992 cuivre à point méthodologique dosage du l'électrode spécifique lors de la titration à l'EDTA. A-) DOSAGE DU CALCIUM |
|
Expériences illustrant les réactions de complexation; applications.
Les ions cuivre forment dans l'eau un complexe hexa-aquacuivre II noté [Cu(H2O)6]2+ . Expérience 7 ) Dosage des ions Calcium et magnésium par l'EDTA. |
|
Dosage de Cu2+ par lEDTA - Unisciel
Dosage de Cu2+ par l'EDTA Simuler la courbe de dosage à l'aide d'un logiciel ad hoc Déterminer le titre en cuivre de la solution fournie |
|
Dosage des ions cuivre et détermination de la formule de la
Dosage des ions cuivre(II) dans la solution de sulfate de cuivre Travail préparatoire : L'EDTA est un ligand hexandente dont la formule peut être résumée |
|
H - Concours Agro Veto
Il est possible de doser les ions cuivre (II) par l'EDTA en présence d'un indicateur coloré comme le murexide Question 1 : On considère une solution à doser |
|
PC*10/11 TP11 Dosage dun mélange des sels Il sagit de doser les
Il s'agit de doser les ions fer(III) et Cu(II) dans une solution (S) contenant du sulfate de cuivre et du sulfate de fer On étalonne d'abord une solution d' |
|
Complexométrie et dosages titrimétriques des cations métalliques
Les pK sont respectivement de 00 ; 15 ; 20 ; 266 ; 616 ; 1024 Les complexes formés par l'EDTA et un cation métallique Mn+ ont pour formule MYn-4 L'EDTA |
|
Lé but de ce travail est lapplication des titrages spectropho
à pH = 10 et à pH = 8 pour le dosage du cuivre(II) par l'acide éthylène diaminetétracétique (E D T A ) en présence de la murexide |
|
TP Dosage Complexometrie1 PDF Laiton Chimie - Scribd
Le laiton est un alliage de cuivre et de zinc (plus éventuellement Doser l'ensemble par l'EDTA en agitant doucement à la main td_tc5_redox pdf |
|
2 Recherche et dosage du calcium du magnésium du cu - CORE
dosage du fer total par complexomètrie par l'E D T A en pré- d'autres anions et cations: calcium magnésium cuivre titane manganèse |
|
Dosage des éléments cobalt nickel cuivre et zinc et leur distribution
La méthode utilisée pour le dosage du cuivre est celle à la dithizone La dithizone forme avec le cuivre en milieu acide minéral dilué (pH 3 |
|
Les dosages complexométriques - Horizon IRD
dosages volumétriques aiJJples et rapides d'un très grand nonbre d'ions oétalliques Ainsi l'aoide éthylène diamine tétraoétique (E D T A ) donne'en |
| Dosage de Cu2+ par l’EDTA Dosage de Cu2+ par l'EDTA - Unisciel |
| Dosage des ions cuivre et détermination de la formule de la |
| 259 Le cuivre extrait à l'EDTA dans les sols de France |
| TP n°3 - Titrage d’ions par réaction de complexation |
| Sujet MG n°01 (1) 1 Présentation |
| TP Dosage du calcium - ac-nancy-metzfr |
| Searches related to dosage du cuivre par l+edta filetype:pdf |
|
Dosage de Cu2+ par lEDTA - Unisciel
Dosage de Cu2+ par l'EDTA Prélever dans un bécher 20 mL de cette solution et doser par de l'EDTA Déterminer le titre en cuivre de la solution fournie |
|
Synthèse et analyse dun complexe du cuivre (II) - Concours Agro Veto
Pour ce faire, on mettra en place deux dosages : un dosage des ions Il est possible de doser les ions cuivre (II) par l'EDTA en présence d'un indicateur coloré |
|
Dosage des ions cuivre et détermination de la formule de la
Dosage des ions cuivre(II) dans la solution de sulfate de cuivre Travail préparatoire : L'EDTA est un ligand hexandente dont la formule peut être résumée sous |
|
TP 5 : Complexes
5 oct 2007 · Une fois cela compris, il est alors possible de doser la concentration Nitrate de cuivre (II) Titrages du calcium et du magnésium par EDTA |
|
Travaux Pratiques de Chimie\ PC\ Oral - concours Centrale-Supélec
17 mai 2015 · Solution aqueuse de ligand EDTA (2Na+, H2 2− ) à environ 1×10−2 mol⋅ L-1 • Solution aqueuse de sulfate de cuivre (Cu2+, SO2− 4 ) |
|
Complexométrie et dosages titrimétriques des cations métalliques
L'EDTA complexe la plupart des cations : Ca2+, Fe2+, Cu2+, Mg2+, Ni2+, Zn2+, AI3+ La stoechiométrie de réaction est de 1 pour 1 Plus le pH est élevé, plus la |
|
Magister SLIMANI ABDELKADER Devant le jury composé - CORE
cuivre avec l'acide citrique, et la méthode volumétrique ou celle du dosage complexométrique pour la complexation du cuivre avec l'EDTA • Enfin, notre étude |
|
Les dosages complexométriques - CORE
Ainsi l'aoide éthylène diamine tétraoétique (E D T A ) donne'en doser Je oaloium, le cuivre et le zino dans des sols acides, mais elle Il;S convient pas |
|
ANALYSE DUN LAITON
cuivre On cherche dans cette manipulation à déterminer la teneur en cuivre puis en iodométrie et spectrophotométrie dosage des ions Zn 2+ par l'EDTA |


































![GUIDE] Les éléments minéraux secondaires et oligo-éléments GUIDE] Les éléments minéraux secondaires et oligo-éléments](https://i1.rgstatic.net/publication/258962874_Selective_and_precise_photometric_titration_of_metal_ions_with_EDTA_using_masking_agents_Part_III_Determination_of_calcium_lead_and_zinc_in_mixtures_using_simple_inorganic_ions_as_masks/links/5c876c9b92851c831973deab/largepreview.png)