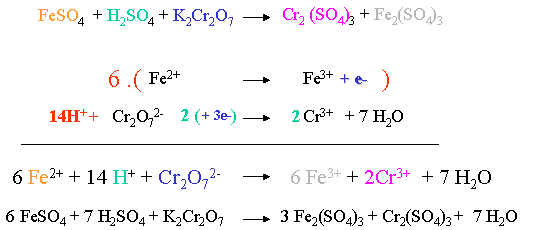oxydoréduction equation
|
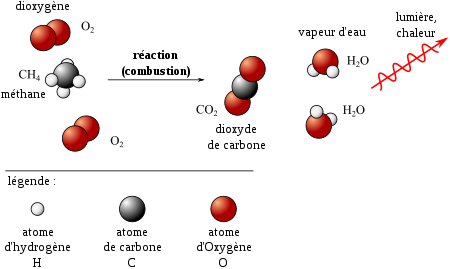
Les réactions doxydo-réduction
Pour avoir autant d'électrons libérés par le réducteur 1 que d'électrons captés par l'oxydant 2 on doit coefficienter chaque demi-équation (en vert) On fait |
Quelle est l'équation de l'oxydation ?
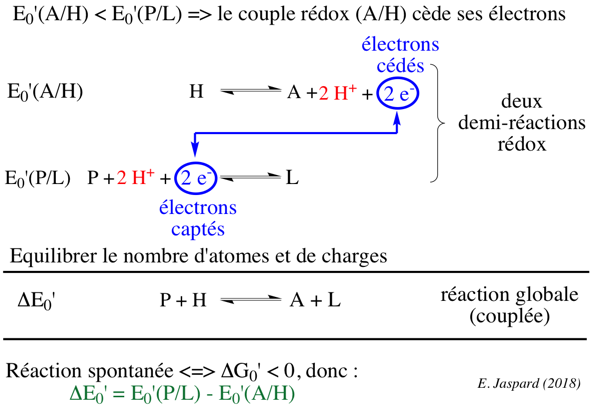
Oxydation : A → A + + e − ; la substance perd un électron .
Réduction : B + e − → B − ; l'électron est accepté par la substance .
Réaction d'oxydoréduction : A + B → A + + B − ; la substance donne un électron à la substance .
La substance est le donneur d'électrons et la substance est l'accepteur d'électrons.Quelles sont les réactions d'oxydoréduction ?
Une réaction d'oxydoréduction est une réaction au cours de laquelle il y a échange d'électrons entre l'oxydant d'un couple et le réducteur d'un autre couple.
Comme toutes les transformations chimiques, les réactions d'oxydoréduction doivent respecter la conservation de la charge électrique.- Une réaction d'oxydoréduction ou réaction rédox est une réaction chimique au cours de laquelle se produit un transfert d'électrons.
Elle consiste en une réaction oxydante couplée à une réaction réductrice.
L'espèce chimique qui capte les électrons est l'oxydant et celle qui les cède, le réducteur.
|
MÉTHODE POUR ÉCRIRE UNE ÉQUATION DOXYDO-RÉDUCTION
UNE ÉQUATION D'OXYDO-RÉDUCTION. Dans le cas ou l'oxydant 1 réagit avec le réducteur 2 : On écrit les demi-équations d'oxydoréduction dans le sens de la |
|
Réactions doxydoréduction
Les réactions d'oxydoréduction sont des réactions chimiques au cours desquelles il y a Tout comme on équilibre l'équation bilan d'une réaction chimique ... |
|
Les réactions doxydo-réduction
Les réactions d'oxydo-réduction. I/ L'oxydoréduction. 1/ Les notions d'oxydant et de réducteur. ? un réducteur est une espèce chimique capable de libérer 1 |
|
Chapitre 3 :Oxydoréduction
I Réactions d'oxydoréduction. A) En solution aqueuse. 1) Définition. • Oxydation : réaction au cours de laquelle une espèce perd un ou plusieurs électrons. |
|
Première Spécialité Activité Expérimentale : Les réactions d
métal aluminium s'oxyde alors que les ions argent sont réduits. Page 4. Document 2 : Méthode pour écrire une demi-équation d'oxydoréduction. Description de |
|
Module 3.1 : Réactions doxydoréduction
Écrivez l'équation de cette réaction identifiez l'oxydant et le réducteur. 0 0 +2 -2. Mg + O2 ? MgO. 1. ( Mg0 -2é ? Mg2+ oxydation |
|
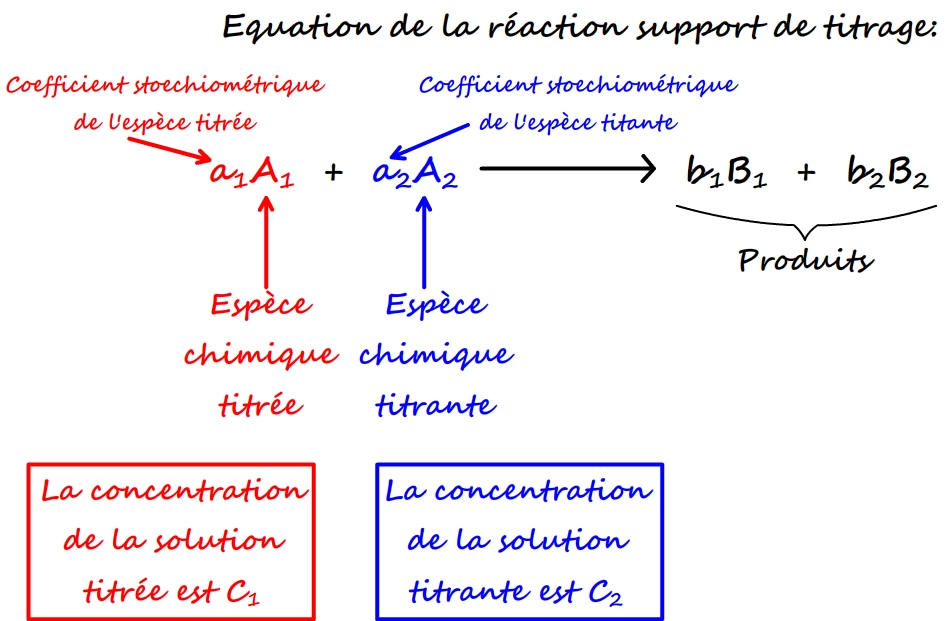
LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
L'ion permanganate est un bon oxydant. Il réagit spon- tanément avec de nombreuses espèces chimiques appelées réducteurs |
|
Oxydoréduction
?5 Étant donné un couple oxydant/réducteur écrire la demi-équation correspondante. ?6 Écrire et localiser les réactions ayant lieu dans une pile. ?7 |
|
? Zn2+
Une OXYDOREDUCTION est une réaction de transfert d'électrons entre deux couples Dans une équation d'oxydoréduction l'oxydant d'un couple réagit avec le ... |
|
On obtient un couple oxydant / réducteur: H+ / H2
4. Des demi-équations rédox à l'équation d'oxydoréduction. Expérience : Fe3+ / Fe2+. : Fe3+ + e = Fe2+. |
|
Chapitre 3 :Oxydoréduction - Melusine
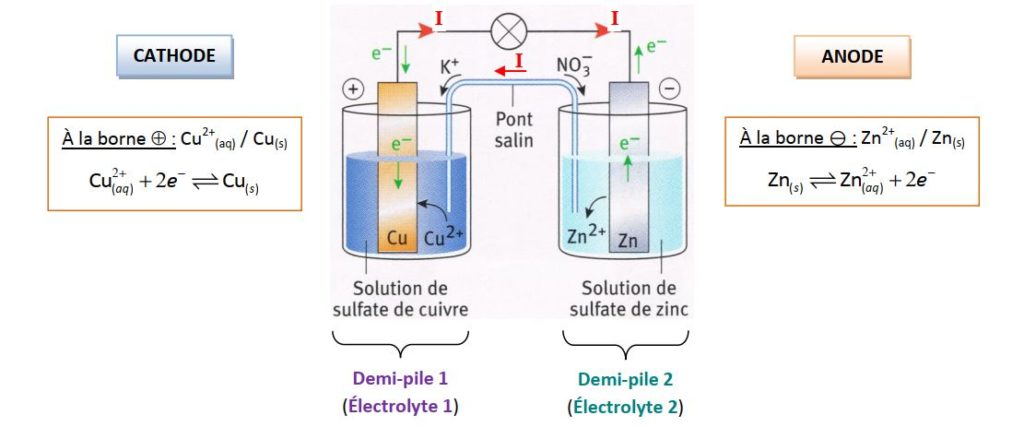
Red1 ² pile Ox2/Red2 : borne œ ? anode ? oxydation Red2 Ox2 + n2e- Equation bilan : Ox1 + Red2 |
|
Les réactions doxydo-réduction - Physique - Chimie
Pour avoir autant d'électrons libérés par le réducteur 1 que d'électrons captés par l'oxydant 2 on doit coefficienter chaque demi-équation (en vert) On fait |
|
Chapitre 4 Oxydo-réduction
À tout oxydant est associé un réducteur reliés par la demi-équation électronique : Ox + n e– ? Red n correspond au nombre d'électrons échangés L'oxydant et |
|
Oxydoréduction - Étienne Thibierge
Exercice 1 : Équations bilan d'oxydoréduction [?00] On s'intéresse aux couples MnO– 4/Mn2+ HClO(aq)/Cl2(g) et Cl2(g)/Cl– On rappelle que MnO– |
|
V- EXERCICES : - Lycée Ismael Dauphin
A partir de ces deux demi-équations d'oxydoréduction donner une équation chimique ayant pour seuls réactifs Cl2(g) et H2O Corrigé Exercice 1 : Ecrire les |
|
Série dexercices : réactions doxydo-réduction pr - AlloSchool
1) Ecrire les formules des couples mis en jeux 2) Ecrire les demi équations correspondantes 3) Etablir l'équation de la réaction d'oxydoréduction 4) Calculer |
|
Chimie - Chapitre 9 : Réactions doxydoréduction Ce quil faut retenir
½ équation redox : Cu = Cu2+ + 2 e- Espèce amphotère : Une espèce pouvant agir en tant qu'oxydant ou en tant que réducteur est dite amphotère |
|
Oxydoréduction – corrigé des exercices Table des matières
Oxydoréduction 2 Comment équilibrer les équations des réactions rédox Equilibrez les équations suivantes à l'aide des nombres d'oxydation et indiquez : |
|
Chapitre 1 - Définitions et équations redox
Chapitre 1 Définitions et équations redox Le concept actuel d'oxydoréduction fait appel à la notion de transfert d'électrons entre |
|
Les réactions doxydoréduction - DSFM
Une demiéquation équilibrée montre les e transférés Il y a une demiéquation d'oxydation et une de réduction Les 2 ensembles forment l'équation rédox Éq |
Quelle est l'équation d'oxydoréduction ?
La réaction d'oxydoréduction est l'addition d'une oxydation et d'une réduction (de manière à simplifier les électrons). L'équation d'une oxydoréduction s'écrit de la manière suivante : Ox1 + Réd2 = Ox2 + Réd1, avec Ox1 / Réd1 et Ox2 / Réd2 des couples oxydant-réducteur.Comment résoudre une équation d'oxydoréduction ?
L'équation d'oxydoréduction s'obtient finalement en combinant les deux demi-équations et consiste en un transfert d'un ou plusieurs électrons du réducteur de l'un des couples à l'oxydant de l'autre couple. Les électrons n'apparaissent donc pas dans le bilan. écrire les demi-équations des deux couples impliqués.Quelle est la formule de l'oxydation ?
Oxydation : A ? A + + e ? ; la substance perd un électron . Réduction : B + e ? ? B ? ; l'électron est accepté par la substance .- Pour écrire une équation d'oxydo-réduction il faut donc commencer par écrire les deux demi équations puis de les combiner pour former l'équation complète en vérifiant que le nombre d'électrons perdus lors de l'oxydation corresponde au nombre d'électrons gagnés lors de la réduction.
Comment écrire l'équation d'une réaction d'oxydoréduction ?
. Les électrons n'apparaissent donc pas dans le bilan. écrire les demi-équations des deux couples impliqués.
Comment déterminer l'oxydant et le réducteur dans une équation ?
. Si dans la demi-équation électronique, l'esp? chimique c? des électrons, c'est un réducteur.
Comment Ecrire une demie équation ?
|
MÉTHODE POUR ÉCRIRE UNE ÉQUATION DOXYDO-RÉDUCTION
UNE ÉQUATION D'OXYDO-RÉDUCTION Dans le cas ou l'oxydant 1 réagit avec le réducteur 2 : On écrit les demi-équations d'oxydoréduction dans le sens de |
|
Solutions aqueuses 2 : réactions doxydo-réduction - UNF3S
Ils forment un couple d'oxydo-réduction Ox/Red dit couple redox Réactions d' oxydoréduction Combiner 2 demi-équations en éliminant les électrons |
|
On obtient un couple oxydant / réducteur: H+ / H2 - Free
4 Des demi-équations rédox à l'équation d'oxydoréduction Expérience : Fe3+ / Fe2+ : Fe3+ + e = Fe2+ |
|
Les réactions doxydoréduction - pontonniers-physique
L'oxydant et le réducteur forment un couple rédox dont la représentation est Ox / Red On associe à ce couple la demi-équation : dRe en Ox = |
|
LES RÉACTIONS DOXYDORÉDUCTION DANS LES TITRAGES
L'ion permanganate est un bon oxydant Il réagit spon- tanément avec de nombreuses espèces chimiques, appelées réducteurs, dans des réactions d' oxydo- |
|
Ecrire une équation doxydoréduction : Méthode : 1) Toujours
Ecrire une équation d'oxydoréduction : Méthode : 1) Toujours commencer par écrire les demi-équations de chacun des couples en mettant à gauche du signe |
|
Oxydoreduction - Lycée Ismael Dauphin
Ecrire l'équation bilan de la réaction chimique traduisant le dépôt métallique Exercice 4 : Ecrire les demi-équations d'oxydoréduction relatives aux couples |
|
Réactions doxydoréduction - Lycée dAdultes
Ox + ne– = Red où n représente le nombre d'électrons échangés 2 2 Equilibrer une demi équation électronique Tout comme on équilibre l'équation bilan d'une |
|
Chapitre 6 : Les réactions doxydoréduction - Physagreg
(aq) 2 Zn Cu aq s Zn Cu + + + → + Les atomes de zinc ont cédé deux électrons, les ions cuivre II en ont accepté deux Équation d'oxydoréduction ou rédox |

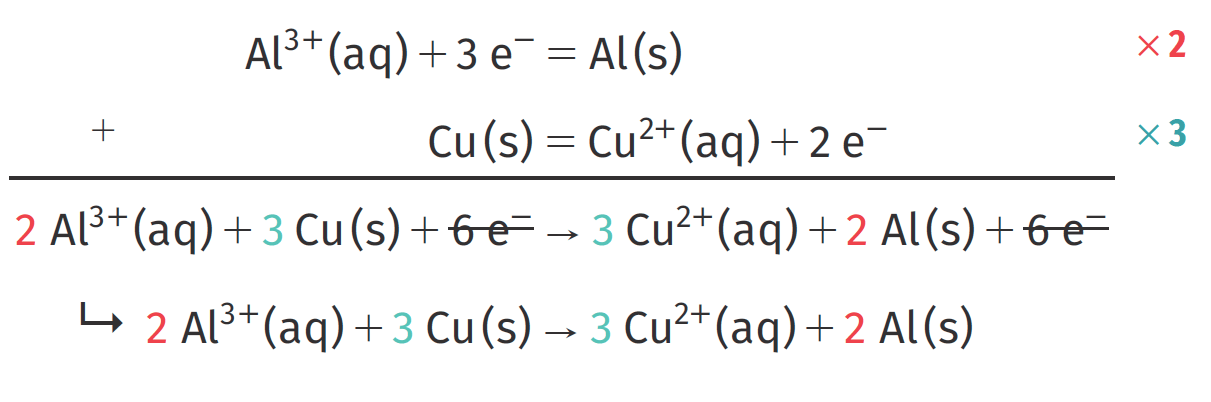







![Chimie: équilibrer une équation d'oxydo-réduction - [PDF Document] Chimie: équilibrer une équation d'oxydo-réduction - [PDF Document]](https://0.academia-photos.com/attachment_thumbnails/40232136/mini_magick20190221-19749-mluji9.png?1550788500)