Exercices de révision- Oxydo-réduction et Piles électrochimiques
|
Première générale
Couples oxydant-réducteur mis en jeu: - BM+(aq) / BMH(aq) - RCOOH(aq) / RCHO(aq) - le glucose est noté RCHO(aq) - la forme oxydée du bleu de méthylène noté |
|
Exercices de révisions Afin de préparer au mieux votre rentrée il est
Donner la composition du système chimique à la fin de la transformation et la masse des produits formés Exercice n°3 : Réactions d'oxydoréduction L'eau |
|
V
Exercice 2 :Ecrire les couples oxydant / réducteur relatifs aux demi-équations d'oxydoréduction suivantes: H2(g) θ 2H+ (aq) + 2e- Au(s) θ Au3+ (aq) + 3e |
|
Série dexercices : réactions doxydo-réduction pr
Série d'exercices : réactions d'oxydo-réduction pr SBIRO Abdelkrim 1)Exercice n o 1 : On ajoute une masse m=28g de la limaille de fer Fe à un volume V=25mL |
1: Écrire l'oxydant et le réducteur de part et d'autre d'une double-flèche. 2: Équilibrer les atomes autres que l'oxygène et l'hydrogène . 3: Équilibrer les atomes d'oxygène en ajoutant autant de molécules de H2O dans l'autre côté. 4: Équilibrer les atomes d'hydrogène en ajoutant autant des ions H+ de l'autre côté.
Comment savoir quel réactif subit une oxydation ?
Ainsi, le réactif qui gagne des électrons est nommé oxydant puisqu'il cause l'oxydation d'une autre substance. À l'inverse, le réactif qui perd des électrons est nommé réducteur puisqu'il cause la réduction de l'autre substance.
Comment savoir qui est l'oxydant et le réducteur ?
On écrit toujours l'oxydant en premier, séparé du réducteur par une barre.
Le couple d'oxydoréduction de l'élément cuivre s'écrit Cu2+ / Cu.
L'oxydant est l'ion Cu2+ et le réducteur qui lui est associé est le métal cuivre Cu.
Couple Fe3+ / Fe2+ : l'oxydant est l'ion Fe3+ et le réducteur est l'ion Fe2+.
Comment savoir si c'est un oxydant ou un réducteur ?
Pour savoir qui est l'oxydant et le réducteur , en utilise cette définition : La substance qui perd des électrons est oxydée et est le réducteur.
La substance qui gagne des électrons est réduite et est l'oxydant .
|
Exercices de révision- Oxydo-réduction et Piles électrochimiques
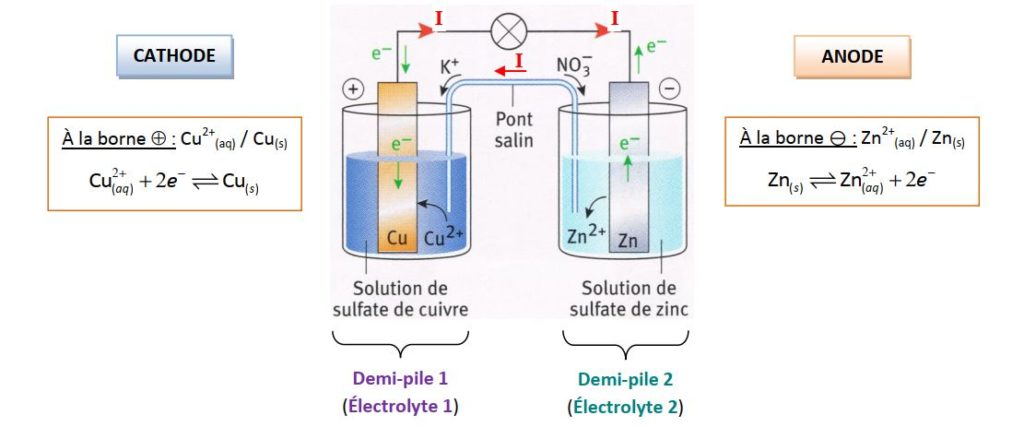
Réactions d'oxydo-réduction et piles électrochimiques. (Exercices de révision). Exercice I. On considère la pile symbolisée par:. |
|
Révision Oxydoréduction Objectifs Exercices
Savoir équilibrer les réactions d'oxydoréduction à l'aide des nombres d'oxydation. les principales différences par rapport à une pile électrochimique. |
|
LES REACTIONS DOXYDOREDUCTION Exercice 1 (Daprès BTS
CORRECTION EXERCICES DE REVISION : LES REACTIONS D'OXYDOREDUCTION. Exercice 1 (D'après BTS ABM 2001 Etude d'une pile). 1. Schéma de la pile :. |
|
Électrochimie
Thèmes abordés dans ce bloc de révisions : oxydoréduction et diagrammes potentiel-pH. II - Rappels de cours. II.1 - Comparaison des courbes i-E pour une pile et |
|
Oxydoréduction – corrigé des exercices Table des matières
Une oxydation est une perte d'électrons. Un oxydant est un accepteur d'électrons. Un oxydant se réduit alors qu'un réducteur s'oxyde. Une réaction |
|
Exercice 1 (6 points) La fabrication du verre Exercice 2 (7 points
On construit une pile électrochimique G2 formée par les deux demi-piles : • une lame de magnésium (Mg) plongeant dans une solution contenant les ions magnésium |
|
Examen final de Chimie 3 Durée: 02 heures
Exercice 01 :Oxydo-réduction et Solubilité (12pts). On réalise une pile électrochimique afin de déterminer le produit de solubilité du sulfate. |
|
Chimie 12e année - Programme détudes : document de mise en
types de piles. Le DVD est aussi disponible à la DREF]. [R] Chimie en solution aqueuse – l'oxydoréduction – piles électrochimiques. |
|
Chapitre 3 :Oxydoréduction
II Piles électrochimiques œ potentiel redox. A) Pile électrochimique. On considère une réaction d'oxydoréduction qui se produit dans une cellule. |
|
Exercices de la séquence n°4 - Piles
Une réaction d'oxydoréduction a lieu lorsque la pile débite du courant. en nombre suffisant pour assurer la production électrochimique d'électricité. |
|
Électrochimie - Numilog
11 1 Les piles ou générateurs électrochimiques primaires 206 16 3 Synthèse de composés non métalliques 313 Exercices 327 Solutions A 1 Potentiels standard de couples d'oxydo réduction Un ouvrage qui donne enfin une vision |
|
Je découvre un extrait du livre - Dunod
Les piles ou générateurs électrochimiques primaires 213 Potentiels standard de couples d'oxydo réduction lecteur par une vingtaine de nouveaux exercices tiques spécifiques et ses visions cinétiques propres et particulières à chaque |
|
Lélectrochimie
électrochimique de réactions de réduction où les espèces sont disposées par ordre C12-6-03 Retracer dans les grandes lignes l'évolution historique des piles réactions totales équilibrées pour les cas où des réactions d'oxydo- réduction |
|
Première D - Direction de la Pédagogie et de la Formation Continue
Côte d'Ivoire un pays émergent à l'horizon 2020, selon la vision du Chef de l'Etat, SEM le fonctionnement de quelques piles électrochimiques : d'exercices interpréter quelques réactions d'oxydo-réduction, à classer quelques couples |
|
Conceptions délèves et détudiants français et tunisiens sur la
les piles électrochimiques repérées chez des élèves et des étudiants français ou tunisiens Mots clés : conceptions, pile, conduction, courant électrique Abstract compris par les apprenants, malgré leur réussite à des exercices d' évaluation plusieurs conceptions greffées sur cette vision du courant électronique |