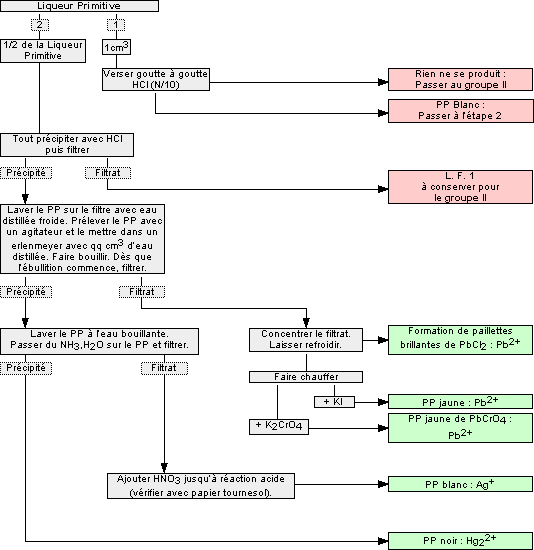
précipitation du chlorure de plomb
|
Équilibres de solubilité
À titre d'exemple le chlorure de plomb PbCl2(s) est en équilibre avec les ions plomb Pb2+ et les ions chlorure Cl– (présents en solution aqueuse) selon : |
|
La précipitation sélective
1) Donner la concentration en ions plomb dans la solution S1 et la concentration en ions chlorure dans la solution S2 Page 2 Partie 1/ Chimie minérale |
|
PRÉCIPITATION DE CHLORURE DE PLOMB
PRÉCIPITATION DE CHLORURE DE PLOMB ? On commence par écrire l'équation de réaction associée à la constante d'équilibre de l'énoncé Il s'agit de la |
|
Précipitation et dissolution
6 mar 2018 · On prélève un même volume V0 = 10 mL de chaque solution que l'on mélange l'une à l'autre Donnée : produit de solubilité du chlorure de plomb Ks |
|
Précipitation et solubilité
Calculer la solubilité dans l'eau pure en g L−1 du chlorure de plomb PbCl2 connaissant pKs = 4 8 3 Calculer la masse d'orthophospate de calcium de |
Quelle est la condition de précipitation ?
CONDITION DE PRECIPITATION :
Soit l'équilibre CxAy = x Cq+ + y Ap-.
On suppose qu'on mélange 2 solutions contenant chacune un ion du précipité.
Les concentrations dans le mélange sont notées [Cq+]0 et [Ap-]0.Comment savoir si il y a précipitation ?
Réaliser le test à la soude
On y introduit une ou deux gouttes de soude.
On observe si il y a la formation d'un précipité.
Si c'est le cas, on observe sa couleur.
Si le précipité est vert, il y a présence d'ions fer(II).Quel est le principe de la réaction de précipitation du chlorure d'argent ?
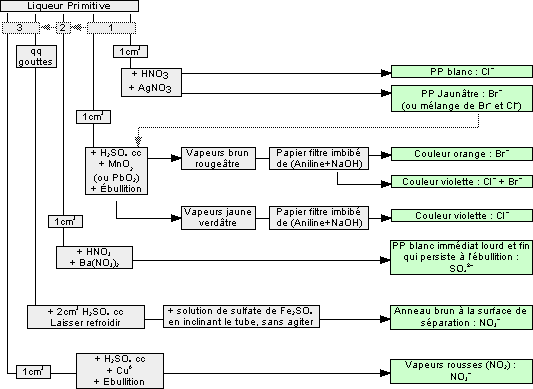
Si on ajoute à une solution de chlorures (ions Cl-) des ions argentiques (ions Ag+) venant d'une solution de nitrate d'argent (AgNO3) en quantité connue et en excès, on obtient un précipité colloïdal blanc de chlorure d'argent AgCl (d'où le nom de dosage argentimétrique des ions Cl-).
- Une réaction de précipitation :
Les ions sont capables de se recombiner et de former un nouveau composé, PbI2.
PbI2 est insoluble dans l'eau H2O.
KNO3 est soluble dans l'eau.
La réaction intervient dans l'eau, de sorte que K+ et le NO3- sont dissous dans l'eau et ne sont pas liés l'un à l'autre.
|
CHIM105B – DS2 - Corrigé
1) (/4) Précipitation du plomb II en milieu chlorure. On mélange 10 mL d'une solution de nitrate de plomb II Pb(NO3)2 |
|
Précipitation et dissolution Précipitation et dissolution
6 mars 2018 On prélève un même volume V0 = 10 mL de chaque solution que l'on mélange l'une à l'autre. Donnée : produit de solubilité du chlorure de plomb Ks ... |
|
16 - Le zincII en sol aq
s'interprète par la réaction de précipitation : Zn ˜ + HO = Zn(OH) . Cette précipitation consomme les ions Znø˜ leur concentration baisse donc |
|
La précipitation sélective
précipitation ? Exercice 2 : précipitation du chlorure de plomb. On dispose de V1 = 10 mL d'une solution S1 de nitrate de plomb de concentration C1 = 1 |
|
16 - Précipitation PbCl2
PRÉCIPITATION DE CHLORURE DE PLOMB ? On commence par écrire l'équation de réaction associée à la constante d'équilibre de l'énoncé. |
|
Equilibres chimiques en solution – DS2 – Corrigé Le plomb II
1) (/5) Précipitation du plomb II en milieu chlorure. On mélange 10 mL d'une solution de nitrate de plomb II Pb(NO3)2 |
|
Correction TD - Réactions de dissolution ou de précipitation
Exercice 1 - Précipitation du chlorure de plomb ? Équation de la réaction de dissolution du chlorure de plomb : PbCl2(s) = Pb2+. |
|
Exercices sur le chapitre « Précipitation - Produit de solubilité »
Exercices sur le chapitre « Précipitation - Produit de solubilité ». Exercice n° 1 : On considère un litre de solution saturée en chlorure de plomb. |
|
TP n° EQUILIBRES PRÉCIPITATION - DISSOLUTION
Donnée : Couleurs des principaux précipité obtenus au cours du TP : chlorure de sodium : blanc chlorure de plomb II : blanc iodure de plomb II : jaune. |
|
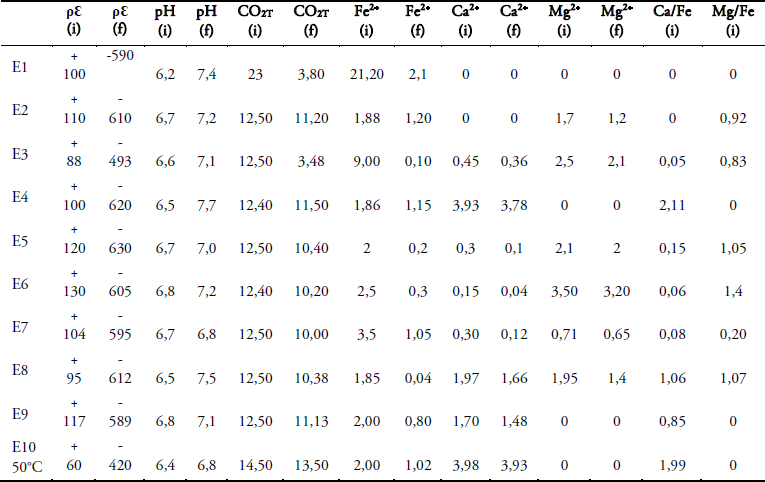
Action des acides sur le plomb et le cuivre
Photo 1 : précipitation du chlorure de plomb dans une solution refroidie d'acide chlorhydrique ayant réagi avec du plomb à chaud. |
|
PRÉCIPITATION DE CHLORURE DE PLOMB - Chimie - PCSI
PRÉCIPITATION DE CHLORURE DE PLOMB ? On commence par écrire l'équation de réaction associée à la constante d'équilibre de l'énoncé |
|
Précipitation et dissolution - Étienne Thibierge
6 mar 2018 · On prélève un même volume V0 = 10 mL de chaque solution que l'on mélange l'une à l'autre Donnée : produit de solubilité du chlorure de plomb Ks |
|
CHIM105B – DS2 - Corrigé
Le plomb II équilibres de précipitation de complexation et d'oxydo-réduction 1) (/4) Précipitation du plomb II en milieu chlorure |
|
Précipitation et solubilité - cpge paradise
Calculer la solubilité dans l'eau pure en g L?1 du chlorure de plomb PbCl2 connaissant pKs = 4 8 3 Calculer la masse d'orthophospate de calcium de |
|
La précipitation sélective
Exercice 2 : précipitation du chlorure de plomb On dispose de V1 = 10 mL d'une solution S1 de nitrate de plomb de concentration C1 = 10 10-1 mol L-1 |
|
Réactions de Précipitation - PTSI Ginette
1 On considère un litre de solution saturée en chlorure de plomb Calculer la concentration en ions Pb2+ de la solution Donnée : pKs(PbCl2(s))=48 |
|
TP n° EQUILIBRES PRÉCIPITATION - DISSOLUTION - Free
Donnée : Couleurs des principaux précipité obtenus au cours du TP : chlorure de sodium : blanc chlorure de plomb II : blanc iodure de plomb II : jaune |
|
Chimie 6 Précipitation solubilité Table des matières - Pierre Adroguer
A l'inverse une solution contenant des ions chlorure comme l'acide Considérons par exemple la dissolution du sulfate de plomb PbSO4 de pKs = 7 |
|
COURS-Precipitationpdf - Physique et chimie en PTSI à Voiron
Dans ce chapitre et les suivants nous allons étudier différents réactions (ou parle aussi d'équilibre) chimiques en solution aqueuse |
|
SMPC (S2) Année universitaire : 2019/2020 Cours de chimie des
a) Montrer que PbCl2(s) précipite b) Calculer les concentrations en ions chlorure et plomb II après précipitation c) Calculer la masse de chlorure de plomb II |
Quelle est la condition de précipitation ?
. On suppose qu'on mélange 2 solutions contenant chacune un ion du précipité.
. Les concentrations dans le mélange sont notées [Cq+]0 et [Ap-]0.
Comment savoir si il y a précipitation ?
. Ce produit peu soluble se nomme précipité et se dépose généralement au fond du récipient, il précipite.
. La formation d'un précipité peut être la suite de la réaction entre deux solutions électrolytes.
Comment faire une réaction de précipitation ?
|
CHIM105B – DS2 - Corrigé
1) (/4) Précipitation du plomb II en milieu chlorure On mélange 10 mL d'une solution de nitrate de plomb II, Pb(NO3)2, de concentration c0=10-1 mol L-1, et 10 |
|
Précipitation et dissolution Précipitation et dissolution
Donnée : produit de solubilité du chlorure de plomb Ks = 1,2 · 10−5 Elles sont successives si, au moment où la deuxième précipitation commence, |
|
Solubilité en solution aqueuse
inverse, sens de la précipitation La solution est saturée ; on ne peut pas dissoudre 2,00 g d'iodure de plomb dans 100 mL d'eau EX8 Dissolution du chlorure |
|
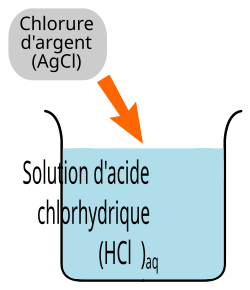
Précipitation - Produit de solubilité A – Introduction : Lors de l
Solubilité du chlorure d'argent dans la solution d'acide chlorhydrique : Soit x la Plaçons-nous à la limite de précipitation (le précipité apparaît) Dans ce cas |
|
Lanalyse de quelques cations : Pb , Fe , Cu , Cr , Co et Ni
PbCl2 chlorure de plomb précipité blanc eau à chaud Tests spécifiques: réactif Les réactions de précipitation et de complexation par l'ammoniac et par l'ion |
|
Stœchiométrie
12 nov 2006 · Br 79 904 Chlore Cl 35 453 Azote N 14 007 Soufre S 32 065 Chrome Cr 51 996 Argent Ag 107 87 Plomb Pb 207 2 Baryum Ba 137 33 Oxyg`ene O 15 999 Fig Précipitation et analyse qualitative MKNO2 |
|
R E A C T I O N S D E P R E C I P I T A T I O N
Les réactions de précipitation Dissolution d'un composé ionique : le chlorure de sodium Reprenons l'exemple de la précipitation de l'iodure de plomb: 2I− |
|
Examen du 13 janvier 2009 - durée : 2 heures - LUTES
a) Ecrire la réaction de précipitation des ions plomb (II) en présence de chlorure Même question dans le cas de l'argent (I) Pb 2+ + 2 |
|
PRÉCIPITÉS - exercices A EXERCICES DE BASE I Solubilité 1 2
VIII Précipitation préférentielle 1 • Calculer la concentration en ions Pb2+ dans une solution saturée en chlorure de plomb 2 • On met un précipité de PbCℓ 2 |