complexe cuivre ammoniaque
|
Complément à l’article « L’analyse d’un complexe
complexe mononucléaire de cuivre(II) Cu(NH 3) a 2+ et ion sulfate dans l’eau Il s’agit donc de déterminer a b et c en effectuant trois dosages : celui de l’ammoniac celui des ions sulfate et celui du cuivre contenus dans un échantillon du solide Déroulement du TP - Le professeur partage les étudiants en groupes de 4 ou 5 élèves |
|
Etude spectrochimique des complexes du Cuivre
Dans la solution B4 il se forme le complexe diaquatétraamine de Cuivre (II) : ( Cu(NH3)4(H2O)2 ) 2+ Δ = 1/ƛmax = 1/630 = 16 120 cm−1 ε = 402 L/mol/cm On réalise bien qu’à chaque ajout d’un |
|
Le complexe Cu
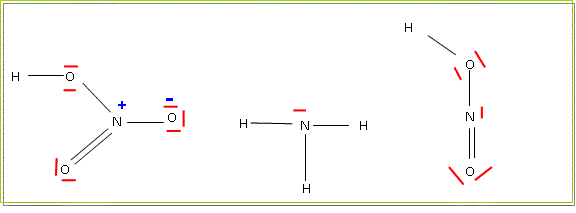
Les sels de cuivre II donnent avec l’ammoniaque en excès un complexe stable de coloration bleue nuit l’ion tétrammine cuivre II selon la réaction : Cu(H 2O) 4 2+ + 4NH 3 → Cu(NH 3)4 2+ + H 2O Pour être rejeté à l’évier les ions Cu 2+ doivent avoir une concentration comprise entre 10-4 et 10-6 mol L-1 Après un TP qui |
|
Préparation et étude spectroscopique de quelques complexes du
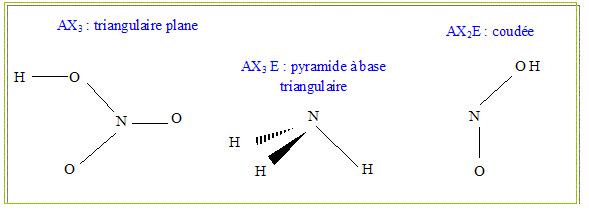
3 3 Commentaires L’eau et l’ammoniac sont des ligands monodentates au niveau de l’oxygène et de l’azote Ces ligands forment avec le cuivre des complexes de stœchiométrie : Cu(H2O) 2+ 6 (hexaaquo cuivre II) et Cu(NH 3) 4(H2O) 2 2+ (tétraamminocuivre II) en solution aqueuse |
|
TP : Synthèse et analyse d’un complexe de cuivre
Ajoutd’ammoniaque: [Cu(H 2 O) x+y] 2+ (aq) +xNH 3(aq) =[Cu(NH 3) x (H 2 O) y] 2+ (aq) +xH 2 O (‘) Solutionbleufoncédufaitdelaprésencede[Cu(NH 3) x (H 2 O) y] 2+ (aq) 3 Agiter5minutes(toutdoitêtredissous!)puisadditionner 5 mL d’éthanol Leselcom-plexeprécipite [Cu(NH 3) x (H 2 O) y] 2+ (aq) +SO 2– 4 (aq) =[Cu(NH 3) x (H 2 O) y |
Comment manipuler le complexe cuivre-éthylènediamine ?
une manipulation analogue peut être réalisée sur le complexe cuivre-éthylènediamine en préparant des solutions de rapport de concentrations éthylènediamine sur ions cuivriques égales à 1, 2, 3, 4 et l’infini. Des indications opératoires sont données dans les référen- ces [4] et [11]. 4.1.
Quels sont les avantages du cuivre ?
Le cuivre offre de telles possibilités ; il s’agit d’un métal courant, présentant une chimie riche, tant au point de vue fondamental [1] qu’au niveau des applications biologiques [2], indus- tielles [3]...
Comment doser la quantité d'ions cuivre(II) dans un complexe solide ?
But : doser la quantité d’ions cuivre(II) présente dans un échantillon du complexe solide. Test qualitatif : dissoudre quelques grains de sulfate de cuivre pentahydraté dans 5 mL d’eau, ajouter 2 ou 3 gouttes d’acide sulfurique concentré, une spatule (grand excès) d’iodure de potassium solide et 1 mL d’empois d’amidon.
Quel est le rapport des concentrations de NH3 et des ions cuivriques ?
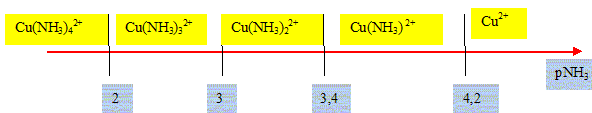
Boucher les erlenmeyers. Ces solutions sont telles que le rapport des concentrations de NH3 et des ions cuivriques varie de 0 (solution I) à (solution VI) et à l’infini, par gros excès de NH3 (solution VII). On observe un approfondissement de la couleur des solutions avec l’accroissement de la quantité de NH 3 ajoutée.
|
E Q U I L I B R E D E C O M P L E X A T I O N
Une solution d'ammoniaque (solution aqueuse d'ammoniac) NH Exemple : complexes ammoniac-cuivre (II). On considère les complexes Cu NH. |
|
Le complexe Cu
Les sels de cuivre II donnent avec l'ammoniaque en excès |
|
Synthèses des complexes
Produits : sulfate de cuivre (II) pentahydraté CuSO4 5 H2O (70 F/kg) ; solution d'ammoniac à 2 mol.L–1 ; alcool à 95 (de l'acool à brûler peut suffire) |
|
TP : Synthèse et analyse dun complexe de cuivre
Ajouter sous la hotte 3 mL d'eau et 5 mL d'ammoniaque concentré. Ajout d'eau : CuSO4 5H2O(s) + (x+y-5) H2O(l) = [Cu(H. |
|
Synthèse et caractérisation dun complexe
Synthèse du complexe. On souhaite synthétiser un sel constitué d'un complexe cuivre-ammoniac et d'ions sulfate de formule [Cu(NH. |
|
Préparation et étude spectroscopique de quelques complexes du
Le cuivre offre de telles possibilités ; il s'agit d'un métal courant présentant une Tableau 1 : Composition des solutions de complexe cuivre-ammoniac. |
|
TP : Synthèse et analyse dun complexe de cuivre
Synthèse du complexe. On souhaite synthétiser un sel constitué d'un complexe cuivre-ammoniac et d'ions sulfate de formule [Cu(NH. |
|
Étude cinétique de loxydation de lammoniac en présence dions
d'oxydation dépend de la concentration en ammoniaque et en complexe tétraammine de cuivre divalent obtenu par dissolution de l'hydroxyde Cu(OH)2 dans |
|
Contrôle des réducteurs doxygène dans leau de chaudière
les frais d'exploitation et le risque de corrosion du cuivre. Le complexe cuivre-ammoniaque circule dans le système d'eau. |
|
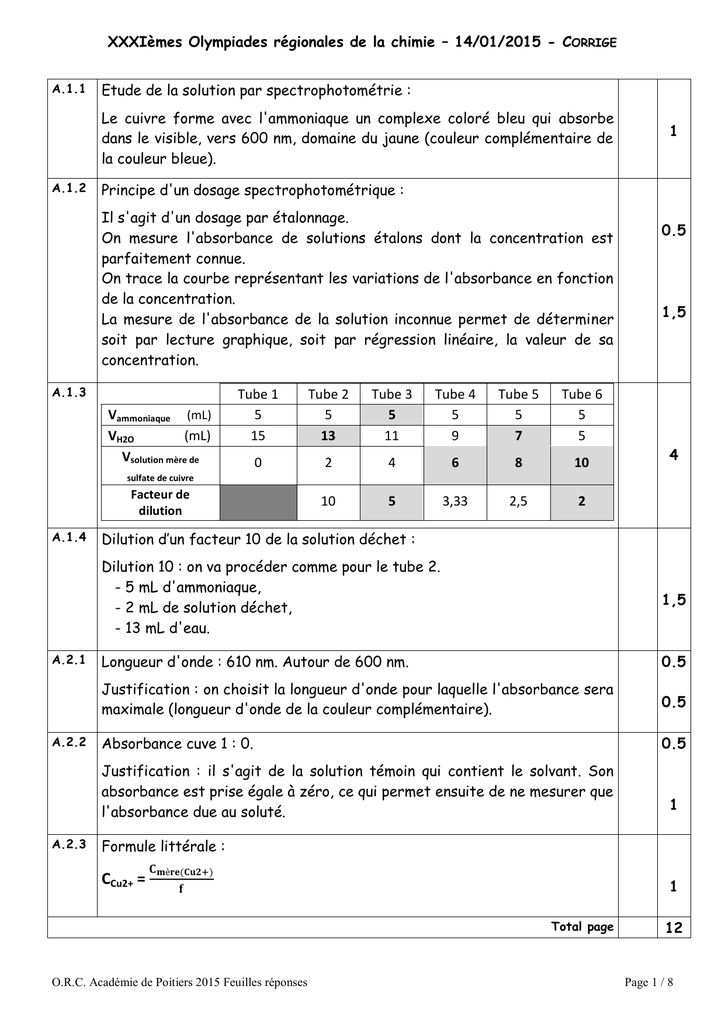
XXXIèmes Olympiades régionales de la chimie – 14/01/2015
14 janv. 2015 Le cuivre forme avec l'ammoniaque un complexe coloré bleu qui absorbe ... Equation de précipitation des ions Cu2+ en hydroxyde de cuivre ... |
|
Le complexe Cu(NH3)4
Les sels de cuivre II donnent avec l'ammoniaque en excès un complexe stable de coloration bleue nuit l'ion tétrammine cuivre II selon la réaction : |
|
Equilibre-complexationpdf
Une solution d'ammoniaque (solution aqueuse d'ammoniac) NH Exemple : complexes ammoniac-cuivre (II) On considère les complexes Cu NH |
|
Lanalyse dun complexe mononucléaire du cuivre(II)
de déterminer a b et c en effectuant trois dosages : celui de l'ammoniac celui des ions sulfate et celui du cuivre contenus dans un échantillon du solide |
|
Synthèses des complexes
L'addition d'une solution d'ammoniac à une solution de sulfate de cuivre conduit à la formation d'un ion complexe l'ion tétraammine cuivre (II) Cu(NH3)4 |
|
TP : Synthèse et analyse dun complexe de cuivre - CPGE Brizeux
Synthèse du complexe On souhaite synthétiser un sel constitué d'un complexe cuivre-ammoniac et d'ions sulfate de formule [Cu(NH |
|
TP : Synthèse et analyse dun complexe de cuivre - CPGE Brizeux
Diminution de la température pour diminuer la solubilité du sel complexe 5 Essorer sur Büchner Laver le solide avec 5 mL d'ammoniaque concentré puis 5 mL d' |
|
Tp11 Les-Complexes PDF Ammonium Cuivre - Scribd
(T1) : Lors de la dissolution du sulfate de cuivre les ions cuivre Cu2+ Lorsque l'ammoniac est en excès il se forme le complexe [Cu(NH3)4]2+ |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
EXEMPLE 2 : STABILITE D'UN COMPLEXE EN FONCTION DU PH ERREUR ! L'ion Ag+ forme avec l'ammoniac des complexes amminés : [Ag(NH3)]+ et [Ag(NH3)2]+ |
|
Étude cinétique de loxydation de lammoniac en présence d - HAL
12 mai 2020 · d'oxydation dépend de la concentration en ammoniaque et en complexe tétraammine de cuivre divalent obtenu par dissolution de l'hydroxyde |
|
Etude spectrochimique des complexes du Cuivre
d'ammoniac à 20 M : on note l'apparition d'un précipité bleu laiteux (Hydroxyde de Cuivre II) témoins du complexe Cu(OH)2 selon les réactions : |
| LES REACTIONS DE COMPLEXATION 1 Les complexes |
| TP : Synthèse et analyse d’un complexe de cuivre |
| Complément à l’article « L’analyse d’un complexe |
| Le complexe Cu - sgenmidipyfr |
| Préparation et étude spectroscopique de quelques complexes du |
| Searches related to complexe cuivre ammoniaque filetype:pdf |
|
E Q U I L I B R E D E C O M P L E X A T I O N
Expérience 2: On mélange • Une solution d'ammoniaque (solution aqueuse d' ammoniac) NH Exemple : complexes ammoniac-cuivre (II) On considère les |
|
TP3 : Analyse dun complexe du cuivre II
d'ammoniaque concentré; agiter 5 minutes; additionner alors 5 mL d'éthanol Le sel complexe précipite; placer l'erlenmeyer dans un bain de glace pendant 40 |
|
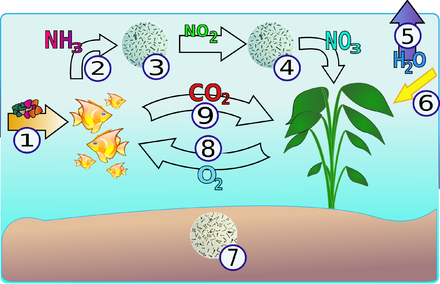
Etude dune eau polluée
Etude de l'ion complexe formé par réaction entre les ions cuivre II et l'ammoniac Dosage des ions nitrate dans un échantillon d'eau polluée 3 Réduction des |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
Un complexe est un édifice polyatomique dans lequel un atome ou un ion L'ion Ag+ forme avec l'ammoniac des complexes amminés : [Ag(NH3)]+ et |
|
TD: Réactions de complexation - PCSI-PSI AUX ULIS
Exercice n°2: Formation de l'ion complexe tétrammine cuivre (II) On mélange 10 mL solution d'ammoniaque de concentration 0,10 mol L-1 On suppose que |
|
TP 5 : Complexes
5 oct 2007 · complexes et essayer de trouver leur formule théorique Nitrate de cuivre (II) mL d'ammoniaque (NH3) 4 M et 100 mL d'eau distillée |
|
TP: Synthèse et analyse de complexes
Synthèse de complexes du cuivre EXP2/ Verser dans 3 tubes à essai : (T1) : une solution de sulfate de cuivre (T2) : une solution d'ammoniaque ; boucher le |