Déterminer la concentration en ions oxonium ou en ion hydroxyde ?
|
[H3O ] = 10
Déterminer la concentration en ions oxonium et en ion hydroxyde dans les solutions suivantes pH [H3O + ] ( en mol L-1 ) [HO - ](en mol L-1 23 46 64 |
|
Exercice 2 : « Concentration en soluté et pH »
Déterminer la concentration en ion oxonium H3O+ de chacune de ces eaux Concentration en ion oxonium : [H3O + ] = 10 –pH ; Eau de chaux : [H3O + ] = 10 |
|
CORRECTION EXERCICE C9
Lorsqu'on dilue la solution la concentration en ions oxonium diminue et celle des ions hydroxyde augmente n°13 p°335 L'acide des fourmis 13 1 Le pH d'une |
|
Activite documentaire
concentration en ions oxonium est élevée par rapport à celle en ions hydroxyde - Soit [H3O+] < [HO¯] alors la solution est basique et d'autant plus |
|
1 Connaissant la concentration en ions hydroxyde des quatre
Connaissant la concentration en ions hydroxyde des quatre solutions aqueuses suivantes déterminer la concentration en ions oxonium [HO-]éq (mol L-1) |
|
Complétez le tableau sans justifier vos résultats
Déterminer la concentration en ion hydroxyde HO − de l'eau de chaux 5 Dans l'eau de chaux expliquer quels sont les ions majoritaires: les ions oxonium H3O+ |
|
C_CH11 – CORRIGÉ DES EXERCİCES
détermination de la concentration en ions L-1 Lorsqu'on dilue la solution la concentration en ions oxonium diminue et celle des ions hydroxyde augmente |
Comment calculer la concentration en ion hydroxyde ?
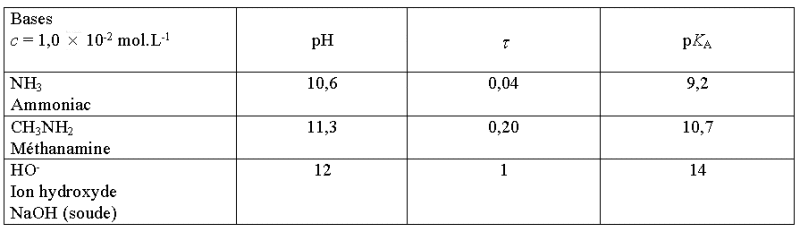
Pour une solution basique de concentration en ions hydroxyde donnée, on peut calculer le pH en utilisant le pOH ("pOH = -log[OH⁻]") et la relation "pH = 14 - pOH".
La fonction logarithmique associée au pH est "f(x) = -log(x)".[H3O+] est la concentration molaire exprimée en mole par litre (mol.
L-1) c° est la concentration standard, c'est une constante qui vaut 1,00 mol.
L-1 à condition que la concentration en ion oxonium soit bien exprimée en mole par litre.
|
[H3O ] = 10
Déterminer la concentration en ion oxonium ou hydroxyde Déterminer la concentration en ions oxonium et en ion hydroxyde dans une solution de pH = 113. |
|
CORRECTION EXERCICE C9
Lorsqu'on dilue la solution la concentration en ions oxonium diminue et celle des ions hydroxyde augmente. n°13 p°335 L'acide des fourmis. |
|
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
À quel couple acide/base appartient l'ion hydroxyde HO– ? Déterminer la concentration molaire C1 en dioxyde de soufre de ce vin et en déduire que sa. |
|
Correction du TP n°7 : Dosage acido-basique 2008-2009 - 1ere S
enfin de déterminer la concentration de l'espèce chimique contenue dans un une solution aqueuse d'hydroxyde de sodium à 20% elle donc constituée d'ions. |
|
CORRIGE
A l'aide du tableau d'avancement déterminer la valeur de xf. - Calcul de la concentration en ions oxonium. On a pH = 32 d'où : [H3O+. (aq)] =6 |
|
Les acides et les bases : p 31 Acide méthanoïque. Une solution
Calculer la concentration molaire effective en ions hydroxyde dans la solution. L'acide conjugué de l'ammoniac NH3 est l'ion ammonium : . |
|
Chapitre 1 Acides et bases
où H3O+ est l'ion hydronium ou oxonium |
|
RÉACTIONS ACIDO-BASIQUES
Le pH et la concentration en ions oxonium H3O+ varient en sens inverse du pH d'une solution permet de calculer sa concentration en ion hydroxyde. |
|
Les acides et les bases + H+ + H3O+ + H+ + NH4
Calculer la concentration molaire effective en ions hydroxyde dans la solution. étant plus faible que celle en H3O+ ; c'est l'ion hydronium H3O+ qui ... |
|
Préparation aux Olympiades Internationales de Chimie 2020 Table
gué est l'ion oxonium H3O+ (l'ion H+ n'existe pas en solution aqueuse) d'une faible concentration d'ions oxoniums et hydroxydes de σ = 5 5 10−4 S·m−1 |
|
Télécharger ce fichier pdf - Labolycée
noter si la solution a été diluée avant le titrage : la concentration trouvée sera donc celle À quel couple acide/base appartient l'ion hydroxyde HO– ? À l' aide des questions 3 3 2 et 3 5, déterminer la quantité de matière d'ions hydroxyde |
|
Transformations chimiques en solution aqueuse - Chimie en PCSI
CONCENTRATION DE TRACE DU DIAGRAMME ions Fe3+ ou Fe2+, et quels sont les domaines d'existence des solides Fe(OH)2(s), de(OH)3(s) oxydé, mais sous laquelle de ces formes : Fe2+ ou l'hydroxyde Fe(OH)2(s) ? en milieu acide : forme acide de l'eau : ion oxonium H3O+ Le tracé est désormais terminé |
|
BTS BAT ET TP : Exercices sur le pH – Module C4
Donnez la relation entre le pH et la concentration en ions hydronium d'une solution aqueuse ion hydroxyde Bien entendu, dès que l'ion hydroxyde rencontre l'ion oxonium, cela redonne deux molécules Le dosage est terminé 3 Quelle |
|
Chapitre 1 : Interactions fondamentales et particules élémentaires
solution contenant la concentration en ion hydroxyde la plus faible : [HO - (aq)]A = 1,0 10 –11 nécessairement des ions oxonium H3O + (aq) et hydroxyde HO Pour finir on homogénéise la solution en retournant la fiole jaugée 3 ou 4 |
|
I Activité documentaire : la pollution aux plastiques, le - AlloSchool
terminer la concentration massique du bleu patenté et de la tartrazine dans le oxonium : pH = -log [H3O+]f À partir de la concentration en ions hydroxyde : M Suet Physique- l'ion oxonium H3O+ étant l'acide le plus fort qui puisse exister |
|
AVANCEMENT FINAL DUNE RÉACTION CHIMIQUE - Lydie Germain
21 oct 2010 · Connaissant la valeur de la concentration et du pH d'une solution réagissant avec une molécule d'eau forme l'ion oxonium 3 est ici le nombre sans unité qui mesure la concentration en ions oxonium exprimé en mol L –1 |
|
Réactions acido-basiques - Cours, examens et exercices gratuits et
L'ion HO− est l'ion hydroxyde contenant, non cet acide, mais l'ion oxonium condition 0 ≤ pH ≤ 14 correspond à des concentrations en ions oxonium comprises entre 1 mol · L−1 et 1 · 10−14 mol · L−1 problème est terminé ; |
|
Exercice I La bouillote magique (6,5 points) - Lycée Pierre Corneille
L'ion hydroxyde HO- est une base forte en solution aqueuse Déterminer le pH de la Déterminer la concentration molaire C'A de l'acide ascorbique dans la solution S ainsi préparée 3 2 3- Pourquoi les ions oxonium H3O+ disparaissent lors de l'hyperventilation ? Pour finir, des corrections respiratoires et rénales |