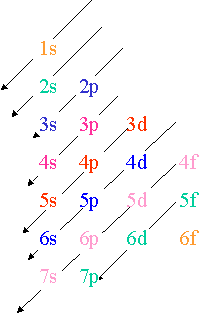
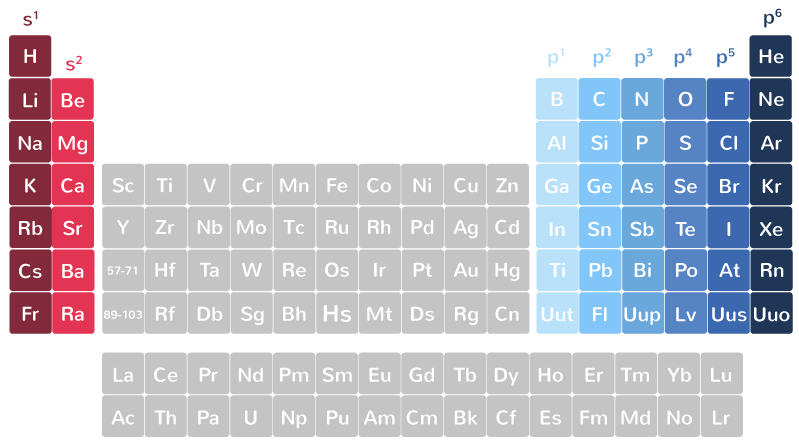
structure electronique 1s 2s
|
Chapitre 1: Structure de latome ; Constituants de la matière
1 Donner les sous-couches électroniques comprises dans la couche n = 4 2 Combien d'orbitales une sous-couche électronique 2p contient-elle |
|
Couches principales Sous-couches Ordre de remplissage des sous
FICHE MÉTHODE – ÉTABLIR LA STRUCTURE ÉLECTRONIQUE 1s 2 électrons sur la sous-couche 2s et 2 électrons sur la sous-couche 2p On note la structure |
|
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
Les atomes forment des liaisons pour acquérir la configuration électronique des gaz rares (règle de l'octet) Pour acquérir la configuration d'un gaz rare le |
|
La structure électronique des atomes
La structure électronique des atomes Page 2 Le rayonnement électromagnétique • N B les orbitales 1s 2s 2p 3s 3p 3d 4s existent seulement dans |
|
Structure électronique des atomes
9 oct 2017 · 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f etc Période 1 : remplissage progressif du niveau 1s le faire entourer d'une couleur 2 éléments Périodes 2 |
|
Thème 12 La structure électronique des atomes
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d 7p Quel atome ou ion a la configuration électronique : 1s 2 2s 2 2p 6 3s 2 3p |
Comment calculer structure électronique ?
Pour trouver la configuration électronique d'un atome, tu dois d'abord connaître le nombre d'électrons qu'il possède.
Le numéro atomique de l'aluminium étant de , il possède électrons .
Tu répartis ensuite les électrons entre les différentes orbitales.Quelle est la structure électronique de l'ion soufre S2 ?
Exercice2 : soufre
.
2) Cet atome possède 16 électrons.
Sa structure électronique est donc : (K)2(L)8(M)6.Quel atome à pour configuration électronique 1s 2 2s 2 2p 4 ?
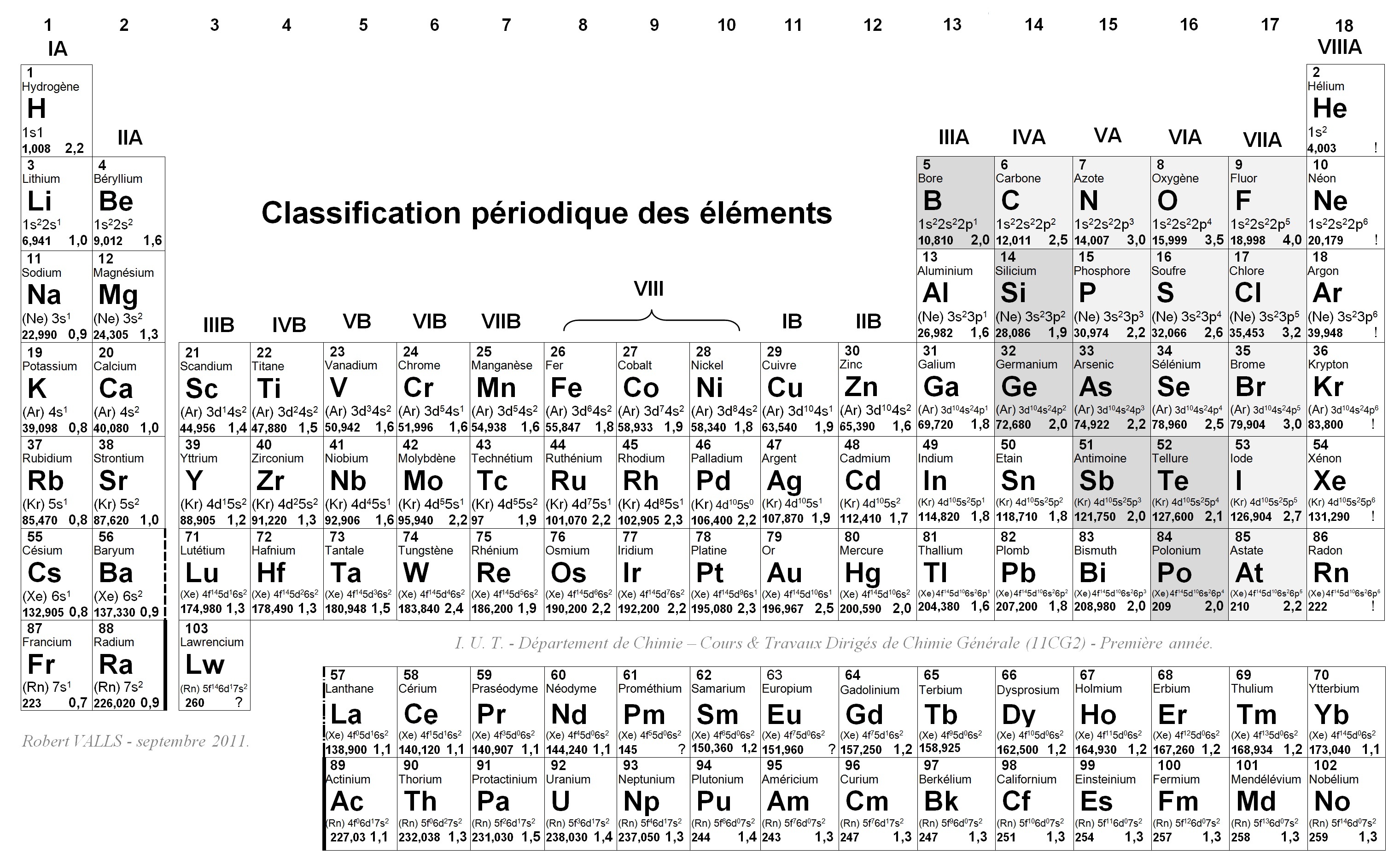
Le lithium, avec trois électrons, présente, à l'état fondamental, la configuration 1s2 2s1, tandis que l'oxygène, avec huit électrons, présente, à l'état fondamental, la configuration 1s2 2s2 2p4, et que l'aluminium, avec treize électrons, présente, à l'état fondamental, la configuration 1s2 2s2 2p6 3s2 3p1.
- 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p5 L'iode possède 7 électrons de valence : 5s2 5p5 Rem : le numéro atomique de l'iode est donc Z = 53.
|
Chapitre 1 - Configuration électronique
1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d. * Pour l'atome de carbone (Z = 6 donc 6 électrons à répartir) : 1s2 2s2 2p2. * Pour l'atome d'oxygène (Z = 8 |
|
De la structure à la polarité Fiche
Une couche électronique ne peut contenir qu'un nombre limité d'électrons : 2 électrons sur les sous-couches 1s 2s et 3s ; 6 électrons. |
|
La structure électronique des atomes
l'énergie d'une orbitale est entièrement déterminée par le nombre quantique principal même si les formes des orbitales sont différentes. 1s < 2s = 2p <. 3s = |
|
Hydrogéno??des et méthode de Slater
Il a donc une structure électronique semblable à celle de l'atome la configuration électronique de l'élément et l'ordonner selon : (1s) (2s2p) (3s |
|
Thème 12 La structure électronique des atomes
l'énergie d'une orbitale est entièrement déterminée par le nombre quantique principal même si les formes des orbitales sont différentes. 1s < 2s = 2p <. 3s = |
|
Fiche de synthèse n° 1.a Structure des molécules et des ions
Les sous-couches de type s (1s 2s |
|
Symbole Nombre délectrons Configuration électronique a. Mg 12 1s
1s. 2. 2s. 2. 2p. 6. 3s. 2. 3p. 6. Symbole. Configuration électronique colonne ; 2 électrons de valence. Configuration électronique : 1s. 2. 2s. |
|
LA LIAISON CHIMIQUE 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f
liaisons ioniques comme avec les liaisons covalentes les atomes ont tendance à acquérir une configuration électronique stable. Configuration électronique. Il |
|
Chimie générale et organique Séries de Travaux Dirigés et Solutions
a) La configuration électronique des éléments dont le numéro atomique varie de Z=3 à Z=10 : 1) Z = 3 3Li : 1s. 2. 2s. 1. 1 électron célibataire. |
|
CHAPTER 9
2S + 1 equals 2 thus the term symbol is written 2S In helium a second electron can occupy the 1s shell provided it has the opposite spin The total spin angular momentum is therefore zero as is the total orbital an-gular momentum The term symbol is 1S as it will be for all other atoms with complete electron shells |
|
APPENDIX I ELECTRONIC STRUCTURE AND VALENCES OF THE ELEMENTS
APPENDIX I - ELECTRONIC STRUCTURE AND VALENCES OF THE ELEMENTS* Period Z Element Electronic Structure Common Valences 1 11 H 1s +1 2 He 1s2 0 2 3 1Li 1s22s +1 24 Be 1s 2s2 +2 25 B 21s 2s 2p1 +3 6 C 21s22s 2p2 +4 +2 7 2N 31s 2s22p +5 +3 -3 8 2O 1s22s 2p4-2 9 2F 1s22s 2p5-1 210 6Ne 1s 2s22p 0 3 11 Na [Ne]3s1 +1 |
|
Searches related to structure electronique 1s 2s PDF
1s2s of the 1s-2stwo-photon (Doppler-corrected) quantum transition of hydrogen re-ported in Ref [1] is f(exp) 1s2s = 2466061413187 035(10) kHz (1) [the uncertainty in the measured frequency is ?f(exp) 1s2s = 10 Hz] Moreover Ref [2] reported a frequency of 2466061413187 018(11)kHz con?rming the above result |
How many electrons are in a 2p atom?
This is because Hund's Rule states that the three electrons in the 2p subshell will fill all the empty orbitals first before filling orbitals with electrons in them. If we look at the element after Nitrogen in the same period, Oxygen (Z = 8) its electron configuration is: 1s 2 2s 2 2p 4 (for an atom).
What is the difference between a 1s and 2s orbital?
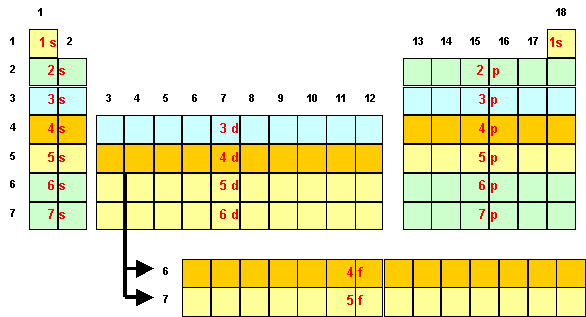
The 1s orbital and 2s orbital both have the characteristics of an s orbital (radial nodes, spherical volume probabilities, can only hold two electrons, etc.) but, as they are found in different energy levels, they occupy different spaces around the nucleus. Each orbital can be represented by specific blocks on the periodic table.
What is the electronic structure of hydrogen?
Hydrogen has an electronic structure of 1s 1. We have already described this orbital earlier. Carbon has six electrons. Two of them will be found in the 1s orbital close to the nucleus. The next two will go into the 2s orbital. The remaining ones will be in two separate 2p orbitals.
What is the electron configuration of oxygen?
If we look at the element after Nitrogen in the same period, Oxygen (Z = 8) its electron configuration is: 1s 2 2s 2 2p 4 (for an atom). Oxygen has one more electron than Nitrogen and as the orbitals are all half filled the electron must pair up. Aufbau comes from the German word "aufbauen" meaning "to build."
Quel est le nombre maximum d'électrons que peuvent contenir les couches 1s 2s et 3s NS ?
. Au-delà de 18 électrons, il faut suivre la règle de Klechkowski (doc.
Quel est le numéro atomique de l'atome dont la structure électronique est 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 ?
Quel est l'atome possédant la structure électronique 1s2 2p2 2p6 3s2 3p2 ?
|
Chapitre 3 :Structure électronique des atomes
Chapitre 3 : Structure électronique des atomes Structure de la matière Page 1 sur 5 I Nombres quantiques A) Origine théorique La résolution de l'équation de |
|
LA STRUCTURE ELECTRONIQUE DES ATOMES
LA STRUCTURE ELECTRONIQUE DES ATOMES Les éléments suivants sont à connaître, car ils permettent de « prévoir » le comportement des atomes en |
|
La structure électronique des atomes
Elle résoud complètement le problème de la structure électronique des atomes Comme dans le cas de la théorie de Bohr, les états énergétiques fournis par l' |
|
SM2 – Structure électronique des atomes - I / Optique
SM2 – Structure électronique des atomes niveaux d'énergie électroniques ℰп de l'atome ne dépendent que du nombre quantique principal |
|
Structure électronique des atomes - Étienne Thibierge
12 déc 2018 · ⊳ Établir la configuration électronique d'un atome dans son état fondamental La connaissance des exceptions à la règle de Klechkowski n'est |
|
Structure électronique des atomes Structure - Étienne Thibierge
9 oct 2017 · Écrire sa configuration électronique Dans le tableau périodique, il se trouve à droite du carbone et au dessus du phosphore En déduire le |
|
Structure électronique des atomes - IMPMC
La configuration électronique définit l'énergie de l'atome à N électrons (dans l' approximation de champ moyen central) : cette énergie est donnée par la somme |
|
Règles de remplissage pour les atomes polyélectroniques
Règle de Hund : pour une sous-couche donnée, la configuration électronique de plus basse énergie est obtenue en plaçant un maximum d'électrons de même |
|
Thème 12 La structure électronique des atomes - DSFM
Exemple: Donnez les différents ensembles de nombres quantiques qui caractérisent un électron situé dans une orbitale 5p Page 23 T12 La configuration |