transition électronique de l'atome d'hydrogène
|
Chapitre 2 :Quantification de lénergie de latome dhydrogène
Chaque état possède une énergie invariante (quantification des niveaux d'énergie de l'hydrogène) Postulat optique : La transition entre deux états accessibles |
|
Chapitre II Latome dhydrogène
Comme ce sont les seules fonctions d'onde électroniques d'un atome connues sans approximation elles servent d'éléments de base pour la construction de |
|
Chapitre XI Transitions électroniques Spectroscopie UV-visible 1
Diagramme énergétique et quelques transitions permises de l'atome d'hydrogène L'atome d'hydrogène est le seul atome dont l'énergie est indépendante de l et |
|
Latome dhydrogène
The continuous transition from micro- to macro-mechanics E Schrödinger Collected papers on wave mechanics Chelsea Publishing New York 1982 pp 41-44 |
|
Spectroscopie de latome dhydrogène Vers une mesure absolue de
24 oct 2001 · Spectroscopie de l'atome d'hydrogène Vers une mesure absolue de la fréquence de la transition 1S-3S Gaëtan Hagel To cite this version: |
|
Spectroscopie haute précision de la transition 1S-3S de latome d
micro-onde pour l'hydrogène électronique (∼1 GHz) passe dans le domaine infra-rouge lointain (∼6 µm) Par contre la force d'oscillateur de la transition de |
Quelle est la structure électronique de l'atome d'hydrogène ?
1s1Le numéro atomique de l'atome d'hydrogène H est Z = 1.
Sa structure électronique est (1s)1.
Il possède un électron célibataire.Quelle est la transition électronique ?
Les transitions électroniques décrivent le passage d'un électron d'un niveau d'énergie à un autre. .
Dans le cas le plus simple d'un atome d'hydrogène (un électron et un proton), l'électron est piégé dans le champ électrique créé par le proton.Comment calculer la transition electronique ?
Etransition = RH(1 / m2 − 1 / n2).
Ces spectres ont grandement contribué à asseoir la mécanique quantique lorsqu'on se rendit compte que l'on observait là la transition électronique. entre les niveaux n et m de l'atome.- L'atome hydrogénoïde est une structure atomique simple qui ne possède qu'un seul électron.
Les atomes d'hydrogène forment une liaison covalente lorsqu'ils partagent leur électron de valence avec un autre atome.
|
Spectroscopie de latome dhydrogène. Vers une mesure absolue de
24 oct 2001 absolue de la fréquence de la transition 1S-3S. Gaëtan Hagel. To cite this version: Gaëtan Hagel. Spectroscopie de l'atome d'hydrogène. |
|
Chapitre XI Transitions électroniques Spectroscopie UV-visible 1
Il devient négligeable dans les états F et on a confondu dans une même colonne les valeurs J = 7/2 et 5/2. 2.2.3. Spectre d'émission de l'atome d'hydrogène. Le |
|
Corrigé de la série de TD N 2 Exercice 1 Exercice 2
structure électronique semblable à celle de l'atome d'hydrogène. (a) Détermination de la transition électronique de la raie m ??? 1 m2 = 0 ? ¯? = 1. |
|
Exercice n°1 : (8 points) Ici absorption de ? à partir du niveau n=2
Combien y a-?t-?il d'orbitales atomiques dégénérées dans une couche électronique n de l'atome d'hydrogène ? (1 pt). 1 ?nm. = RH Z2 (. 1 n2 ?. 1 m2 ). Page 2 |
|
Excitation et ionisation des atomes dhydrogène et dhélium par des
7 feb 2008 F La section efficace totale d'interaction photon-atome. 277. G Amplitude de transition avec état fondamental amélioré. |
|
Chapitre 12 : Physique quantique
29 ago 2013 Pour l'atome d'hydrogène l'énergie En (en eV) de chaque niveau est donné ... émise lors de la transition électronique du niveau n = m au ... |
|
Série de TD N?2
n et m de la transition électronique tel que n<m. Calculer la longueur d'onde relative à la même transition dans l'atome d'hydrogène. En déduire son. |
|
SERIE DEXERCICES SUR Pl 4.· MVEAUX DTNEKGIE
L'atome d'hydrogène est dans son état fondamental. basse pression est due à la transition électronique entre les niveaux 2 et 3. |
|
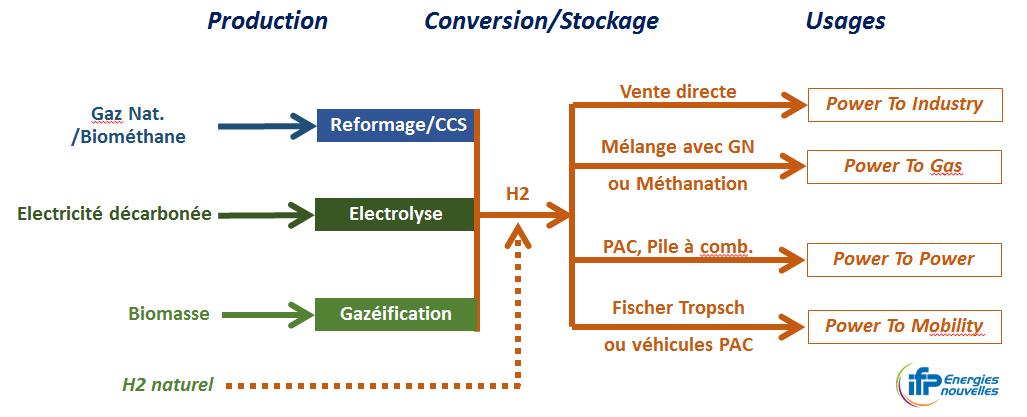
Plan de déploiement de lhydrogène pour la transition énergétique
poursuite de la transition énergétique vers la neutralité carbone à l'horizon agroalimentaire métallurgie |
|
Notations des états et transitions spectroscopiques
Exemple : O2+ est un atome d'oxygène deux fois ionisé. La configuration électronique des ions atomiques se détermine comme pour les atomes (voir ci?dessus). VI. |
|
Modèle de Bohr de l’atome d’hydrogène (leçon) Khan Academy
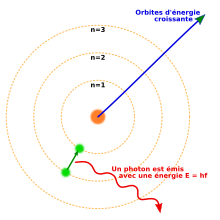
La lumière rouge de l’atome d’hydrogène est donc émise pour la transition électronique de la couche 3 à la couche 2 Note : la formule de Rydberg est la même que celle utilisée dans les exercices 3 1 et 3 2 mais avec d’autres unités |
|
Chapitre 2 : Spectre des Hydrogénoïdes et Modèle de BOHR
Chaque saut de l'électron d'un niveau à un autre est appelé une transition électronique Pour revenir sur cet état de base il doit restituer de l'énergie Cette énergie sera émise sous forme d'énergie lumineuse L'énergie du photon émis est donnée par la relation de Planck : E = h ? |
|
Chapitre II - sorbonne-universitefr
Les solutions de l’équation de Schrödinger pour l’atome d’hydrogène revêtent une importance particulière Comme ce sont les seules fonctions d’onde électroniques d’un atome connues sans approximation elles servent d’éléments de base pour la construction de fonctions approchées pour les autres atomes et les molécules 2 1 |
|
Chapitre 2 : Structure électronique des atomes
I 2 3 Spectre de rayonnement de l’atome d’hydrogène Le passage de l’électron d’un n iveau n 1 à un niveau n 2 s’accompagne d’une variation de l’énergie de l’atome ; Si n 2 n 1 l’atome absorbe de l’énergie et E = E 2-E 1 0 Si n 2 n 1 l’atome émet de l’énergie et E = E 2-E 1 0 Et dans les deux cas : |
|
Searches related to transition électronique de l+atome d+hydrogène PDF
dérite par l’életron autour du noyau de l’atome d’hydrogène qui est aratérisée par la valeur n=1 déterminer: •1 le rayon de la première orbite en ( A°) •2 la vitesse de l’életron pour l’état fondamental de l’atome d’hydrogène •3 les énergies qui correspondent aux trois premiers niveaux ( en eV) •Données |
Comment déduire la transition effectuée par un électron de l'atome d'hydrogène ?
Avec la longueur d'onde d'une radiation émise (ou absorbée) par un électron de l'atome d'hydrogène, il est d'abord possible de déduire la transition effectuée.
Comment est constitué l’atome ?
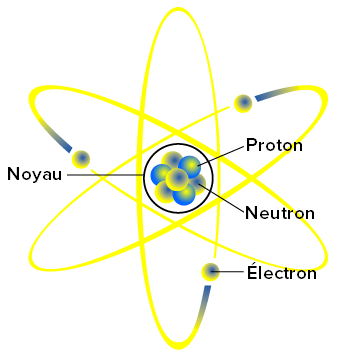
CHAPITRE I : STRUCTURE DE LA MATIERE CONSTITUTION DE L’ATOME 1. Stutue de l’atome. - Le noyau et les électrons. - Les atomes sont onstitués d’un noyau très dense, chargé positivement, entouré d’életrons (harge életrique négative). - Le noyau est constitué de deux types de particules (protons et neutrons) appelées nucléons.
Qui a inventé l'hydrogène ?
Bohr fût le premier à la reconnaître en introduisant l'idée de quantification dans son modèle de la structure de l'atome d'hydrogène, et il fût ainsi capable d'expliquer le spectre d'émission de l'hydrogène et des autres systèmes hydrogénoïdes.
Quelle est la configuration électronique du chlore ?
Exemple du chlore Le chlore (Cl) dispose de Z=17 électrons, et possède la configuration électronique 2: 1s 2s22p63s23p5. On étudie dans cet exemple un électron de valence (c'est-à-dire appartenant à la dernière couche électronique, ici 3s23p5) : Ainsi, la charge effective pour un électron de la sous-couche 3s ou 3p sera
Comment calculer transition electronique ?
. Ces spectres ont grandement contribué à asseoir la mécanique quantique lorsqu'on se rendit compte que l'on observait là la transition électronique. entre les niveaux n et m de l'atome.
Quelles sont les différentes transitions electroniques des molécules ?
. Par contre une transition avec changement de spin est interdite selon les deux règles.
|
Chapitre XI Transitions électroniques Spectroscopie UV-visible 1
Il devient négligeable dans les états F et on a confondu dans une même colonne les valeurs J = 7/2 et 5/2 2 2 3 Spectre d'émission de l'atome d'hydrogène Le |
|
Spectroscopie des transitions électroniques des cations
1 avr 2015 · à 6563 Å) qui trace la recombinaison électronique de l'hydrogène 2 1 Structure du naphtalène et numérotation de ses sites atomiques 52 |
|
Atome dhydrogène et hydrogénoïdes
Dans ce chapitre nous allons nous intéresser à l'atome d'hydrogène, le aux transitions radiatives entre niveaux des ions multichargés sont beaucoup interactions entre moments magnétiques électronique et nucléaire (cf "terme de contact |
|
Exercice n°1 : (8 points) Ici absorption de λ à partir du niveau n=2
Les orbitales atomiques ayant la même énergie sont dites dégénérées Une couche électronique n de l'atome d'hydrogène a une énergie En dépendant |
|
Physique quantique - Physique terminale S
29 août 2013 · Pour l'atome d'hydrogène, l'énergie En (en eV) de chaque niveau émise lors de la transition électronique du niveau n = m au niveau n = p, |
|
Spectroscopie haute précision de la transition 1S-3S de latome d
service électronique : les bons plans verts de Brigitte Delamour, la maitrise et la L'étude poussée du spectre de raie de l'atome d'hydrogène fut le moteur du |
|
Quantification des niveaux dénergie - Académie dOrléans-Tours
A la découverte de la quantification des niveaux d'énergie électroniques Type d' activité électroniques d'un atome d'hydrogène est appelé transition |
|
Chapitre 10: Etats énergétiques quantifiés - Alrlu
Etude expérimentale du spectre d'émission de l'atome d'hydrogène En comparant le transitions électroniques d'une orbite vers une autre se font par sauts |