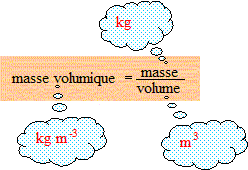masse volumique acide chlorhydrique
|
ACIDE CHLORHYDRIQUE 33%
- Densité: 1 16+/-0 015 - Stockage: Tenir à l'abri de la lumière de la chaleur et du froid - Composition: Acide chlorhydrique en solution Précautions d |
|
Acide chlorhydrique 37%
m) Densité relative 120 g/cm3 à 25 °C n) Hydrosolubilité Soluble (réaction ADR/RID: ACIDE CHLORHYDRIQUE IMDG: HYDROCHLORIC ACID IATA: Hydrochloric acid |
|
Acide chlorhydriqueconc-30/36% solution aqueuse
Masse moléculaire 7647-01-0 017-002-01-X 231-595-7 MW4025000 36 46 g/mol о о acide chlorhydriqueconc-30/36 solution aqueuse: TA-Luft Klasse 5 2 4/III |
|
Chlorure dhydrogène (ou acide chlorhydrique) et solutions aqueuses
Masse molaire 3646 Point de fusion - 1142 °C Point d'ébullition - 849 °C Densité 1045 g/cm à - 55 °C Densité gaz / vapeur 1268 Pression de vapeur |
|
Exercice 2 : Fabrication et dosage dune solution dacide chlorhydrique
Fabrication et dosage d'une solution d'acide chlorhydrique Version adaptée : 1) Déterminer la masse volumique du chlorure d'hydrogène gazeux à la température |
|
Fiche de Données de Sécurité: Acide chlorhydrique
Les ingrédients sont classés par ordre décroissant en poids ou en volume des ingrédients au moment de la formulation Attention: flux de masse ou |
Quelle est la masse volumique de l'acide chlorhydrique ?
T° fusion
−30 °C, solution à 37 % T° ébullition 48 °C , 38 % HCl Solubilité 700 g l−1 (eau) Masse volumique environ 1,19 g cm−3 à 20 °C (solution à 37 %) Quelle est la masse volumique de l'acide ?
Lorsqu'il est destiné à être employé comme électrolyte pour batterie au plomb, l'acide est dilué à une concentration de 29 à 32 % (soit [H2SO4] ≈ 4,2 à 5 mol/l ), avec une masse volumique de 1 250 à 1 280 kg/m3, soit environ 30 °Bé.
Quelle est la densité du HCL 37% ?
La solution concentrée de HCl contient 37,0 % de HCl et a une densité de 1,19 g/mL .
- densité. 1,2 g/mL à 25 °C (lit.)
|
ACIDE CHLORHYDRIQUE 33%
- Densité: 1.16+/-0.015. - Stockage: Tenir à l'abri de la lumière de la chaleur et du froid. - Composition: Acide chlorhydrique |
|
ENVIROGUIDE LE CHLORURE DHYDROGENE ET LACIDE
Masse volumique. Acide chlorhydrique. Chlorure d'hydrogene. 11391 g/ml. 1 |
|
Acide chlorhydrique 23%
Jul 19 2017 calcaires |
|
Travail dirigé 5 : La concentration dune solution
Calculer la concentration molaire d'une solution d'acide chlorhydrique HCl sachant que de soluté et la masse volumique de cette solution. |
|
Cette épreuve est constituée de trois exercices. Elle comporte
C on introduit un excès d'une solution d'acide chlorhydrique dans un flacon contenant un Masse volumique de l'acide propanoïque pur : ? = 0 |
|
Premier exercice
suivantes : « Acide chlorhydrique masse volumique : 1190 kg.m. -3. ; pourcentage en masse d'acide pur : 37 ; masse molaire de chlorure d'hydrogène HCl : 36 |
|
Chlorure dhydrogène (ou acide chlorhydrique) et solutions aqueuses
L'acidification de l'eau de boisson par l'acide chlorhydrique jusqu'à pH 2 provoque chez le rat exposé pendant 21 semaines |
|
Nom : Groupe : ______ Date :
Déterminer la masse de l'acide chlorhydrique (mHCl) dans le premier calorimètre concentration molaire et du volume de l'acide chlorhydrique (HCl). |
|
FICHE TECHNIQUE ACIDE CHLORHYDRIQUE 30%
Apr 19 2005 ACIDE CHLORHYDRIQUE 30%. FORMULE: HCl. No. CAS : 7647-01-0. Chlorure d'hydrogène. No. CE : 231-595-7. Acide chlorhydrique. ASPECT VISUEL. |
|
Acide chlorhydrique < 37%
Acide chlorhydrique < 37%. Version. 5.1. Date de révision: 07-28-2021. Numéro de la FDS: 10000001219. Date de dernière parution: 04-13-2021. |
|
Acide chlorhydrique — Wikipédia
Nom Substance Détails Chlorure d'hydrogène anhydre N° CAS 7647-01-0 Etat Physique Gaz Masse molaire 3646 Point de fusion - 1142 °C Point d'ébullition - 849 °C Densité 1045 3g/cm à - 55 °C Densité gaz / vapeur 1268 Pression de vapeur 4 220 kPa à 20 °C Point critique Pression : 83 10 kPa |
|
Fiche technique Produit : Acide chlorhydrique 23 %
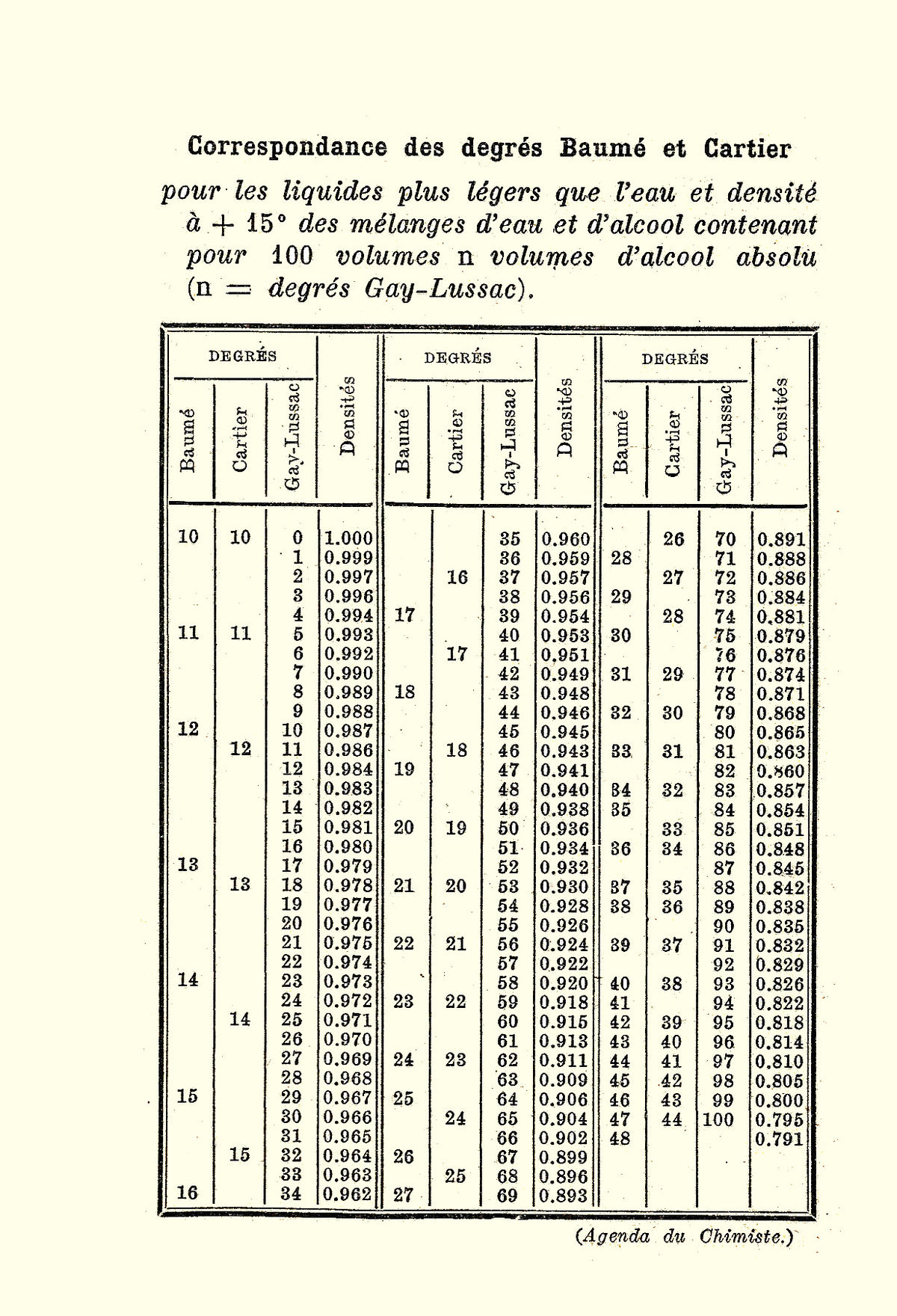
Produit : Acide chlorhydrique 23 N° de fiche : 0008 indice 4 du 04/06/09 Code produit : 00008 Caractéristiques techniques Valeur typique Méthodes Masse volumique à 20°C (Kg/l) 1110 – 1130 I824-2 Méthode 6 Degré baumè 14 - 17 Aspect Clair légèrement jaune Titre acidimètrique ( en poids ) 22 - 26 |
|
Fiche technique
Produit : Acide Chlorhydrique 32 N° de fiche : 0008 indice 5 du 02/05/11 Code produit : 00008 Caractéristiques techniques Valeur typique Méthodes Masse volumique à 20°C (Kg/l) 1160 – 1190 I824-2 Méthode 6 Degré baumé 20 – 22 Aspect Clair légèrement jaune Titre acidomètrique ( en poids) 30 – 36 *Teneur en fer (ppm) < 6 |
Qui a découvert l'acide chlorhydrique ?
Voir la page de discussion pour plus de détails. L'acide chlorhydrique a été découvert au voisinage de l'an 800 par l' alchimiste Jabir Ibn Hayyan, qui l'obtint en mélangeant du sel ( chlorure de sodium, NaCl) et du vitriol ( acide sulfurique, H 2 SO 4) en solution [réf. à confirmer] 8 .
Que faire en cas de déversement d’acide chlorhydrique ?
Le sol des locaux sera imperméable et formera une cuvette de rétention afin qu’en cas de déversement, les solutions aqueuses d'acide chlorhydrique nepuissent se répandre au dehors. Mettre le matériel électrique et non-électrique, y compris l’ éclairage et la ventilation, en conformité avec la réglementation concernant les atmosphèresexplosives.
Est-ce que l'acide chlorhydrique est un bon réactif acide ?
Ces propriétés, alliées au fait qu'il est disponible comme réactif pur, font de l'acide chlorhydrique un très bon réactif acide ou un très bon acide pour le titrage de solutions basiques de concentrations inconnues.
Quelle est la production d'acide chlorhydrique ?
La production d'acide chlorhydrique avoisine à l'heure actuelle les vingt millions de tonnes par an (estimation en légère augmentation). Les propriétés physiques de l'acide chlorhydrique, telles que les points d'ébullition ou de fusion, dépendent de la concentration ou de la molarité d'HCl en solution aqueuse.
Comment calculer la masse de l'acide chlorhydrique ?
. Et ca de tonne m=1.17*0.400=0.468g.
Quel volume d'acide chlorhydrique ?
Quel est l'équation bilan de l'acide chlorhydrique ?
. La réaction globale est la suivante: Na+ + OH- + H+ + Cl- <--> H2O + NaCl (sel de table).
Pourquoi il ne faut pas verser de l'acide dans l'eau ?
. Parmi les réactions les plus connues, il y a celle provoquée par l'eau. Les acides sont des substances hydroréactives et leur mélange avec l'eau dégage de la chaleur et des vapeurs corrosives.
. Des projections de liquide corrosif peuvent aussi survenir.
|
Calculs sur les concentrations
Calculer la masse d'acide nitrique dans 125 g d'une Calculer le volume d'une solution d'acide chlorhydrique à 32,14 ( ρ = 1,16 g/ml) qu'on peut obtenir à |
|
Correction HCl (ece) - pcpagnol
On dispose d'un flacon d'acide chlorhydrique à 23 en masse de soluté apporté La solution masse volumique de la solution à 23 ρ = 1,19 g·cm-3 |
|
ACIDE CHLORHYDRIQUE - Astrosurf
Masse volumique ou densité C Concentration molaire en mole/L pH Potentiel d' hydrogène m Masse en g Exemple : acide chlorhydrique à 37 , densité = 1, |
|
Acide chlorhydrique - Association Toxicologie-Chimie
Formule brute : HCl, (H2O)n Masse Molaire : 36,47 g mol-1 remarque : pour HCl, et non HCl, (H2O)n Origines : Constituant du suc gastrique produit par les |
|
Dosage dune solution dacide chlorhydrique concentrée
On veut connaître la concentration molaire c0 de cette solution La solution S0 a une masse volumique ρ0 = 1160 g L-1 Le pourcentage massique de la solution |
|
Ou acide chlorhydrique - INRS
L'acidification de l'eau de boisson par l'acide chlorhydrique jusqu'à pH 2 provoque, chez le rat exposé pendant 21 semaines, une baisse du volume de l' urine |
|
Travail dirigé 5 : La concentration dune solution - Unité AFO
Calculer la concentration molaire d'une solution d'acide chlorhydrique HCl sachant que sur l'étiquette on de soluté et la masse volumique de cette solution |
|
Exercice 2 : Fabrication et dosage dune solution dacide chlorhydrique
Fabrication et dosage d'une solution d'acide chlorhydrique Version adaptée : 1) Déterminer la masse volumique du chlorure d'hydrogène gazeux à la |