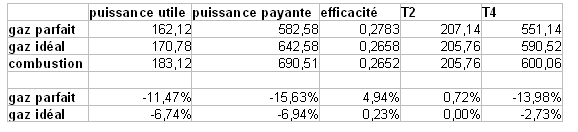
loi des gazs parfaits unités
|
3 Propriétés des gaz
Un gaz qui obéit à ces lois est appelé gaz parfait ou gaz idéal Les trois lois se réduisent à une loi générale des gaz parfaits qui s'applique à tous les |
|
Chapitre 1 Gaz parfait (rappels de L2)
Ce chapitre concerne la définition et l'étude des propriétés des gaz dits parfaits Comme on le verra le concept de gaz parfait est une idéalisation dont |
|
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
En astrophysique on préfère introduire la masse volumique ρ = nM/V où M est la masse molaire On écrit la loi de comportement adiabatique sous la forme P = aργ |
|
Chapitre III Gaz parfaits
Enoncé de la loi : A température constante le produit de la pression d'une masse gazeuse par son volume est constant (cette loi est d'origine |
|
La loi des gaz parfaits
C'est la température absolue ou températures Kelvin (unité : le Kelvin K) La valeur de k' est constante à une pression donnée Référence: bc-1-loidesgaz pdf |
|
Loi des gaz parfaits : p V = n R T
Cette formule relie p : la pression d'un gaz en Pascal (Pa) V : le volume qu'occupe le gaz en mètre cube (m³) n : le nombre de mole que contient ce |
Quelle est l'unité de R ?
R est la constante des gaz parfaits (R = 8,31 J·K -1·mol -1).
Cette constante étant exprimée dans le Système International, cela impose que toutes les autres grandeurs de cette relation soient elles aussi dans le système international.Quelle est l'unité de la constante des gaz parfaits ?
La constante des gaz parfaits est égale à 8,314 kPa⋅L/mol⋅K 8 , 314 kPa ⋅ L / mol ⋅ K .
Il est toutefois important que les unités de mesure des différentes caractéristiques soient respectées afin de pouvoir utiliser cette constante.C'est quoi r dans PV nRT ?
Il existe une loi des gaz parfaits qui s'écrit sous la forme PV = nRT, où P est la pression d'un gaz (en pascals), V le volume occupé par le gaz (en m3), n la quantité de matière (en moles), R la constante universelle des gaz parfaits (8,3144621 J/K/mol), et T est la température (en kelvins).
- Loi des gaz parfaits - Points clés
La température et le volume ont une relation proportionnelle.
Plus l'un augmente, plus l'autre augmente.
Le nombre de moles et le volume ont une relation proportionnelle.
La pression et le volume ont une relation inverse.
|
Chapitre 15 Modèle du gaz parfait
Il faut bien veiller à respecter les unités lors de l'application de l'équation d On parle d'équation d'état du gaz parfait ou encore de loi du gaz parfait. |
|
Premier et Second Principes
On écrira que l'énergie interne e et l'enthalpie h par unité de masse sont pour un gaz parfait or on a toujours la loi des gaz parfaits PV = nmolRT d'o`u 0 = ... |
|
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
En astrophysique on préfère introduire la masse volumique ρ = nM/V où M est la masse molaire. On écrit la loi de comportement adiabatique sous la forme P = aργ. |
|
Objectif général de lexpérience 1 Introduction
27 sept. 2017 Le premier objectif de l'expérience est de vérifier la loi de Boyle-Mariotte qui relie la pression et le volume d'un gaz parfait à température ... |
|
RISQUES LIÉS AUX ÉQUIPEMENTS SOUS PRESSION
Des exemples illustrant des niveaux de pression sont présentés dans la fiche 1. 2 • RAPPELS THÉORIQUES. 2.1. DÉFINITIONS. 2.2. LOI DES GAZ PARFAITS. Un gaz réel |
|
Terminale générale - Gaz parfaits et thermodynamique - Fiche de
Loi de Boyle-Mariotte. Pour un gaz parfait lors d'une transformation isotherme : PV=constante e. Equation des gaz parfaits. Pour un gaz parfait : PV=nRT f |
|
Biophysique de1 letat gazeux
Unités : • Le Pascal ou N/m2: Pa. Dim: MLT-2.L-2= ML-1T-2. • Le cm de mercure Si on applique la loi des gaz parfaits: ▫ Au gaz i : PVi = ni RT Vi =ni RT. |
|
Les Maths et la Chimie peuvent faire bon ménage …. PLAN (10h TD)
16 janv. 2020 Loi des gaz parfaits. 2. Importance des unités. 3. Représentation graphique. 4. Formule logarithmique. 5. Intégrale d'une fonction. 6. Exercices ... |
|
Chapitre III. Gaz parfaits
RT ou encore c'est un gaz qui obéit rigoureusement aux trois lois. MARIOTTE Pour l'unité U.D.M d'un gaz parfait |
|
3. Propriétés des gaz
Un gaz qui obéit à ces lois est appelé gaz parfait ou gaz idéal. Les trois lois se réduisent à une loi générale des gaz parfaits qui En exprimant la pression ... |
|
Le système international Les unités de base
Les unités dérivées. Superficie. Mètre carré 3/Loi des gaz parfaits :P.V = n.R.T. R = Constante des gaz parfaits. Donner la dimension et unité de R? |
|
P.V = n.R.T P.V = m.r.T P.V = n.R.T P.V = m.r.T
CHALEUR TRAVAIL & ENERGIE INTERNE DES GAZ PARFAITS L'état d'un gaz parfait est décrit par ses trois variables d'état: ... LOI DE JOULES. |
|
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Loi des gaz parfaits : PV = nRT. Energie interne : U = nCvT. Enthalpie : H = nCpT. Relation de Mayer : Cp ? Cv = R. R est la constante des gaz parfaits |
|
I. Équilibre homogène
des gaz parfaits : sont des pressions partielles à l'équilibre leur unité est atm. ... V est le volume du gaz |
|
Chapitre III. Gaz parfaits
ou encore c'est un gaz qui obéit rigoureusement aux trois lois. MARIOTTE Pour l'unité U.D.M d'un gaz parfait |
|
GAZ PARFAIT – MASSE VOLUMIQUE
On démontrera dans le cours de thermodynamique physique que l'équation d'état des gaz parfaits peut se mettre sous la forme : PV nRT. = Attention aux unités |
|
Premier et Second Principes
On écrira que l'énergie interne e et l'enthalpie h par unité de masse sont pour un gaz parfait e = cvT et h = cpT avec cp/cv = ? |
|
TD1 Corrigé : Équations aux dimensions et Ordres de grandeur
d'après la loi des gaz parfaits : PV = nRT. Complément : l'unité SI de R s'écrit : ... K?1 avec 1J = 1kg.m2.s?2 unité SI d'énergie. |
|
3. Propriétés des gaz
Les trois lois se réduisent à une loi générale des gaz parfaits qui En exprimant la pression en d'autres unités on obtient encore:. |
|
Chapitre III Gaz parfaits
Enoncé de la loi : A pression constante l'augmentation de volume d'un gaz parfait (dilatation ou détente) est proportionnelle à la température absolue |
|
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Loi des gaz parfaits : PV = nRT Energie interne : U = nCvT Enthalpie : H = nCpT Relation de Mayer : Cp ? Cv = R R est la constante des gaz parfaits |
|
La loi des gaz parfaits - Meine Mathe
Envisageons une transformation à pression constante d'un gaz d'un état 1 vers un état 2 : Soient T1 et V1 la température absolue et le volume à l'état 1 Soient |
|
Chapitre 15 Modèle du gaz parfait
Il faut bien veiller à respecter les unités lors de l'application de l'équation d'état du gaz : V majuscule en mètre cube (m3) et P majuscule en pascal (Pa) |
|
Les gaz - La chimie
L'équation des gaz parfaits • on peut mettre les trois lois ensemble: • l'équation des gaz parfaits: PV = nRT • R est la constante des gaz parfaits |
|
Loi des gaz parfaits - Wikipédia
Les lois des gaz décrivent le comportement des gaz lorsqu'on maintient constant l'une des variables d'état – volume pression ou température – et que l'on |
|
LOI DES GAZ PARFAITS - Lycée Cézanne
Lycée Paul Cézanne – 2005 - TP Physique n°13 LOI DES GAZ PARFAITS OBJECTIFS: • Montrer que la pression d'un gaz est proportionnelle à sa température |
|
Gaz parfait : Cours et exercices corrigés - F2School
Enoncé de la loi :Seconde forme de la loi de MARIOTTE On désigne par 'v' le volume d'une unité de masse de gaz parfait et par 'Vm' le volume molaire |
|
Chapitre 1 Gaz parfait (rappels de L2)
Ce chapitre concerne la définition et l'étude des propriétés des gaz dits parfaits Comme on le verra le concept de gaz parfait est une idéalisation dont |
|
Loi des gaz parfaits : p V = n R T - sciences
Loi des gaz parfaits : p V = n R T Cette formule relie p : la pression d'un gaz en Pascal (Pa) V : le volume qu'occupe le gaz en mètre cube (m³) |
Quelle est l'unité de la constante des gaz parfaits ?
La constante des gaz parfaits est égale à 8,314 kPa?L/mol?K 8 , 314 kPa ? L / mol ? K . Il est toutefois important que les unités de mesure des différentes caractéristiques soient respectées afin de pouvoir utiliser cette constante.C'est quoi CP et CV ?
Il s`agit de la quantité de chaleur à fournir à un système pour élever sa température de 1°C. On distingue Cp, capacité calorifique à pression constante et Cv, à volume constant.C'est quoi le R dans PV nRT ?
Il existe une loi des gaz parfaits qui s'écrit sous la forme PV = nRT, où P est la pression d'un gaz (en pascals), V le volume occupé par le gaz (en m3), n la quantité de matière (en moles), R la constante universelle des gaz parfaits (8,3144621 J/K/mol), et T est la température (en kelvins).- L'équation du gaz parfait s'exprime ainsi : P V = n R T où est la pression, le volume, le nombre de moles, la constante des gaz et la température.
Quel est l'unité de la constante des gaz parfaits ?
. On rappelle que 1 Torr = 1 mmHg , qu'un bar vaut 10 5 Pa , qu'une atmosphère est égale à 1 , 013 10 5 Pa et qu'une calorie vaut 4 , 18 Joules .
Quel est la formule des gaz parfaits ?
Quelle est la valeur de la constante R ?
Comment utiliser la loi des gaz parfait ?
. On peut donc l'utiliser pour trouver une variable inconnue lorsque les trois autres sont connues.
|
PV = nRT - Matthieu Barreau
et pourtant volume et pression ont varié • LOI DE JOULES: L'ENERGIE INTERNE D'UN GAZ PARFAIT N'EST |
|
Température, pression, gaz parfaits - Laboratoire de physique des
unité Pascal 1 Pa = 1 Nm -2 Pression de l' L'équation des gaz parfaits relie P, V et T: P V = n R T P est la pression (Pa) V/T = cte V ∝ T (loi de Charles) |
|
La loi des gaz parfaits
Sur le manomètre on peut lire la pression du gaz contenu dans la séringue en abscisse T C'est la température absolue ou températures Kelvin (unité : |
|
Thermodynamique et gaz parfaits
Gaz parfaits, description thermique → relier quantitativement la chaleur à l' énergie → unité commune Distribution des vitesses au sein d'un gaz : loi |
|
Lois physiques des gaz - Reanesth
14 fév 2013 · Unités de mesure, état gazeux ○ Connaître Lois des gaz parfaits (Boyle- Mariotte, Gay-Lussac, Charles, Loi sur la compressibilité des gaz |
|
GAZ PARFAIT – MASSE VOLUMIQUE
On utilise systématiquement les unités du système international : la température T en kelvin (K), la pression en pascal Un mélange idéal de gaz parfaits est un mélange de gaz parfaits tel qu'il peut être considéré lui-même (loi de Dalton) |
|
Chapitre 3 LES GAZ PARFAITS : EXEMPLES DE CALCULS DE
Loi des gaz parfaits : PV = nRT Energie interne : U = nCvT Enthalpie : H = nCpT Relation de Mayer : Cp − Cv = R R est la constante des gaz parfaits, Cv et Cp |
|
Les gaz - La chimie
unités pour la pression: • la pression la loi d'Avogadro dit aussi que, à pression et à température la loi des gaz parfaits permet de déterminer la masse |
|
Le mod`ele du gaz parfait et ses limitations - Les Pages
La théorie cinétique permet d'établir l'équation d'état des gaz parfaits `a partir uniquement de o`u kB est la constante de Boltzmann qui sera déterminée par un choix judicieux d'unité pression partielle pk suit la loi des gaz parfaits |
















![TD3 - corr[1] - Fichier PDF TD3 - corr[1] - Fichier PDF](https://guy-chaumeton.pagesperso-orange.fr/images09/imgD.jpg)




![TD3 - corr[1] - Fichier PDF TD3 - corr[1] - Fichier PDF](https://jeretiens.net/wp-content/uploads/2016/05/nombre_avogadro.jpg)








 Cours Et TD Thermodynamique - telechargez pdf PDF](+52????️) Cours Et TD Thermodynamique - telechargez pdf](https://i.ytimg.com/vi/_GeAqHdczgg/maxresdefault.jpg)